2. 河南农业大学生命科学学院, 郑州 450002;
3. CAAS-ICRAF农用林业与可持续畜牧业联合实验室, 北京 100193;
4. 东北农业大学, 食品安全与营养协同创新中心, 哈尔滨 150030
2. College of Life Science, Henan Agricultural University, Zhengzhou 450002, China;
3. CAAS-ICRAF Joint Laboratory on Agroforestry and Sustainable Animal Husbandry, Beijing 100193, China;
4. Synergetic Innovation Center of Safety and Nutrition, Northeast Agricultural University, Harbin 150030, China
乳腺生长发育的研究、泌乳机制的研究及乳腺生物反应器的研究都离不开体外培养乳腺上皮细胞作为研究模型[1, 2, 3]。乳腺上皮细胞的建系是其他研究工作的基础,而且乳腺上皮细胞不是永生的,因此人们在细胞水平上进行了大量的研究。过去已经报道过的牛乳腺上皮细胞系主要包括BMEC+H[1]、MAC-T[2]、PS-BME[3]、BME-UV[4]、L-1[5]等。
中国荷斯坦奶牛是我国主要的奶牛品种,目前关于中国荷斯坦奶牛乳腺上皮细胞体外培养的研究较少,且缺乏高效培养方法的报道。奶牛乳腺上皮细胞体外培养方法主要包括酶消化法、机械破碎法、组织块培养法和乳汁分离法[6]。机械破碎法优点是操作简单、试验成本低、细胞迁出快,缺点是对细胞的破坏性大,本文通过一些细节上的改进,旨在建立一种高效的奶牛乳腺上皮细胞体外培养方法,并确定激素及细胞因子诱导乳腺上皮细胞合成β-酪蛋白的能力。
1 材料与方法 1.1 材料 1.1.1 主要试剂及耗材DMEM/F12、0.25%胰蛋白酶-乙二胺四乙酸(trypsin-EDTA)、抗菌-抗真菌剂(Antibiotic-Antimycotic)、GlutaMAXTM、胎牛血清(fetal bovine serum,FBS)均为Gibco产品;CCK-8细胞增殖检测试剂盒为Dojindo公司产品;二甲基亚砜(DMSO)为Sigma公司产品;Trizol试剂为Invitrogen公司产品;鼠源的角蛋白18抗体为Abcam公司产品;山羊抗小鼠免疫球蛋白G(IgG)二抗为EarthOx公司产品;35 mm培养皿为Corning公司产品;反转录试剂盒(PrimeScript RT reagent Kit with gDNA Eraser)、实时定量PCR试剂盒(SYBR Green ExTaqTM Ⅱ)均为TaKaRa公司产品。
1.1.2 培养液乳腺上皮细胞的原代生长培养液:DMEM/F12+20%FBS+1×谷氨酰胺;乳腺上皮细胞的传代生长培养液:DMEM/F12+10%FBS+1×谷氨酰胺;冻存培养液:DMEM/F12+20%FBS+10%DMSO。8种不同诱导培养液,分别在DMEM/F12中添加:1)1 μg/mL地塞米松+5 μg/mL催乳素+5 μg/mL胰岛素(DPI-1组),2)1 μg/mL地塞米松+10 μg/mL催乳素+5 μg/mL胰岛素(DPI-2组),3)5 μg/mL β-雌二醇(E组),4)10 ng/mL类胰岛素生长因子Ⅰ(insulin-like growth factor Ⅰ,IGF-Ⅰ,10-IGF-Ⅰ组),5)100 ng/mL IGF-Ⅰ(100-IGF-Ⅰ组),6)200 ng/mL IGF-Ⅰ(200-IGF-Ⅰ组),7)400 ng/mL IGF-Ⅰ(400-IGF-Ⅰ组),8)1 000 ng/mL IGF-Ⅰ(1000-IGF-Ⅰ组)。
1.2 方法 1.2.1 奶牛乳腺上皮细胞原代培养方法屠宰健康的泌乳中期中国荷斯坦奶牛,无菌条件下取大约4 cm3乳腺组织块放入含有10×Antibiotic-Antimycotic的磷酸盐缓冲液(PBS)的无菌离心管中,37 ℃保温带回实验室。用含1×Antibiotic-Antimycotic的PBS清洗3遍,剪去结缔、脂肪及可见导管组织。样品放入表面皿中剪为1 mm3大小,之后移入15 mL离心管,加入含1×Antibiotic-Antimycotic的PBS,上下颠倒混匀后离心(900 r/min,2 min),倒掉上清,重复清洗直到液体清亮为止。用无菌镊子将组织块直接接种到直径60 mm的培养皿中,组织块间间隔约1 cm,在每个组织块上方滴1滴FBS,促进其贴壁,放入培养箱,6 h后加原代生长培养液。以上是组织块的培养方法,主要是将乳腺组织剪为1 mm3大小的组织块接种于培养皿中培养。机械破碎法是在1 mm3大小组织块的基础上进一步进行机械剪切破碎,使组织呈现黏稠状,PBS重悬,单层纱布过滤,过滤下的液体移入15 mL离心管中,900 r/min离心5 min,倒掉上清,将沉淀的小组织块用原代生长培养液重悬,取350 μL接种到直径35 mm的培养皿中,放入培养箱,6 h后再补加650 μL的原代生长培养液。机械破碎法与组织块培养法的最大区别在于机械破碎法将组织块剪切的更小,可能对组织有一定的机械破坏性,但细胞容易从组织中迁移出来。每日观察2种培养方法获得的细胞的生长状态,待迁移出的细胞长满培养皿的80%时,进行纯化和传代。
1.2.2 乳腺上皮细胞的纯化利用成纤维细胞和乳腺上皮细胞对胰酶的敏感性不同进行纯化。具体方法为先用0.25% trypsin-EDTA消化贴壁细胞,在倒置显微镜下观察,等全部细胞回缩后,添加含FBS的原代生长培养液立即终止消化,并进行吹打,将没有消化下来的细胞继续培养。利用成纤维细胞对胰酶更加敏感,容易脱落的原理进行纯化。经过若干次处理即可得到纯的乳腺上皮细胞。
1.2.3 生长曲线的绘制将纯化的细胞以1×104个/mL的密度接种于24孔板中,每孔300 μL,放入二氧化碳培养箱中。采用细胞计数仪连续8 d测定细胞数。以时间为横坐标,以细胞数为纵坐标,细胞数取3个孔的平均值,绘制细胞生长曲线。
1.2.4 免疫荧光组织化学染色法鉴定乳腺上皮细胞采用免疫荧光组织化学染色法检测培养的乳腺上皮细胞中角蛋白18的表达。待细胞汇合度达到80%时,用PBS冲洗细胞2次。室温下用1 mL甲醇固定30 min。然后用1 mL 0.2% TritonX-100通透处理5 min,PBS冲洗细胞2次。用1 mL含10%鸡血清的PBS(封闭液)封闭30 min。去除封闭液,细胞用一抗,即鼠源的角蛋白18抗体(1 ∶ 100封闭液稀释),室温孵育1 h。PBS冲洗3次,然后用二抗,即山羊抗小鼠IgG(1 ∶ 50封闭液稀释)避光振荡孵育30 min。PBS冲洗3次,荧光显微镜下观察染色结果。选用成纤维细胞作为阴性对照,染色方法相同。
1.2.5 实时定量PCR法检测乳腺上皮细胞β-酪蛋白mRNA的表达提高乳腺上皮细胞的接种密度到1×105个/mL,用不含血清的DMEM/F12培养细胞12 h,使细胞状态一致。然后用8种诱导培养液培养,以DMEM/F12为对照。培养24 h后,弃去培养液,PBS清洗3遍,然后每皿加1 mL Trizol试剂,裂解细胞提取总RNA(操作程序参照Trizol试剂盒说明书)。按照反转录试剂盒说明书进行反转录。在ABI7500上进行实时定量PCR,操作参照实时定量PCR试剂盒说明书进行。数据采用2-△△Ct的方法计算,以甘油醛-3-磷酸脱氢酶为内参基因。实时定量PCR引物序列及参数见表1。
| 表1 实时定量PCR引物序列及参数 Table 1 Sequences and parameters of primers for RT-qPCR |
组织块培养法细胞迁出速度比较缓慢。培养3 d后首先可见成纤维细胞,随后可以观察到乳腺上皮细胞,当细胞汇合度达到80%时进行消化,未消化掉的组织块加培养液继续培养,约15 d后得到大量的乳腺上皮细胞(图1-a、图1-b)。机械分离法在培养7 d后得到大量的乳腺上皮细胞(图1-c、图1-d)。2种培养方法都可以得到成纤维细胞和乳腺上皮细胞混杂生长的原代细胞。仔细观察细胞形态,培养10 d后发现有3种类型的乳腺 上皮细胞(图2),分别是成群生长的铺路石型细胞、独立生长的大圆饼型细胞、内多泡的腺体型细胞。
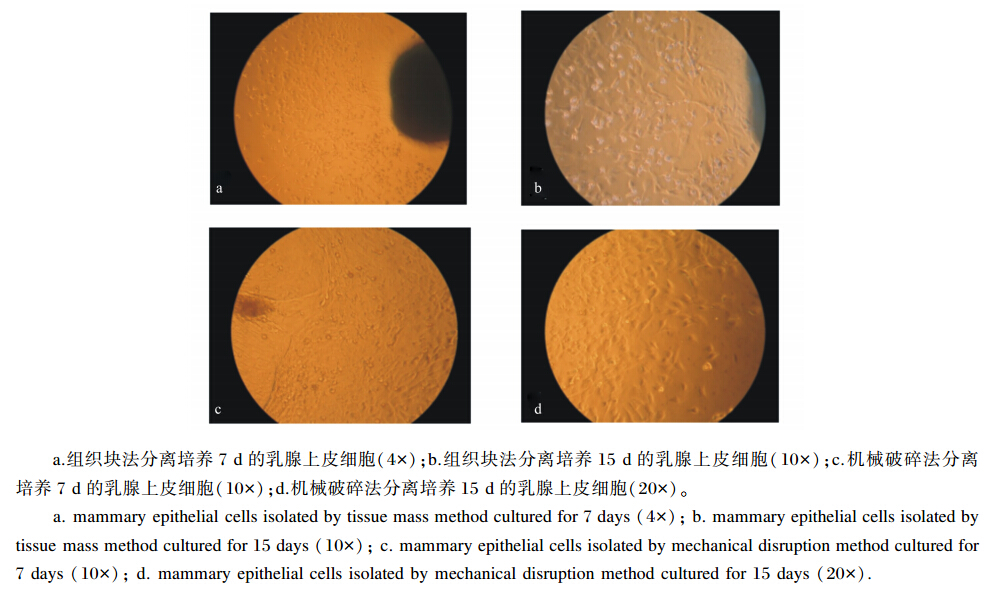 | 图1 原代培养的奶牛乳腺上皮细胞 Fig. 1 Primary culture of bovine mammary epithelial cells |
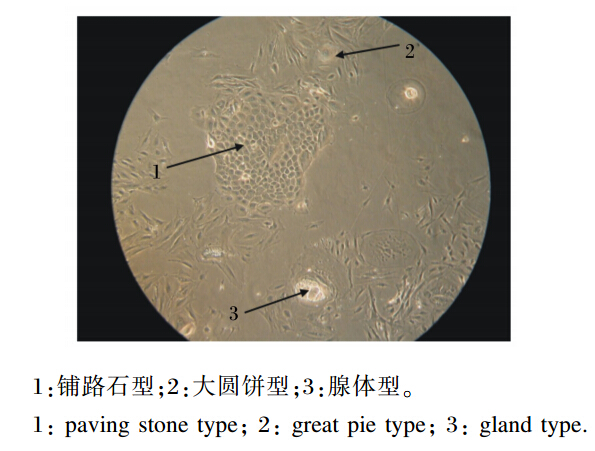 | 图2 3种类型的奶牛乳腺上皮细胞 Fig. 2 Three types of bovine mammary |
未纯化前乳腺上皮细胞和成纤维细胞各自聚集生长,且细胞边界清晰可见(图3-a)。相对于乳腺上皮细胞,成纤维细胞对胰酶更加敏感,消化时先脱壁,利用这个特点经过若干次传代可将成纤维细胞去除,得到纯的呈铺路石状排列的乳腺上皮细胞(图3-b、图3-c)。消化下来的成纤维细胞继续接种培养,形态呈长梭形(图3-d)。
2.3 奶牛乳腺上皮细胞生长曲线生长曲线显示1~2 d为乳腺上皮细胞的潜伏期,3~6 d为指数增长期,之后就进入平台期(图4)。细胞生长曲线呈“S”型,说明培养的乳腺上皮细胞具有正常的增殖能力,适合用于后续的试验研究。
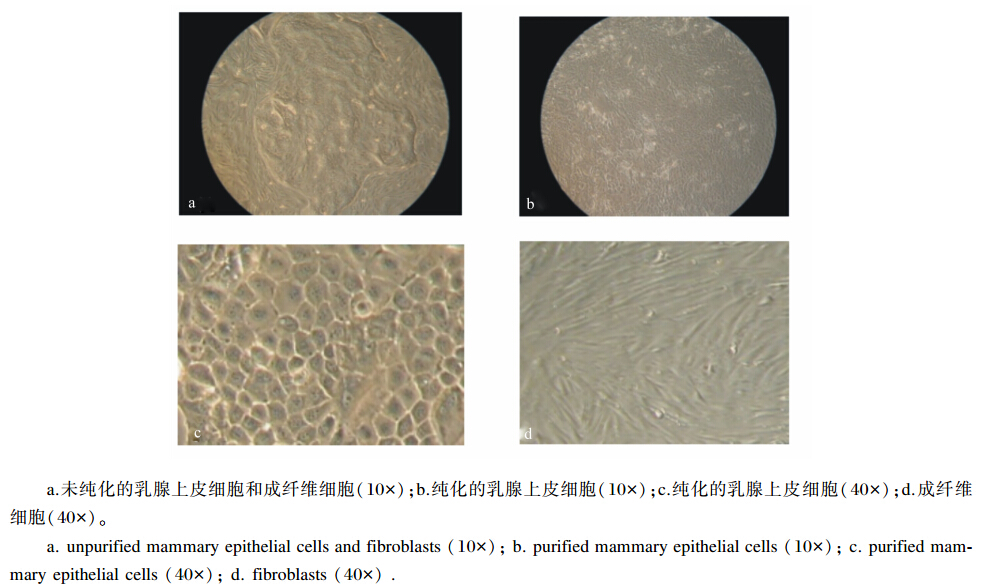 | 图3 奶牛乳腺上皮细胞的纯化 Fig. 3 Purification of bovine mammary epithelial cells |
采用免疫细胞荧光染色法对成纤维细胞、纯化的乳腺上皮细胞及第20代的乳腺上皮细胞进行角蛋白18表达的检测。阴性对照成纤维细胞没有绿色荧光,而纯化的乳腺上皮细胞及第20代的乳腺上皮细胞绿色荧光明显。这表明本次试验分离得到较纯的乳腺上皮细胞,并且传至第20代仍然具有上皮细胞的典型特征。
2.5 奶牛乳腺上皮细胞中β-酪蛋白的诱导表达结果100-IGF-Ⅰ组β-酪蛋白mRNA表达量最高,显著高于除200-IGF-Ⅰ组外的其他各组(P<0.05)(图6),说明在8种激素和细胞因子组合中,100 ng/mL IGF-Ⅰ对奶牛乳腺上皮细胞β-酪蛋白mRNA的诱导表达效果最好。
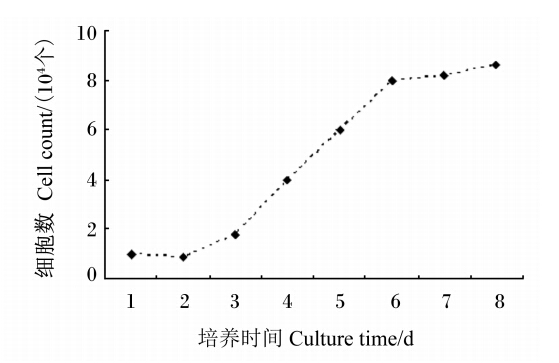 | 图4 奶牛乳腺上皮细胞的生长曲线 Fig. 4 The growth curve of bovine mammary epithelial cells |
奶牛乳腺上皮细胞培养技术应用于许多研究领域,例如泌乳机理[7]、乳成分的生物合成[8]、细 胞与细胞的相互作用[9]、细胞转运蛋白[10]及先天 免疫系统[11]的研究。目前文献报道的奶牛乳腺上皮细胞的培养方法主要集中于组织块培养法[12, 13]和胶原酶消化法[14, 15, 16]。组织块培养法的优点是可以得到大量的细胞,缺点是培养时间长。胶原酶消化法的优点是获得细胞的时间短,但细胞数量少。综合以上方法的优缺点,本试验采用机械分离法,既可以获得大量细胞,培养时间也较短,且不需要用胶原酶消化,节约试验成本。过去也有研究学者报道机械分离法对细胞结构的损伤大[17],但本试验结果表明此方法是可行的,产生差异的原因可能主要是操作细节。机械法分离培养奶牛乳腺上皮细胞主要有几个方面需注意:第一先是取样避免污染,所有器械高压灭菌处理,最好是采用Antibiotic-Antimycotic,即既抗真菌又抗细菌;第二是机械破碎之后要用单层纱布过滤,这样即可以去掉大的组织块,又避免孔隙太小时过滤下来的全是受到损伤的组织碎片;第三是原代培养的乳腺上皮细胞可以使用FBS促使其贴壁,待其完全贴壁之后再添加基础培养液进行培养。
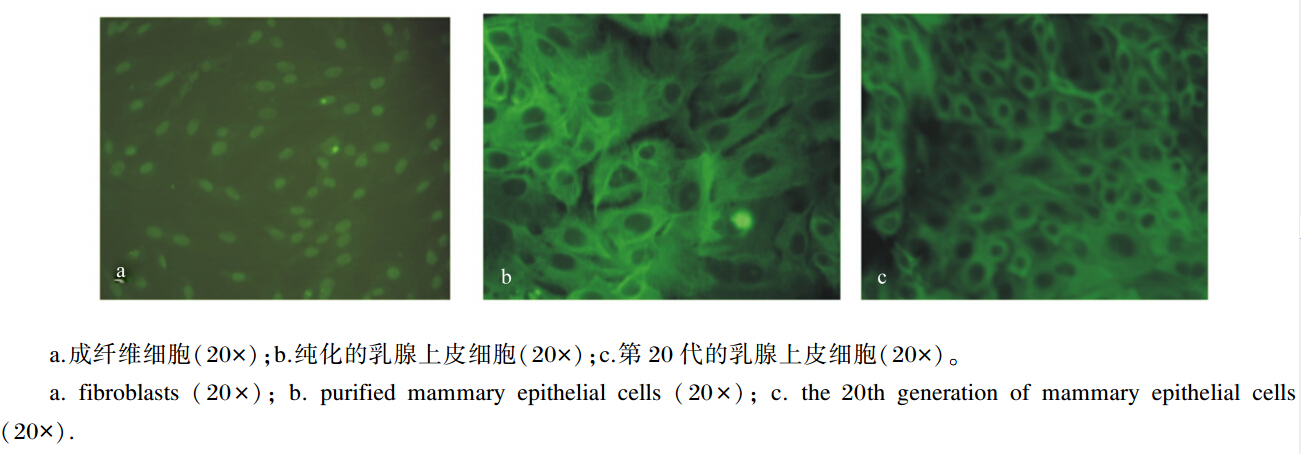 | 图5 荧光显微镜下观察奶牛乳腺上皮细胞角蛋白18的表达 Fig. 5 Keratin 18 expression of bovine mammary epithelial cells observed under fluorescence microscope |
对于奶牛乳腺上皮细胞的纯化,很多文献都报道利用2种细胞对胰酶的敏感性不同进行纯化[13, 18]。本试验也采用此种方法,摸索方法时发现未纯化的2种细胞呈现清晰的生长界线时进行纯化效果好(图3-a),细胞纯化时对消化时间的要求较高。消化过程中高频率观察细胞消化状态,细胞回缩变圆,且有个别成纤维细胞漂起时立即终止消化。纯化后的细胞进行生长曲线的绘制时,形状典型,说明细胞增殖能力正常。
上皮细胞特异性标志物的单克隆抗体被用于鉴别上皮细胞。常用的上皮细胞特异性标志物有角蛋白、上皮细胞膜抗原等单克隆抗体[19]。目前用于奶牛乳腺上皮细胞检测的角蛋白主要包括角蛋白5、角蛋白7、角蛋白8、角蛋白18。本试验选择角蛋白18对纯化后的乳腺上皮细胞及纯化后传至第20代的细胞进行鉴定,结果都呈阳性。这说明本次试验得到的是乳腺上皮细胞,且传至第20代的细胞仍然具有上皮细胞的典型特征。
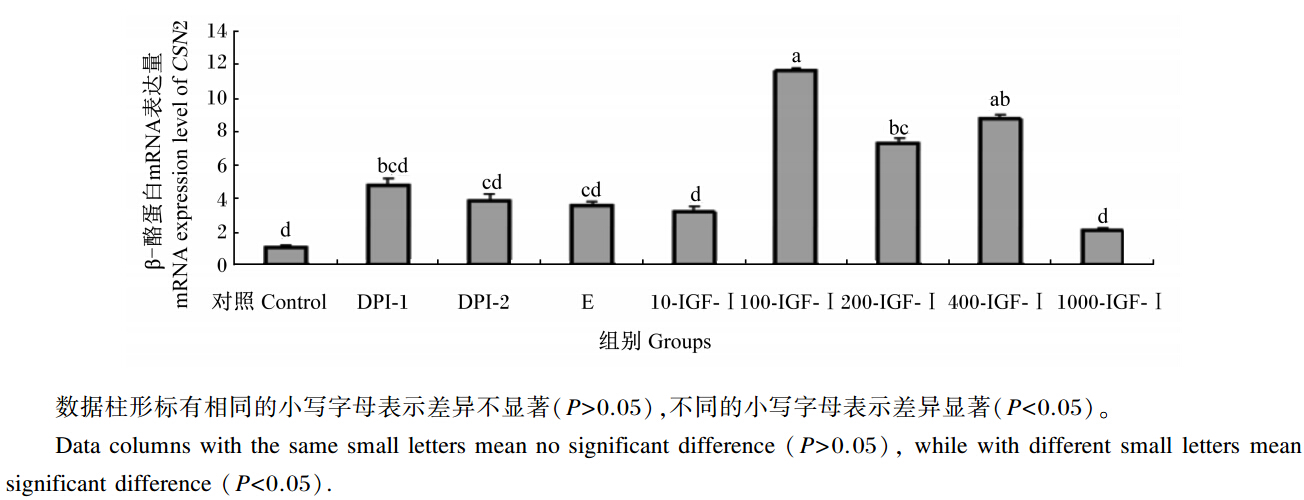 | 图6 不同诱导培养液对奶牛乳腺上皮细胞β-酪蛋白mRNA表达的影响 Fig. 6 Effects of different induced cultured mediums on CNS2 mRNA expression of bovine mammary epithelial cells |
奶牛乳腺发育和乳的合成是受系统激素和局部因子调节的。催乳素和糖皮质激素是分泌型的细胞分化和乳生成的主要调节物[20, 21]。胰岛素具有促进泌乳和DNA合成的作用[22]。雌激素的浓度在妊娠后期逐渐增加,分娩前几天达到峰值。Akers[23]研究发现在乳腺上皮细胞中添加17β-雌二醇可以显著增加催乳素诱导的α-乳白蛋白的表达。作为奶牛乳腺上皮细胞中重要的细胞因子,IGF-Ⅰ通过磷脂酰肌醇3-激酶(PI3K)和丝裂原活化蛋白激酶(MAPK)2个信号通路来调节乳腺上皮细胞的增殖、分化、凋亡与代谢[23]。IGF-Ⅰ通过PI3K/蛋白激酶B(AKT)信号通路,激活下游哺乳动物雷帕霉素靶蛋白(mTOR)信号通路,从而在翻译水平上调节乳蛋白的合成[24]。因此,本试验选择地塞米松、催乳素、胰岛素、β-雌二醇、IGF-Ⅰ为研究对象,使用剂量依据先前的研究报道[12, 25]。牛乳蛋白以酪蛋白为主,β-酪蛋白的mRNA表达水平能很好地反映奶牛乳腺上皮细胞的泌乳功能。本试验中,外源添加IGF-Ⅰ显著提高了β-酪蛋白mRNA的表达,表明一定浓度的IGF-Ⅰ能增强奶牛乳腺上皮细胞合成β-酪蛋白的能力。本试验为后期开展奶牛乳腺发育和泌乳功能研究奠定了基础。
4 结 论① 本试验采用的机械破碎法是一种高效的奶牛乳腺上皮细胞培养方法。
② 100 ng/mL IGF-Ⅰ对细胞中β-酪蛋白mRNA表达的诱导效果最好。
| [1] | LIU H Y,ZHAO K,LIU J X.Effects of glucose availability on expression of the key genes involved in synthesis of milk fat, lactose and glucose metabolism in bovine mammary epithelial cells[J]. PLoS One,2013,8(6):e66092. ( 2) 2)
|
| [2] | MONZANI P S,BRESSAN F F,MESQUITA L G,et al.β-casein gene expression by in vitro cultured bovine mammary epithelial cells derived from developing mammary glands[J]. Genetics and Molecular Research,2011,10(2):604-614. ( 2) 2)
|
| [3] | SPERONI L,WHITT G S,XYLAS J,et al.Hormonal regulation of epithelial organization in a three-dimensional breast tissue culture model[J]. Tissue Engineering Part C:Methods,2014,20(1):42-51. ( 2) 2)
|
| [4] | SCHMID E,FRANKE W W,GRUND C,et al.An epithelial cell line with elongated myoid morphology derived from bovine mammary gland. Expression of cytokeratins and desmosomal plaque proteins in unusual arrays[J]. Experimental Cell Research,1983,146(2):309-328. ( 1) 1)
|
| [5] | HUYNH H T,ROBITAILLE G,TURNER J D.Establishment of bovine mammary epithelial cells (MAC-T):an in vitro model for bovine lactation[J]. Experimental Cell Research,1991,197(2):191-199. ( 1) 1)
|
| [6] | GIBSON C A,VEGA J R,BAUMRUCKER C R,et al.Establishment and characterization of bovine mammary epithelial cell lines[J]. In Vitro Cellular & Developmental Biology:Animal,1991,27(7):585-594. ( 1) 1)
|
| [7] | ZAVIZION B,VAN DUFFELEN M,SCHAEFFER W,et al.Establishment and characterization of a bovine mammary myoepithelial cell line[J]. In Vitro Cellular & Developmental Biology:-Animal,1996,32(3):149-158. ( 1) 1)
|
| [8] | GERMAN T,BARASH I.Characterization of an epithelial cell line from bovine mammary gland[J]. In Vitro Cellular & Developmental Biology:Animal,2002,38(5):282-292. ( 1) 1)
|
| [9] | 王加启,反刍动物营养学研究方法[M]. 北京:现在教育出版社,2011:225-226. ( 1) 1)
|
| [10] | GROVES T D D,LARSON B L.Preparation of specifically labeled milk proteins using bovine mammary-cell cultures[J]. Biochimica Et Biophysica Acta:General Subjects,1965,104(2):462-469. ( 1) 1)
|
| [11] | CLOSE M J,HOWLETT A R,ROSKELLEY C D,et al.Lactoferrin expression in mammary epithelial cells is mediated by changes in cell shape and actin cytoskeleton[J]. Journal of Cell Science,1997,110(22):2861-2871. ( 1) 1)
|
| [12] | KATZ E,STREULI C H.The extracellular matrix as an adhesion checkpoint for mammary epithelial function[J]. International Journal of Biochemistry & Cell Biology,2007,39(4):715-726. ( 2) 2)
|
| [13] | PAYE J M,AKERS R M,HUCKLE W R,et al.Autocrine production of insulin-like growth factor-I (IGF-Ⅰ) affects paracellular transport across epithelial cells in vitro[J]. Cell Communication and Adhesion,2007,14(2/3):85-98. ( 2) 2)
|
| [14] | GRIESBECK-ZILCH B,MEYER H H D,KUHN C H,et al.Staphylococcus aureus and Escherichia coli cause deviating expression profiles of cytokines and lactoferrin messenger ribonucleic acid in mammary epithelial cells[J]. Journal of Dairy Science,2008,91(6):2215-2224. ( 1) 1)
|
| [15] | HU H,WANG J Q,BU D,et al.In vitro culture and characterization of a mammary epithelial cell line from Chinese Holstein dairy cow[J]. PLoS One,2009,4(11):e7636. ( 1) 1)
|
| [16] | 弓超,王凌云,周欢敏.牛乳腺上皮细胞体外分离和培养[J]. 动物医学进展,2011,32(7):66-71. ( 1) 1)
|
| [17] | NOVARO V,ROSKELLEY C D,BISSELL M J.Collagen-Ⅳ and laminin-1 regulate estrogen receptor αexpression and function in mouse mammary epithelial cells[J]. Journal of Cell Science,2003,116(14):2975-2986. ( 1) 1)
|
| [18] | 佟慧丽,尹德云,李庆章,等.奶山羊乳腺上皮细胞系的建立[J]. 东北农业大学学报,2008,39(8):104-109. ( 1) 1)
|
| [19] | 李吉霞,葛秀国,王文秀,等.牛乳腺上皮细胞的分离培养[J]. 黑龙江畜牧兽医,2012(4):4-6. ( 1) 1)
|
| [20] | 宋亚南,陈志伟,刘东武.牛乳腺上皮细胞体外培养体系研究进展[J]. 生命科学仪器,2008,6:3-8. ( 1) 1)
|
| [21] | PANTSCHENKO A G,YANG T J.Mitogenic responsiveness of caprine mammary epith elial cells to endocrine and cytokine factors[J]. Endocrine,1999,10(2):123-130. ( 1) 1)
|
| [22] | 薛庆善.体外培养的原理与技术[M]. 北京:科学出版社,2001:387. ( 1) 1)
|
| [23] | AKERS R M.Lactation and the mammary gland ames[M]. Iowa:Wiley-Blackwell,2002:45-78. ( 2) 2)
|
| [24] | NEVILLE M C,MCFADDEN T B,FORSYTH I.Hormonal regulation of mammary differentiation and milk secretion[J]. Journal of Mammary Gland Biology and Neoplasia,2002,7(1):49-66. ( 1) 1)
|
| [25] | CIFRIAN E,GUIDRY A J,O'BRIEN C N.Bovine mammary teat and ductal epithelial cell cultures[J]. American Journal of Veterinary Research,1994,55:239-246. ( 1) 1)
|
| [26] | SAMANI A A,YAKAR S,LEROITH D,et al.The role of the IGF system in cancer growth and metastasis:overview and recent insights[J]. Endocrine Reviews,2007,28(1):20-47. ( 0) 0)
|
| [27] | BURGOS S A,CANT J P.IGF-1 stimulates protein synthesis by enhanced signaling through mTORC1 in bovine mammary epithelial cells[J]. Domestic Animal Endocrinology,2010,38(4):211-221. ( 0) 0)
|
| [28] | SHAO Y,WALL E H,MCFADDEN T B,et al.Lactogenic hormones stimulate expression of lipogenic genes but not glucose transporters in bovine mammary gland[J]. Domestic Animal Endocrinology,2013,44(2):57-69. ( 0) 0)
|




