2. 广东粤海饲料集团公司, 湛江 524002
during Different Growth Stages
2. Guangdong Yuehai Feed Group Co., Ltd., Zhanjiang 524002, China
凡纳滨对虾(Litopenaeus vannamei)原产于南太平洋沿岸的暖水水域,分类学上隶属节肢动物门(Arthropoda)甲壳纲(Crustacea)软甲亚纲(Malacostraea)十足目(Decapoda)游泳亚目(Natantia)对虾科(Penaidas)对虾属(Penaeus)白对虾亚属(Lito-peuaeus),是世界上养殖最多、产量最大的三大虾种之一,1988年由中国科学院海洋研究所引进我国大陆。20世纪90年代以来,我国开展了对凡纳滨对虾的人工繁殖研究,并取得了成功[1]。随后南方的广东、海南、广西、福建沿海地区及北方的山东、辽宁等地区大规模养殖。2012我国凡纳滨对虾养殖总产量达145.3万t,占全国对虾养殖总量的55.2%[2]。现在凡纳滨对虾已成为三大对虾的首选品种,也是目前世界上养殖单产最高的对虾品种[3, 4]。
有关对虾蛋白质营养的研究很多,Smith等[5]用不同体重的凡纳滨对虾进行试验,结果表明凡纳滨对虾的蛋白质需要量为30%;李广丽等[6]用鱼粉和豆粕为蛋白质源研究了初始体重为0.45 g的凡纳滨对虾的蛋白质需要,结果表明饲料蛋白质水平为44.12%,能量蛋白质比为33.0 kJ/g时凡纳滨对虾生长最快,饲料系数最低;刘立鹤等[7]用不同蛋白质水平的饲料投喂初始体重为0.3 g的凡纳滨对虾,结果表明凡纳滨对虾的生长与饲料蛋白质水平具有显著的相关性,但当饲料中粗蛋白质含量达到36%后,其增重效果不再明显。研究认为,凡纳滨对虾饲料中蛋白质水平的下限在36.0%左右,中期和后期饲料蛋白质水平分别为48.3%和46.9%时可获得最佳的生长效果[5]。黄凯等[8]以明胶和酪蛋白为蛋白质源配制了蛋白质水平为28%~48%的5种饲料,分别在盐度为2‰和28‰的水体中养殖初始体重为0.011 g的凡纳滨对虾,结果发现对虾的蛋白质需要量随水体盐度的增加而增加,在盐度为2‰的水体中对虾的蛋白质需要量为26.7%,在盐度为28‰的水体中对虾的蛋白质需要量为33.0%。但是,这并不是说凡纳滨对虾的生长在低盐度水体中比在高盐度水体中快,相反地,在相同饲料蛋白质水平下,凡纳滨对虾的生长在高盐度水体中比在低盐度水体中显著加快。
尽管蛋白质营养是研究对虾营养最重要和成果最多的领域,但比较不同生长阶段凡纳滨对虾蛋白质需要量的研究不多。由于蛋白质的质量(如蛋白质源和氨基酸组成)、养殖环境条件(水温、溶氧、盐度、水质等)和研究对象规格等的差异,研究结果也不尽相同。因此,本试验以凡纳滨对虾为研究对象,拟研究其在幼虾阶段和养成阶段的蛋白质需要量,以期为研制适应不同生长阶段凡纳滨对虾生长的饲料提供科学依据,从而促进凡纳滨对虾养殖业的可持续发展。
1 材料与方法 1.1 试验饲料以鱼粉、酪蛋白、明胶和小麦蛋白粉为主要蛋白质源,鱼油、豆油和大豆卵磷脂为主要脂肪源,用明胶和酪蛋白调整饲料中粗蛋白质含量,配制蛋白质水平分别为29.31%、33.19%、37.11%、41.45%、45.58%和49.03%的6种试验饲料。试验饲料组成及营养水平见表1。所有原料粉碎后过60目筛并按比例混合均匀,维生素和矿物质等微量组成采用逐级扩大法混合,然后加入鱼油、豆油和大豆卵磷脂以及水混合均匀,用F-26型双螺杆挤条机压制成粒径为1.0和1.5 mm的饲料,90 ℃烘箱中熟化30 min,自然风干后密封放入-20 ℃冰箱中保存备用。
1.2 试验对象及饲养管理养殖试验在广东粤海饲料集团东海岛试验基地进行,虾苗来源于粤海虾苗场孵化的进口1代苗。由于试验对象规格需求不同,试验1(幼虾阶段养殖试验)与试验2(养成阶段养殖试验)并非同时进行。正式试验前先将所需虾苗暂养于室外水泥池(2 m×2 m×1 m)中,待虾苗长至接近试验所需规格时,将其转入正式试验的室内养殖系统(300 L圆型玻璃钢桶)中继续暂养1周。暂养期间,试验1所用对虾根据虾苗规格先后投喂丰年虫、虾片、粤海牌南美白对虾开口料及0号料(粗蛋白质含量42.0%,粗脂肪含量7.5%);继续生长到试验2所需规格的对虾投喂粤海牌南美白对虾2号料(粗蛋白质含量40.0%,粗脂肪含量7.0%)。试验分组前24 h虾苗停止喂食,挑选体质健壮、规格基本一致的虾苗进行试验。试验1每桶放养40尾对虾,试验2每桶放养30尾对虾,每种饲料均设3个重复(桶)。试验1和试验2所用对虾初始体重分别为(0.52±0.01) g和(7.93±0.03) g。
| 表1 试验饲料组成及营养水平(干物质基础) Table 1 Composition and nutrient levels of experimental diets (DM basis) |
试验开始后2周内若发现有死虾,及时捞出称重,并补充相同大小的对虾;2周以后若有死虾,捞出称重并做好记录。试验1和试验2的养殖期分别为56和42 d。试验期间每天于07:00、11:00、17:00和21:00各投喂1次,投喂1 h后观察对虾的摄食情况,并根据摄食情况适当调整投喂量。试验用水为经砂滤、沉淀后的海水,试验期间连续充气,水温为(26.7±1.3) ℃,水体pH为7.7±0.1,盐度为(19.4±1.7)‰,溶氧浓度>6.0 mg/L,氨氮浓度≤0.05 mg/L。试验1前期每2天换水1次,中、后期每天换水,每日换水量占养殖桶容积的70%以上;试验2期间每天换水1次,换水量占养殖桶容积的70%以上。
1.3 样品采集试验结束后饥饿24 h后,称重并记录尾数,计算增重率(weight gain rate,WGR)、特定生长率(specific growth rate,SGR)、存活率(survival rate,SR)、饲料系数(feed conversion ratio,FCR)及蛋白质效率(protein efficiency ratio,PER)。每桶随机取3~5尾虾,于-20 ℃冰箱中保存,用于全虾常规营养成分分析。每桶另随机取10尾虾,单独测量体长、体重后,于第5步足基部血窦取血,盛于1.5 mL离心管中于4 ℃冰箱放置过夜后,5 000 r/min离心10 min,取上清液置于-80 ℃冰箱中保存,用于血清生化指标测定。取血后的虾剥离肝胰腺并称重、记录数据,用与计算肝体指数(hepatosomatic index,HSI);剩余部分取肌肉于-20 ℃冰箱保存,用于肌肉常规营养成分分析。试验前、后分别测量对虾的体长与体重,用于计算肥满度(condition factor,CF)。
1.4 指标测定饲料、全虾及肌肉常规营养成分分析:水分含量的测定采用105 ℃常压干燥法;粗蛋白质含量的测定采用微量凯氏定氮法;粗脂肪含量的测定采用索氏抽提法;粗灰分含量的测定采用550 ℃马福炉灼烧法。
血清生化指标测定:血清总蛋白(total protein,TP)、甘油三酯(triglyceride,TG)、总胆固醇(total cholesterol,TC)含量由湛江市农垦医院使用日立7600-110型全自动生化分析仪进行测测。血清天冬氨酸转氨酶(aspartate aminotransferase,AST)、丙氨酸转氨酶(alanine aminotransferase,ALT)、超氧化物歧化酶(superoxide dismutase,SOD)、碱性磷酸酶(alkaline phosphatase,AKP)活性均采用南京建成生物工程研究所生产的相关试剂盒测定,相应操作均参照试剂盒所附说明书进行。血清酚氧化酶(phenol oxidase,PO)活性综合文献[9, 10]的方法进行测定。
1.5 计算公式
SR(%)=100×终末尾数/初始尾数;
WGR(%)=100×(终末均重-初始均重)/初始均重;
FCR=投饲总量/(终末体重-初始体重);
SGR(%/d)=100×(ln终末体重-ln初始体重)/饲养天数;
PER(%)=100×(终末体重-初始体重)/蛋白质摄入量;
CF(g/cm3)=100×体重/体长3;
HSI(%)=100×肝胰腺/体重。
数据均以平均值±标准差(mean±SD)表示。用SPSS 17.0软件对所有数据进行单因素方差分析(one-way ANOVA),当组间有显著差异(P<0.05)时,采用Duncan氏法进行多重比较。
2 结果与分析 2.1 饲料蛋白质水平对不同生长阶段凡纳滨对虾生长性能的影响由表2可知,饲料蛋白质水平对幼虾阶段和养成阶段凡纳滨对虾的SR均无显著影响(P>0.05),其中,幼虾阶段对虾的SR均大于90%,养成阶段对虾的SR均大于96.67%。随着饲料蛋白质水平的升高,2个生长阶段对虾的WGR、SGR均先显著上升(P<0.05)而后趋于稳定(P>0.05)。以SGR为评价指标,通过折线模型拟合回归方程得出,凡纳滨对虾幼虾阶段和养成阶段的蛋白质需要量分别为38.6%(图1)和36.8%(图2)。与WGR和SGR的趋势相反,2个生长阶段对虾的FCR随饲料蛋白质水平的升高均先显著下降(P<0.05)而后趋于稳定(P>0.05)。幼虾阶段对虾在饲料蛋白质水平为29.31%~37.11%时,PER下降不显著(P>0.05),但当饲料蛋白质水平为37.11%~49.03%时,PER随饲料蛋白质水平的升高显著下降(P<0.05);养成阶段对虾的PER随饲料蛋白质水平的升高持续下降,29.31%和33.19%组显著高于41.15%、45.58%和49.03%组(P<0.05)。2个生长阶段对虾的HSI均不受饲料蛋白质水平的显著影响(P>0.05)。幼虾阶段对虾的CF在29.31%组最低,显著低于除33.19%组外的其他各组(P<0.05),其余各组间无显著差异(P>0.05);养成阶段对虾的CF随饲料蛋白质水平的升高无显著变化(P>0.05)。
| 表2 饲料蛋白质水平对不同生长阶段凡纳滨对虾生长性能的影响 Table 2 Effects of dietary protein level on growth performance of Pacific white shrimp (Litopenaeus vannamei) during different growth stages |
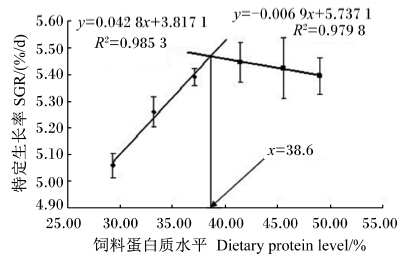 | 图1 凡纳滨对虾幼虾阶段的蛋白质需要量 Fig. 1 Protein requirement of Pacific white shrimp (Litopenaeus vannamei) during juvenile shrimp stage |
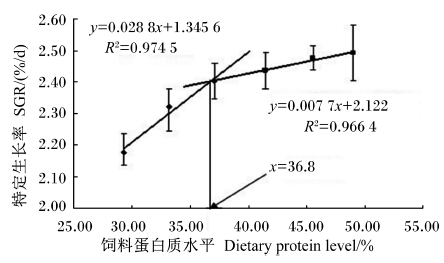 | 图2 凡纳滨对虾养成阶段的蛋白质需要量 Fig. 2 Protein requirement of Pacific white shrimp (Litopenaeus vannamei) during grow out stage |
由表3可知,幼虾阶段和养成阶段对虾的全虾干物质含量均不受饲料蛋白质水平的显著影响(P>0.05)。随着饲料蛋白质水平的升高,幼虾阶段对虾的全虾粗蛋白质含量呈现上升趋势,但组间无显著差异(P>0.05);养成阶段对虾的全虾粗蛋白质含量除29.31%组显著低于其余各组(P<0.05)外,其余各组间无显著差异(P>0.05)。幼虾阶段对虾的全虾粗脂肪含量随饲料蛋白质水平的升高先上升后下降,在37.11%组达到最高值,并与45.58%和49.03%组有显著差异(P<0.05);养成阶段对虾的全虾粗脂肪含量在各组间无显著差异(P>0.05)。幼虾阶段对虾的全虾粗灰分含量随饲料蛋白质水平的升高呈波动变化,29.31%和41.45%组显著高于33.19%和37.11%组(P<0.05);养成阶段对虾的全虾粗灰分含量各组间无显著差异(P>0.05)。
| 表3 饲料蛋白质水平对不同生长阶段凡纳滨对虾全虾常规营养成分的影响(干物质基础) Table 3 Effects of dietary protein level on common nutritional components of whole body of Pacific white shrimp (Litopenaeus vannamei) during different growth stages (DM basis) |
由表4可知,随着饲料蛋白质水平的升高,幼虾阶段对虾的肌肉干物质含量无显著变化(P>0.05)。养成阶段对虾的肌肉干物质含量随饲料蛋白质水平的升高呈上升趋势,其中45.58%和49.03%组显著高于29.31%和41.45%组(P<0.05)。随着饲料蛋白质水平的升高,幼虾阶段对虾的肌肉粗蛋白质含量在41.45%组达到最高值,并与29.31%和49.03%组有显著差异(P<0.05);养成阶段对虾的肌肉粗蛋白质含量随饲料蛋白质水平的升高呈上升趋势,其中45.58%和49.03%组显著高于29.31%、33.19%和37.11%组(P<0.05)。幼虾阶段对虾的肌肉粗脂肪含量随饲料蛋白质水平的升高呈下降趋势,且29.31%组与除37.11%组外的其他各组均有显著差异(P<0.05);养成阶段对虾的肌肉粗脂肪含量各组间无显著差异(P>0.05)。幼虾阶段对虾的肌肉粗灰分含量随饲料蛋白质水平的升高呈波动变化,33.19%组显著高于37.11%、41.45%和49.03%组(P<0.05);养成阶段对虾的肌肉粗灰分含量各组间无显著差异(P>0.05)。
| 表4 饲料中蛋白质水平对不同生长阶段凡纳滨对虾肌肉常规成分的影响(干物质基础) Table 4 Effects of dietary protein level on common nutritional components of muscle of Pacific white shrimp (Litopenaeus vannamei) during different growth stages (DM basis) |
饲料蛋白质水平对不同生长阶段凡纳滨对虾血清生化指标的影响见表5。
幼虾阶段对虾:血清TP含量各组间无显著差异(P>0.05);在饲料蛋白质水平为29.31%~33.19%时,血清TC含量随着饲料蛋白质水平的升高显著上升(P<0.05),随后则显著下降(P<0.05);血清TG含量随饲料蛋白质水平的升高整体呈上升趋势,41.45%和49.03%组显著高于29.31%和33.19%组(P<0.05);血清SOD活性随饲料蛋白质水平的升高先上升后下降,37.11%和41.45%组显著高于其他各组(P<0.05);血清PO活性随饲料蛋白质水平的升高呈先下降后上升趋势,在41.45%和45.58%组出现较低值,显著低于其他各组(P<0.05);血清ALT活性随饲料蛋白质水平的升高呈先下降后上升趋势,在37.11%组出 现最低值,并显著低于其他各组(P<0.05);血清 AST活性各组间无显著差异(P>0.05)。
养成阶段对虾:随着饲料蛋白质水平的升高,血清AKP活性先升高后降低,45.58%组显著高于29.31%和33.19%组(P<0.05);血清SOD活性随饲料蛋白质水平的升高先上升后降低,在45.58%组达到最高值,并显著高于其他各组(P<0.05);血清PO活性随饲料蛋白质水平的升高先降低后上升,在37.11%组达到最低值,并显著低于29.31%、33.19%和49.03%组(P<0.05);血清ALT活性各组间没有显著差异(P>0.05);血清AST活性随饲料蛋白质水平的升高呈先上升后降低的趋势,在37.11%组达到最高值,并显著高于29.31%、33.19%和45.58%组(P<0.05)。
| 表5 饲料蛋白质水平对不同生长阶段凡纳滨对虾血清生化指标的影响 Table 5 Effects of dietary protein level on serum biochemical indices of Pacific white shrimp (Litopenaeus vannamei) during different growth stages |
本试验结果显示,当饲料蛋白质水平在37.11%~49.03%之间时,幼虾阶段和养成阶段凡纳滨对虾的WGR和SGR均没有显著变化,但当饲料蛋白质水平低于37.11%时,其WGR和SGR显著低于蛋白质水平在37.11%~49.03%时,且FCR显著升高。通过建立SGR与饲料蛋白质水平的折线模型并拟合回归方程,可以得出凡纳滨对虾幼虾阶段和养成阶段的蛋白质需要量分别为38.6%和36.8%。本试验结果与Smith等[5]的研究结果比较吻合,而低于李广丽等[6]的研究结果。李广丽等[6]的试验是在盐度较低的情况下进行的,而且试验配方同本试验也有较大的差异。此外,养殖对虾的规格、养殖环境(包括水温、盐度、放养密度等)及饲料蛋白质品质(主要是氨基酸组成)等均会影响到蛋白质的需要量。
和其他动物一样,凡纳滨对虾也依靠蛋白质在体内构成组织和器官,维持生长。从外界饲料中摄取的蛋白质,在消化道中经消化分解成氨基酸被吸收,供体组织和器官蛋白质的更新、修复及维持蛋白质现状;构成各种酶类和激素等具有特殊生物学功能的物质;供体蛋白质的增加,即用于生长;作为部分能量的来源[9]。从本试验结果看,饲料蛋白质水平过高反而降低对虾的生长性能,这一结果表明饲料蛋白质水平并非越高越好。相反,随着饲料蛋白质水平的升高,对虾的PER持续降低。这一结果说明,饲料蛋白质水平较低时,蛋白质的利用效率较高,对虾能够充分利用饲料中的蛋白质,且主要用于维持体内蛋白质的更新、修复及正常的生理代谢;当饲料蛋白质水平较高时,过高的蛋白质被分解作为能量来源,其对蛋白质的利用效率下降,造成饲料蛋白质浪费。因此,适宜的饲料蛋白质水平不仅能降低饲料成本,还能提高对虾的PER,减轻饲料、粪便对水体的污染。
随着凡纳滨对虾的生长,其对饲料蛋白质的需要量降低,这与已有的对鱼类[9]以及甲壳类的研究结果[10, 11]一致。对比幼虾阶段和养成阶段凡纳滨对虾的生长结果,幼虾阶段对虾的WGR、SGR及PER均比养成阶段高,说明幼虾阶段对虾的生长速度比养成阶段快,对饲料的利用效率也比养成阶段高。有研究表明,只有满足养殖动物最低的氨基酸需要量,才能保证养殖动物正常的生长性能[9]。本试验中低蛋白质饲料组(29.31%组)对虾的生长性能较低可能与其饲料中必需氨基酸含量较低有直接的关系,随着饲料蛋白质水平的升高,饲料中必需氨基酸如赖氨酸和蛋氨酸含量相应增加,生长性能随之增加。
3.2 饲料蛋白质水平对不同生长阶段凡纳滨对虾全虾和肌肉常规营养成分的影响本试验结果表明,饲料蛋白质水平显著影响幼虾阶段及养成阶段凡纳滨对虾全虾及肌肉的部分常规营养成分。徐新章等[12]指出,饲料蛋白质水平与对虾蛋白质增重呈显著的正相关关系;李二超等[13]研究了不同盐度下饲料蛋白质水平对凡纳滨对虾体成分的影响,结果表明对虾虾体粗蛋白质含量随饲料蛋白质水平的升高而显著上升。然而,楼伟风等[14]对人工养殖与天然中国对虾体成分的比较结果表明,上述2种虾体的粗蛋白质、氨基酸含量基本一致;潘英等[15]对不同环境下凡纳滨对虾体成分分析结果表明,不同环境下虾体组分没有显著变化;李广丽等[6]的研究结果也表明饲料蛋白质水平不影响凡纳滨对虾虾体粗蛋白质含量。造成各试验结果不一致的原因可能与试验用对虾的规格(生长阶段)、养殖环境以及饲料蛋白质源等不同有关。本试验中饲料蛋白质水平对不同生长阶段的凡纳滨对虾全虾及肌肉的常规营养成分的影响不同,说明饲料蛋白质水平对凡纳滨对虾全虾及肌肉的常规营养成分的影响还与对虾的生长阶段有关,虾体粗蛋白质含量的变化主要通过对虾生长而表现出来。至于饲料蛋白质水平与虾体蛋白质沉积的关系,还有待进一步深入研究。
3.3 饲料蛋白质水平对不同生长阶段凡纳滨对虾血清生化指标的影响动物正常生理状态下,血液主要生化指标相对恒定,血清成分变化能在一定程度上反映动物的健康状态,同时血清成分也随着其生理状态的变化而相应变化[16]。本试验结果表明,凡纳滨对虾血清TC含量随着饲料蛋白质水平的升高呈先上升后下降趋势,而血清TG含量则随饲料蛋白质水平的升高整体呈上升趋势。饲料蛋白质水平对凡纳滨对虾血清TP含量无显著影响。Engle等[17]认为甲壳类动物血清TP含量受季节、溶氧等环境因子的影响较大。刘树青等[18]认为对虾血清TP含量的提高可以相应提高对虾血清中溶菌物质、杀菌物质的含量,从而提高对虾的抗病力。
幼虾阶段的试验结果表明,随着饲料蛋白质水平的升高,凡纳滨对虾血清SOD活性先上升后下降,且37.11%和41.45%组显著高于其他各组;血清PO活性随饲料蛋白质水平的升高则出现逐步降低的趋势,且41.45%和45.58%组显著低于其余各组。养成阶段的试验结果表明,随着饲料蛋白质水平的升高,凡纳滨对虾血清AKP、SOD活性变化相似,随着饲料蛋白质水平从29.31%升高到37.11%,血清AKP、SOD活性显著升高,而随着饲料蛋白质水平的进一步升高,血清AKP和SOD活性并未显著升高。SOD是广泛存在于生物体内的含Cu、Zn、Mn、Fe的金属类酶。它作为生物体内重要的自由基清除剂,可以清除体内多余的超氧阴离子,在防御生物体氧化损伤方面起着重要作用[19, 20, 21, 22, 23]。AKP是机体生长代谢、维持机体内环境稳定的一种酶,其活性受营养因素的影响。Velasco等[24]给凡纳滨对虾投喂蛋白质水平分别为5%、15%和40%的饲料50 d,发现幼虾PO活性、呼吸爆发强度等指标均受饲料蛋白质水平的影响,40%组幼虾的生长速度比5%和15%组快,血细胞表达量也比5%和15%组高,并指出低蛋白质饲料直接影响对虾免疫系统的正常运转,降低免疫相关酶及因子活性。本试验结果表明,随饲料蛋白质水平的升高,凡纳滨对虾养成阶段的血清SOD和PO活性与幼虾阶段的变化趋势相似,说明饲料蛋白质水平影响凡纳滨对虾的血清酶活性,从而影响凡纳滨对虾的健康。在适宜的饲料蛋白质水平下,对虾保持良好的健康状态,其血清AKP、SOD活性有所上升。
本试验中,血清PO活性随着饲料蛋白质水平的升高而呈现降低的趋势,饲料蛋白质水平为37.11%时血清PO活性最低。一般认为,PO是甲壳类动物主要的非特异性免疫酶,是衡量甲壳类机体免疫功能的重要指标。除了参与机体的免疫机制以外,PO还参与甲壳动物蜕皮过程中的硬化及伤口新表皮的硬化[25]。本试验中,在适宜的蛋白质水平下,血清PO活性最低,说明此时对虾处于良好的生理状态,而过低或过高的蛋白质水平都会影响到对虾的非特异性免疫反应。
AST和ALT是机体代谢必不可少的转氨酶[26, 27, 28, 29]。在幼虾阶段,饲料蛋白质水平对凡纳滨对虾血清AST活性未产生显著影响,但37.11%组血清ALT活性则显著低于其余各组。在养成阶段,饲料蛋白质水平对凡纳滨对虾血清ALT活性无显著影响,但随着饲料蛋白质水平的升高,对虾血清AST活性先升高后下降,在37.11%组达到最高值,并显著高于29.31%、33.19%和45.58%组。AST和ALT主要存在于肝细胞中,是反映肝脏损伤程度的重要指标。林仕梅等[30]认为血清转氨酶(AST和ALT)活性与机体健康状态有关,当组织细胞坏死时,细胞膜渗透能力增大,细胞内的转氨酶大量释放出来进入到血液中,从而使转氨酶的活性升高。在本试验中,饲料蛋白质水平对2个生长阶段凡纳滨对虾血清转氨酶活性的影响不一致,可能是因为环境因子对转氨酶活性的影响比营养物质的影响要大。
4 结 论以SGR为评价指标,经折线模型拟合回归方程后得出,凡纳滨对虾幼虾阶段和养成阶段的蛋白质需要量分别为38.6%和36.8%。
| [1] | 张伟权.世界重要养殖品种--南美白对虾生物学简介[J]. 海洋科学,1990,3(3):69-73. ( 1) 1)
|
| [2] | 农业部渔业局.中国渔业统计年鉴2013[M].北京:中国农业出版社,2013. ( 1) 1)
|
| [3] | 艾春香.蟹类营养与饲料[C]//福建省水产动物营养暨养殖技术研讨会论文集.厦门:[出版者不详],2004.( 1) 1)
|
| [4] | 陈文汉,宁凌.中国对虾产业现状及相关研究综述[J]. 渔业经济研究,2008(2):21-27. ( 1) 1)
|
| [5] | SMITH L L,LEE P G,LAWRENCE A L,et al.Growth and digestibility by three sizes of Penaeus vannamei Boone:effects of dietary protein level and protein source[J]. Aquaculture,1985,46(2):85-96. ( 3) 3)
|
| [6] | 李广丽,朱春华,周歧存.不同蛋白质水平的饲料对南美白对虾生长的影响[J]. 海洋科学,2001,25(4):1-4. ( 3) 3)
|
| [7] | 刘立鹤,郑石轩,徐焕新.不同鱼粉含量的饵料对南美白对虾生长的影响[J]. 广东饲料,2002,11(5):21-22. ( 1) 1)
|
| [8] | 黄凯,王武,卢洁.南美白对虾幼虾饲料蛋白质的需要量[J]. 中国水产科学,2003,10(4):308-32l. ( 1) 1)
|
| [9] | 李爱杰.水产动物营养与饲料学[M]. 北京:中国农业出版社,1996:36-38. ( 4) 4)
|
| [10] | 秦钦,蔡永祥,陈校辉,等.不同规格日本沼虾饲料蛋白最适含量研究[J]. 饲料研究,2010(4):4-7. ( 2) 2)
|
| [11] | 陈义方,林黑着,牛津,等.不同规格南美白对虾蛋白质需要量的研究[J]. 广东农业科学,2011(13):7-10. ( 1) 1)
|
| [12] | 徐新章,李爱杰.中国对虾配饵中蛋白质、糖、纤维素、脂肪的适宜含量及日需量研究[J]. 海洋科学,1988(6):1-6. ( 1) 1)
|
| [13] | 李二超,陈立侨,曾嶒,等.不同盐度下饵料蛋白质含量对凡纳滨对虾生长、体成份和肝胰腺组织结构的影响[J]. 水产学报,2008,32(3):425-432. ( 1) 1)
|
| [14] | 楼伟风,李爱杰,徐家敏.中国对虾(Penaeus orientalis Kishiouys)粗蛋白、氨基酸含量的比较分析[J]. 青岛海洋大学学报,1989,19(2):70-79. ( 1) 1)
|
| [15] | 潘英,王如才,罗永巨,等.海水和淡水养殖南美白对虾肌肉营养成分的分析比较[J]. 青岛海洋大学学报,2001,31(6):828-834. ( 1) 1)
|
| [16] | DJANGMAH J S.The effects of feeding and starvation on copper in the blood and hepatopancreas,and on blood proteins of Crango villgaris (Fabricius)[J]. Comparative Biochemistry and Physiology,1970,32:709-731. ( 1) 1)
|
| [17] | ENGLE D W,BROUNER M,MCKENNA S.Hemocyani concentrations in marine crustaceans as a function of environmental conditions[J].Marine Ecology Progress Series,1993,93:235-244. ( 1) 1)
|
| [18] | 刘树青,江晓路,牟海津,等.免疫多糖对中国对虾血清溶菌酶、磷酸酶和过氧化物酶的作用[J]. 海洋与湖沼,1999,30(3):278-283. ( 1) 1)
|
| [19] | 孙虎山,李光友.栉孔扇贝血淋巴中超氧化物歧化酶和过氧化氢酶活性及其性质的研究[J]. 海洋与湖沼,2000,31(3):259-265. ( 1) 1)
|
| [20] | HALLIWELL B.Free radical in biochemistry and medicine[M]//MEYERS R A.Molecular biology and biotechnology:a comprehensive desk reference. :Wiley-VCH,1995:327-331.( 1) 1)
|
| [21] | KOHEN R,NYSKA A.Oxidation of biological systems:oxidative stress phenomena,antioxidants,redox reactions,and methods for their quantification[J]. Toxicologic Pathology,2002,30:620-650. ( 1) 1)
|
| [22] | MCCORD J M,FRIDOVICH I.Superoxide dismutase:an enzymic function for erythrocuprein (hemocuprein)[J]. The Journal of Biological Chemistry,1969,244(22):6049-6055. ( 1) 1)
|
| [23] | SHEN W Y,FU L L,LI W F,et al.Effect of dietary supplementation with Bacillus subtilis on the growth,performance,immune response and antioxidant activities of the shrimp(Litopenaeus vannamei)[J]. Aquaculture Research,2010,41:1691-1698. ( 1) 1)
|
| [24] | VELASCO M,LAWRENCE A L,CASTILLE F L,et al.Dietary protein requirement for Litopenaeus vannamei[EB/OL].[2014-04-08].http://www.doc88.com/p-902538271602.html. ( 1) 1)
|
| [25] | 孟凡伦,张玉臻,孔健,等.甲壳动物中的酚氧化酶原激活系统研究评价[J]. 海洋与湖沼,1999,30(1):110-115. ( 1) 1)
|
| [26] | YAN Q,XIE S,ZHU X,et al.Dietary methionine requirement for juvenile rockfish,Sebastes schlegel[J]. Aquaculture Nutrition,2007,13:163-169. ( 1) 1)
|
| [27] | 马志英,朱晓鸣,解绶启,等.异育银鲫幼鱼对饲料苯丙氨酸需求的研究[J]. 水生生物学报,2010,34(5):1012-1021. ( 1) 1)
|
| [28] | YAMAMOTO.Determination of toxicity by biochemical method[M]//EGAMI N.Fishes as laboratory.Tokyo:Soft Science,1981:568-574.( 1) 1)
|
| [29] | CHAPLIN A E,HUGGINS A K,MUNDAY K A.The distribution of L-α-aminotransferases in Carcinus maenas[J]. Comparative Biochemistry and Physiology,1967,20:195-198. ( 1) 1)
|
| [30] | 林仕梅,罗莉,叶元土,等.喹乙醇对草鱼耗氧率及组织转氨酶活力的影响[J]. 中国饲料,1997(22):31-34. ( 1) 1)
|




