2. 中国水产科学研究院黄海水产研究所, 青岛 266071;
3. 山东科合海洋高技术有限公司, 威海 264513
2. Yellow Sea Fisheries Institute, Chinese Academy of Fishery Sciences, Qingdao 266071, China;
3. Shandong Kehe Marine High-Technology Co., Ltd., Weihai 264513, China
刺参(Apostichopus japonicus Selenka),又称仿刺参,隶属于棘皮动物门(Echinodermata),刺参科(Stichopodidae),仿刺参属(Apostichopus)。目前,我国刺参养殖年产值高达300亿元以上[1],成为一个重要的海珍品养殖产业。然而,刺参配合饲料的研究与生产滞后于产业发展需求,成为制约刺参养殖业健康可持续发展的一个重要因素,急需加大力度开展对刺参高效配合饲料的研究。
纤维素酶是一种复合酶,是在各种酶组分的协同作用下,能降解纤维素,使之变成纤维寡糖、纤维二糖和葡萄糖的酶的总称[2],主要包括外切β-葡聚糖酶、内切β-葡聚糖酶和β-葡萄糖苷酶等,还含有高活性的木聚糖酶[3],已广泛地应用于动物饲料中。研究表明,纤维素酶能够提高草鱼[4, 5]、奥尼罗非鱼[6]和日本沼虾[7]等的生长速度、消化酶活性,降低饲料系数,提高异育银鲫[8]和日本沼虾[7]等的非特异性免疫力。目前,纤维素酶在刺参饲料中的应用研究较少,仅见徐彬[9]研究纤维素酶体外酶解饲料后投喂对刺参生长的影响,然而体外酶解饲料存在增加操作工序和效率问题。
刺参属于低营养等级的底栖沉积物食性,饲料主成分海藻粉中含有较多的粗纤维,而其自身肠道中纤维素酶含量较低[10],造成刺参对饲料利用率不高。本试验拟通过在幼刺参饲料中添加纤维素酶,研究其对幼刺参生长性能、消化能力和非特异性免疫力的影响,分析并确定纤维素酶在幼刺参饲料中的适宜添加量,旨在为提高刺参饲料利用率提供参考依据。
1 材料与方法 1.1 试验材料刺参由山东省科合海洋高技术有限公司提供。纤维素酶为饲料级粉状酶制剂,购自苏柯汉(潍坊)生物工程有限公司,活性为20 000 U/g。
1.2 基础饲料试验以马尾藻、海带粉、脱胶海带粉、酵母、鱼粉、豆粕、维生素预混料和矿物质预混料等为原料,配制粗蛋白质含量为20.25%、粗脂肪含量为0.95%的粉状基础饲料,其组成及营养水平见表1。
| 表1 基础饲料组成及营养水平(干物质基础) Table 1 Composition and nutrient levels of the basal diet (DM basis) |
1.3 试验设计
试验采用单因素试验设计,在基础饲料的基础上,以0、0.025%、0.050%、0.100%、0.200%和0.400%的纤维素酶替代等量的基础饲料,制成6种试验饲料,分别用D1(对照)、D2、D3、D4、D5和D6组表示。所有饲料原料粉碎粒度均小于150 μm(过100目筛),然后按配方逐级添加,小型搅拌机混合均匀,制成粉状饲料,最后将纤维素酶溶于水(饲料与水比为99 ∶ 1)均匀喷洒到饲料表面。另单独配制加入0.50%的三氧化二铬(Cr2O3)作为指示剂的试验饲料用于消化试验,配制方法同上。试验饲料自然晾干后,-20 ℃保存备用。
1.4 饲养管理养殖试验于2013年10月14日至2013年12月2日(共计49 d)在山东科合海洋高技术有限公司刺参养殖车间内进行。正式试验前暂养5 d,暂养期间投喂基础饲料。暂养结束后,选取630头体质健壮、大小均称,平均体重为(1.44±0.01) g的幼刺参,随机分成6组,每组3个重复,每个重复35头,饲养于规格为150 L的塑料水槽中,水槽中放置养殖刺参用塑料筐1个,每个筐上插入10个波纹板。试验期间水温变化情况见图1,盐度控制在30.5~31.5,连续充气,溶氧浓度保持在5 mg/L以上,pH为7.5~8.0。
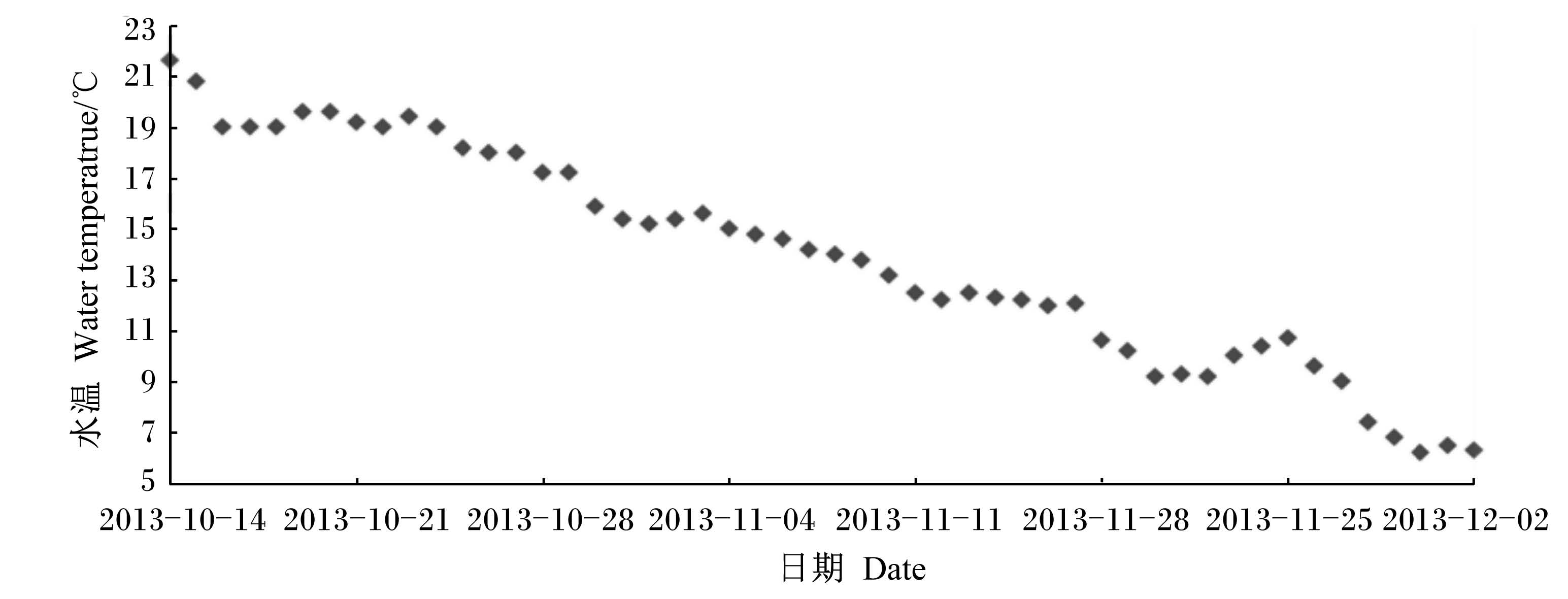 | 图1 试验期间水温变化情况
Fig. 1 Water temperature variation during experiment |
每天投喂1次,10:00左右将各组试验饲料和6倍量的湿海泥(含水量67%,过80目筛,试验基地多年生产使用该湿海泥的料泥最适比例是1 ∶ 6)分别置于不同的白色塑料杯中,加入适量海水,搅拌均匀后静置浸泡3~4 h。14:00左右吸底换水1次,换水量为1/2~2/3,换水后将已浸泡完的试验饲料和湿海泥混合均匀后进行投喂。饲料初始投喂量为刺参体重的3%,然后根据每天观察到的刺参的摄食和排便情况及时调整投喂量,并记录每天的水温、投喂量和死亡情况。
消化试验单独养殖,除投喂时不添加湿海泥直接投喂已浸泡饲料和收集粪样外,试验用刺参、分组、饲养管理及养殖条件等与养殖试验一致。
1.5 样品采集与处理 1.5.1 样品采集试验前后分别对各组刺参进行计数、称重,称重方法参照李旭等[11]的方法。
试验结束时,各组随机选取5头刺参,其中2头刺参取前肠、中肠、后肠,其他3头刺参取全肠道,并保存于液氮中带回实验室,转移至-80 ℃超低温冰箱中保存,用于消化酶和免疫酶活性的测定。
消化试验粪样收集:采用虹吸法收集包膜完整粪样。每9 d每组换1批(35头)刺参,先用各组试验饲料暂养5 d,暂养结束后收集粪便,连续收集4 d作为1个重复,共收集3个重复。将收集的粪样55 ℃烘干,-20 ℃保存以备测定。
1.5.2 样品处理刺参肠道粗酶液的制备:从-80 ℃冰箱中取出前肠、中肠、后肠和全肠道,冰浴中解冻,准确称其湿重,按重量体积比1 ∶ 9加入9倍体积的生理盐水后,在冰浴中机械匀浆。将匀浆液于4 ℃下离心20 min(2 500 r/min),取其上清液即为粗酶液,并于4 ℃冰箱中保存备用(24 h内分析完毕)。粗酶液蛋白质浓度采用南京建成生物工程研究所生产的蛋白质定量测定试剂盒(考马斯亮蓝法)测定。
1.6 测定指标生长指标计算公式如下:
特定生长率(specific growth rate,SGR,%/d)=100×[ln末体重(g)-ln初体重(g)]/饲养天数(d); 饲料系数(feed conversion ratio,FCR)=摄食量(g)/[末体重(g)-初体重(g)]; 摄食率(feed intake,FI,%)=100×摄食量(g)/{饲养天数(d)×[末体重(g)+初体重(g)]/2}; 成活率(survival rate,SR,%)=100×终末刺参头数/初始刺参头数。饲料和粪样中Cr2O3含量采用GB/T 13088—2006《饲料中铬的测定》中方法测定,饲料中营养物质表观消化率计算公式如下:
干物质表观消化率(apparent digestibility coefficient of dry matter,ADCd,%)=100×[1-饲料中Cr2O3含量(%)/粪便中Cr2O3含量(%)]; 粗蛋白质表观消化率(apparent digestibility coefficient of crude protein,ADCp,%)=100×{1-[饲料中Cr2O3含量(%)×粪样中粗蛋白质含量(%)]/[粪便中Cr2O3含量(%)×饲料中粗蛋白质含量(%)]}。刺参的前肠、中肠和后肠淀粉酶(amylase,AMS)活性与全肠道中超氧化物歧化酶(superoxide dismutase,SOD)和酸性磷酸酶(acid phosphatase,ACP)活性均用南京建成生物工程研究所生产的相关试剂盒测定,其操作步骤见试剂盒说明书。
1.7 数据统计与分析试验数据用平均值±标准差表示,用Excel 2010处理数据,SPSS 17.0统计软件进行单因素方差分析(one-way ANOVA)。若差异显著,进行Duncan氏法多重比较检验,显著性水平为P<0.05。
2 结果与分析 2.1 饲料中添加纤维素酶对幼刺参生长性能的影响由表2可知,各组刺参SGR的顺序是D4组> D3组>D2组>D5组>D6组>D1组,其中D4、D3和D2组与D1组差异显著(P<0.05),分别较D1组提高了30.97%、18.06%和14.84%,且D4、D3和D2组之间有显著差异(P<0.05),D5和D6组与D1组差异不显著(P>0.05)。D4组的FCR最低,为1.87,随后依次是D3、D2、D5和D1组,D6组最高,为2.46,其中D4组与D1、D5、D6组差异显著(P<0.05),分别较D1、D5、D6组降低了30.48%、25.67%和31.55%,与D2、D3组差异不显著(P>0.05),D2、D3、D5和D6组与D1组之间无显著差异(P>0.05)。饲料中不同添加量的纤维素酶对刺参FI和SR无显著影响(P>0.05)。
| 表2 饲料中添加纤维素酶对幼刺参生长性能的影响 Table 2 Effects of dietary cellulase on growth performance of juvenile sea cucumber (Apostichopus japonicus Selenka) |
由表3可知,各组饲料ADCd和ADCp随着纤维素酶添加量的增加先上升再下降。各组饲料ADCd为43.00%~49.52%,其中D4组最高,为49.52%,显著高于其他各组(P<0.05),比D1组提高了15.16%;D3和D5组显著高于D1组(P<0.05),分别较D1组提高了6.74%和8.28%;D2和D6组与D1组差异不显著(P>0.05)。各组饲料ADCp为47.37%~60.18%,其中D4组最高,为60.18%,显著高于其他各组(P<0.05),比D1组提高了19.29%;D6组最低,显著低于其他各组(P<0.05),与D1组相比降低了6.11%;D3和D5组显著高于D1组(P<0.05),分别较D1组提高了10.86%和10.47%,D2组与D1组差异不显著(P>0.05)。
| 表3 饲料中添加纤维素酶对饲料ADCd和ADCp的影响 Table 3 Effects of dietary cellulase on ADCd and ADCp in diets |
2.3 饲料中添加纤维素酶对幼刺参前肠、中肠和后肠中AMS活性的影响
由表4可知,前肠、中肠和后肠中AMS活性最高的组分别是D4、D5和D6组。在前肠中,D4组显著高于D1组(P<0.05),其他组与D1相比均无显著差异(P>0.05)。在中肠中,除D6组,其他 组均显著高于D1组(P<0.05),且D5组显著高于D2、D3和D6组(P<0.05),但与D4组差异不显著(P>0.05)。在后肠中,D6组显著高于其他各组(P<0.05),D2、D3、D4和D5组与D1组相比均无显著差异(P>0.05)。
| 表4 饲料中纤维素酶对幼刺参前肠、中肠和后肠中AMS活性的影响 Table 4 Effects of dietary cellulase on AMS activity in foregut,midgut and hindgut of juvenile sea cucumber (Apostichopus japonicus Selenka) |
由表5可知,肠道中SOD活性随着纤维素酶添加量的增加先上升后下降,D4组最高,其次是D5组,二者均显著高于D1组(P<0.05),D2、D3和D6组与D1组相比无显著差异(P>0.05)。肠道中ACP活性随着纤维素酶添加量的增加先上升后下降,D4组最高。D4、D5和D6组均显著高于D1组(P<0.05),D2和D3组与D1组无显著差异(P>0.05)。
| 表5 饲料中添加纤维素酶对幼刺参肠道中SOD和ACP活性的影响 Table 5 Effects of dietary cellulase on SOD and ACP activities in gut of juvenile sea cucumber (Apostichopus japonicus Selenka) |
纤维素是构成植物细胞壁的主要物质,细胞壁保护植物细胞中的营养物质不流失,然而,当植物进入动物消化道,细胞壁将阻碍动物对蛋白质和脂肪等营养物质的吸收利用。纤维素酶对水解纤维素有重要的意义,在一定条件下能够将大分子的纤维素水解成较小分子的纤维二糖和葡萄糖等糖类。当添加有纤维素酶的饲料进入动物消化道后,在消化道中纤维素酶酶解饲料,破坏饲料中植物的细胞壁,使之释放出更多的营养物质,促进动物生长[12]。本试验结果表明,在饲料中添加0.025%~0.100%的纤维素酶能够提高刺参的SGR和降低FCR,这与高春生等[4]在草鱼上所得结果相一致。但当纤维素酶添加量为0.200%和0.400%时,刺参的SGR和FCR与对照组差异不显著,其原因可能是过多的外源性酶对内源性酶的分泌有抑制作用,出现酶活性饱和现象[13],从而影响刺参的SGR和FCR。本试验结果表明,饲料中添加纤维素酶对刺参的FI无显著影响,这与Flores等[14]报道的饲料中添加酶制剂不能提高动物采食量,但能提高SGR和降低FCR的结果相一致。
3.2 饲料中添加纤维素酶对饲料ADCd和ADCp的影响高春生等[15]研究表明,在饲料中添加0.10%的纤维素酶能够提高鲤鱼对饲料中干物质和粗蛋白质的表观消化率,与对照组比较分别提高了6.80%和10.65%。施培松[16]报道,在分泌纤维素酶较少的鱼类饲料中添加纤维素酶,可有效地提高饲料中营养物质的消化吸收率。这与本试验在刺参饲料中添加0.050%~0.200%的纤维素酶能够有效地提高饲料ADCd和ADCp的结果相一致,其原因可能是:1)纤维素酶破坏植物细胞壁,使植物细胞内容物被释放出来,在纤维素酶和其他酶的协同作用下将不易消化的大分子多糖、蛋白质和脂类降解成小分子物质,有利于动物胃肠道的消化吸收;2)纤维素酶刺激动物体内内源酶的分泌,提高部分内源酶活性,增强动物的消化吸收功能;3)半纤维素等非淀粉多糖部分溶于水后会增加消化物的黏度,对内源酶作用于营养物质造成障碍,而添加的纤维素酶能分解半纤维素等非淀粉多糖,降低动物肠道消化物黏度,增加内源酶的扩散,提高酶与营养物质接触面积,促进饲料的良好消化[4]。本试验结果表明,刺参饲料中添加0.400%的纤维素酶对饲料ADCd无显著影响,对ADCp有抑制作用,分析其原因可能是过多的纤维素酶对刺参体内内源酶的分泌有抑制作用[13]。
3.3 饲料中添加纤维素酶对幼刺参前肠、中肠和后肠中AMS活性的影响肠道是刺参消化吸收的主要器官,在体腔内先是右侧下行,接着左侧上行,最后中下方下行,弯曲2次,分为3段,依次称为前肠、中肠和后肠,分别占整个肠道1/4、1/4和1/2。AMS是刺参肠道中最主要的一种内源性消化酶,存在于刺参整个肠道中,对刺参消化吸收淀粉等营养物质有重要的意义,其活性能够体现刺参对饲料中淀粉等营养物质的消化能力。有研究报道刺参肠道AMS活性受到pH、温度和底物浓度等多种因素的影响[17, 18]。本试验研究了饲料中添加纤维素酶对刺参前肠、中肠和后肠中AMS活性的影响,其结果表明饲料中添加纤维素酶能够提高刺参前肠、中肠和后肠中AMS活性,这与纤维素酶能够提高草鱼肠道中AMS活性的研究结果[5]相一致。其中,饲料中添加0.100%、0.200%和0.400%的纤维素酶分别对刺参前肠、中肠和后肠中AMS活性影响最为显著,而过多(0.400%)的纤维素酶对前肠和中肠中AMS的分泌无促进作用,分析其原因可能是随着纤维素酶添加量的增加,导致酶解产物量也相应地上升,肠道中营养物质也随之增加,而已消化但未被动物及时吸收的营养物质将累积,消化道中纤维素酶过量则会抑制AMS的分泌[19],随着营养物质在经整个肠道过程中被吸收利用,纤维素酶添加量的增加也相应能够提高后肠中AMS活性。
3.4 饲料中添加纤维素酶对幼刺参肠道中SOD和 ACP活性的影响SOD作为活性氧清除剂来清除体内自由基,能使体内超氧阴离子(O-2)转变为H2O2和O2的反应加速,是抗氧化系统中的关键性酶,也是机体免疫调节网络的重要组成部分,机体内SOD活性高低标志着有机体清除自由基能力的强弱[20]。ACP是动物体内巨噬细胞溶酶体的标志酶,也是巨噬细胞内典型的水解酶之一,在酸性条件下,ACP可通过水解作用来破坏掉表面带有磷酸酯的异物,并能修饰或改变细菌等外来异物的表面分子结构组成等,从而加快对异物的吞噬和清除速度,在刺参抵抗疾病、免疫应答及细胞损伤与修复过程中具有一定的生物学意义[21]。刺参肠道[22, 23]、体壁和体腔液[24]中均可以检测到SOD和ACP的存在。本试验结果表明,在刺参肠道中可以检测到SOD和ACP的存在,同时在饲料中添加纤维素酶能够提高刺参肠道中SOD和ACP活性,分析其原因可能是:1)营养物质利用率的提高对免疫应答有间接作用的结果,因为添加纤维素酶后提高了动物的消化吸收能力,特别是提高了机体对蛋白质等营养物质的利用率,从而促进了相关免疫因子的合成,加强了机体代谢水平,产生了更多的O-2等自由基,相应地也提高了SOD的活性[25];2)纤维素酶酶解饲料过程中产生了一些寡糖等免疫增强物质,促进了机体免疫应答反应,从而提高了ACP活性[8]。这与纤维素酶能够增强鹅[26]、鸡[27]和异育银鲫[8]等动物机体免疫能力的研究结果相一致。然而,过多(0.400%)的纤维素酶对刺参肠道SOD活性无明显的促进作用,其原因可能是0.400%的纤维素酶对ADCp有抑制作用,降低了相关免疫因子的合成,导致未能提高SOD活性。
4 结 论在本试验条件下,饲料中添加适量纤维素酶可促进幼刺参生长,提高其消化能力和非特异性免疫力。综合考虑生长、消化和非特异性免疫指标,在幼刺参饲料中纤维素酶的适宜添加量为0.100%。
| [1] | 农业部渔业局.2012中国渔业统计年鉴[M]. 北京:中国农业出版社,2012:13. ( 1) 1)
|
| [2] | 中华人民共和国国家发展和改革委员会.QB 2583-2003纤维素酶制剂[S]. 北京:中国标准出版社,2003. ( 1) 1)
|
| [3] | 中国产业研究报告网.2013-2018年中国纤维素酶行业全景调研与投资趋势评估报告[EB/OL].[2014-03-20] http://www.chinairr.org/report/R02/R0206/201309/25-141602.html. ( 1) 1)
|
| [4] | 高春生,范光丽,李建华,等.纤维素酶对草鱼生长性能和饲料消化率及体成分的影响[J]. 中国农学通报,2006,22(10):473-475. ( 3) 3)
|
| [5] | ZHOU Y,YUAN X C,LIANG X F,et al.Enhancement of growth and intestinal flora in grass carp:the effect of exogenous cellulase[J]. Aquaculture,2013,416/417:1-7. ( 2) 2)
|
| [6] | 王纪亭.非淀粉多糖酶在奥尼罗非鱼饲料中的应用及其作用机理的研究[D]. 博士学位论文.北京:中国农业大学,2005:31-57. ( 1) 1)
|
| [7] | 谢国驷.日本沼虾(Macrobrachium nipponense)饲料适宜蛋白水平及环保型添加剂的研究[D]. 硕士学位论文.南京:南京农业大学,2007:35-57. ( 2) 2)
|
| [8] | 张丽.外源酶制剂对异育银鲫生长、消化酶及非特异性免疫的影响[D]. 硕士学位论文.武汉:武汉工业学院,2008:8-27. ( 2) 2)
|
| [9] | 徐彬.刺参幼参预消化配合饲料的研究[D]. 硕士学位论文.北京:中国农业科学院,2009:52-56. ( 1) 1)
|
| [10] | 周玮,田甲申,黄俊鹏,等.不同生长阶段仿刺参肠道内含物及消化酶活性的变化[J]. 大连海洋大学学报,2010,25(5):460-464. ( 1) 1)
|
| [11] | 李旭,章世元,陈四清,等.四种饲料原料对刺参生长、体成分及消化生理的影响[J]. 饲料工业,2013,34(8):36-40. ( 1) 1)
|
| [12] | VEERESH J,WU J C.Microbial cellulases:engineering,production and applications[J]. Renewable and Sustainable Energy Reviews,2014,33:188-203. ( 1) 1)
|
| [13] | KAO C,BLAHA J H,SKARKOWA L.Estimation of the enzyme preparation required to obtain optimum nutrient utilization and growth performance in young broiler chicks fed on barley diets[J]. Zivocisna Vyroba,1996,41(1):18-19. ( 2) 2)
|
| [14] | FLORES M P,CASTANON J I R,MCNAB J M.Effect of enzyme supplementation of wheat and triticale based diet for broiler[J]. Animal Feed Science Techology,1994,49(3/4):237-243. ( 1) 1)
|
| [15] | 高春生,程会昌,霍军,等.纤维素酶在鲤鱼饲料中的应用试验[J]. 粮食与饲料工业,2006(9):32-33. ( 1) 1)
|
| [16] | 施培松.复合酶制剂对草鱼鱼种生长性能及消化酶的影响[D]. 硕士学位论文.武汉:华中农业大学,2005:13-34. ( 1) 1)
|
| [17] | 姜令绪,杨宁,李建,等.温度和pH对刺参(Apostichopus japonicus)消化酶活力的影响[J]. 海洋与湖沼,2007,38(5):476-480. ( 1) 1)
|
| [18] | 吴永恒,王秋月,冯政夫,等.饲料粗蛋白含量对刺参消化酶及消化道结构的影响[J]. 海洋科学,2010,36(1):36-41. ( 1) 1)
|
| [19] | 蒋正宇,周岩民,王恬.外源α-淀粉酶对21日龄肉鸡消化器官发育、肠道内源酶活性的影响[J]. 畜牧兽医学报,2007,38(7):672-677. ( 1) 1)
|
| [20] | 赵保路.氧自由基和天然抗氧化剂[M]. 北京:科学出版社,1999:61-63. ( 1) 1)
|
| [21] | 李继业.养殖刺参免疫学特征与病害研究[D]. 博士学位论文.青岛:中国海洋大学,2007:33-56. ( 1) 1)
|
| [22] | 张涛,白岚,李蕾,等.不同添加量的益生菌组合对仿刺参消化和免疫指标的影响[J]. 大连水产学院学报,2009,24(增刊):64-68. ( 1) 1)
|
| [23] | 李旭. 刺参幼参饲料原料选择与蛋白质营养需求的研究[D]. 硕士学位论文.扬州:扬州大学,2013:25-40. ( 1) 1)
|
| [24] | 江晓路,杜以帅,王鹏,等.褐藻寡糖对刺参体腔液和体壁免疫相关酶活性变化的影响[J]. 中国海洋大学学报,2009,39(6):1188-1192. ( 1) 1)
|
| [25] | 钟国防,周洪琪.木聚糖酶和复合酶制剂PS对尼罗罗非鱼生长性能、非特异性免疫能力的影响[J]. 海洋渔业,2005,27(4):286-291. ( 1) 1)
|
| [26] | 王芬,王灵坤.复合纤维素酶制剂对东北白鹅生长性能及免疫性能的影响[J]. 畜牧与兽医,2013,45(8):75-78. ( 1) 1)
|
| [27] | 何万领,李晓丽,王占彬,等.粗纤维素复合酶对肉鸡生产性能、消化酶活性及免疫功能的影响[J]. 中国粮油学报,2010,25(8):65-69. ( 1) 1)
|




