脂肪酸是人和动物所必需的能量物质和结构材料,脂肪酸的吸收、转运和代谢是机体能量平衡的重要决定因素。过去,人们普遍认为循环系统中的游离脂肪酸是通过自由扩散的方式通过细胞膜进入细胞。近年来,由多种蛋白质介导的脂肪酸跨膜转运逐渐被发现和确认,这些转运蛋白能够促进游离脂肪酸被不同的细胞吸收和排出。脂肪酸转运蛋白1(fatty acid transport protein 1,FATP1,也被称为SLC27A1)就是一种能够运输脂肪酸的跨膜蛋白,它是FATP蛋白家族6个成员中最先被发现也是最为重要的一员。研究表明FATP1能够特异性结合脂肪酸(特别是长链和超长链不饱和脂肪酸)并运输它们通过细胞膜[1, 2, 3, 4]。此外,还有试验表明,FATP1对于脂肪酸进入细胞后的代谢也有重要影响,它能够促进脂肪酸的酰基化[5, 6]。基于FATP1在脂肪酸转运和代谢中的关键性作用,许多研究都认为它对动物脂肪代谢和脂肪沉积具有重要的影响[7, 8, 9]。
猪的肌内脂肪(intramuscular fat,IMF)主要存在于肌纤维内,一般在出生后逐渐开始形成,在肥育期大量沉积[10]。肌内脂肪含量对于猪肉品质有重要影响,合适的肌内脂肪含量能够显著提高肉的风味和嫩度。荣昌猪是我国优良的地方猪种,具有高肌内脂肪沉积的特性。本试验旨在研究FATP1基因(也被称为SLC27A1基因)在荣昌猪不同组织中的表达规律,并分析猪肌肉中FATP1的表达与肌内脂肪沉积的相关性,以期为猪的遗传育种选育和动物脂肪代谢研究提供理论基础。
1 材料与方法 1.1 试验动物试验选用80只1日龄健康的荣昌仔猪正常饲养,分别在1、7、20、50、90、150日龄放血屠宰(n=5)。迅速分离背最长肌和半腱肌用于肌内脂肪含量检测,肌内脂肪含量测定采用索氏抽提法。另取背肌、腿肌、心脏、肝脏、背脂、腹脂、脾脏、肺脏、小肠组织样品在液氮中迅速冷冻,-80 ℃保存,用于总RNA和蛋白质提取。
1.2 荧光定量PCR和反转录PCR取-80 ℃冻存的组织样品约0.5 g,液氮中研磨粉碎,使用RNAiso Plus试剂盒(TaKaRa公司)提取样品中的总RNA,核酸定量仪检测RNA的浓度,1%琼脂糖凝胶电泳检测RNA完整性。使用反转录试剂盒(TaKaRa公司)将总RNA反转录为cDNA。反转录PCR检测FATP1基因的组织表达差异,使用BioRad公司梯度PCR仪进行反转录PCR反应,反应体系为:TaqMix(天根公司)12.5 μL,二乙基焦碳酸酯(diethypyrocar-bonate,DEPC)处理水9 μL,上游引物1 μL,下游引物1 μL,模板cDNA 1.5 μL。反应体系为:94 ℃预变性3 min;94 ℃变性30 s、58 ℃退火30 s、72 ℃延伸1 min 30个循环,72 ℃延伸5 min。1%凝胶电泳30 min检测PCR产物,凝胶成像系统读取电泳条带亮度值,以FATP1基因条带的亮度/β-肌动蛋白(β-actin)基因条带的亮度作相对定量计算。使用ABI公司的StepOne定量PCR系统检测FATP1基因的发育表达变化。荧光定量PCR反应使用SYBR Premix Ex TaqTM Ⅱ试剂盒(TaKaRa公司),反应体系为:SYBR Premix Ex TaqTM Ⅱ(2×) 12.5 μL,上游引物1 μL,下游引物1 μL,cDNA模板2 μL,ddH2O 8.5 μL。反应条件: 95 ℃预变性30 s;95 ℃ 5 s、 60 ℃ 35 s 40个循环。β-actin基因为参照基因,2-△△CT法计算基因的相对表达水平。PCR反应使用的FATP1基因引物序列:上游GGACCTCTGTCTTAGCCTCACT,下游CGCATCCTTCAGTCTTTGTTCT;β-actin基因引物序列:上游GCGGCATCCACGAAACTAC,下游TGATCTCCTTCTGCATCCTGTC。
1.3 Western blotting取0.5 g左右的新鲜组织样品冰上匀浆,加1 mL放射免疫分析(radio-immunoprecipitation assay,RIPA)蛋白裂解液(碧云天公司),冰上反应30 min,12 000 r/min 4 ℃离心10 min, 吸取上清液移入新的1.5 mL离心管中,煮沸10 min使蛋白质变性。使用二辛可宁酸(bicinchonininc acid,BCA)法蛋白浓度检测试剂盒(康为公司)检测样品总蛋白浓度。12%的十二烷基硫酸钠-聚丙烯酰胺凝胶(SDS-PAGE)进行蛋白质分离(60 V,4 h),然后转印到0.22 μm聚偏氟乙烯(polyvinylidene fluoride,PVDF)膜(Millipore公司)上。转印完的PVDF膜用5%的脱脂牛奶溶液室温封闭2 h。用FATP1的一抗溶液(多克隆兔抗,Sigma公司)4 ℃孵育过夜,用含有吐温-20的三羟甲基氨基甲烷(Tris buffered saline with Tween-20,TBST)溶液漂洗干净后使用二抗溶液(鼠抗兔,博士德公司)室温孵育1 h。最后用电化学发光试剂(electrochemiluminescence,ECL,Millipore公司)和自动发光曝光仪进行拍照分析。微管蛋白(tublin,单克隆鼠抗,碧云天公司)一抗作为内参抗体。
1.4 数据统计分析试验数据采用平均值±标准差表示,试验结果采用SPSS 13.0分析软件中的ANOVA过程进行单因素方差分析,采用Pearson法进行相关性分析,以P<0.05作为显著性标准。
2 结果与分析 2.1 FATP1基因及其编码蛋白质在荣昌猪上的组织表达差异FATP1基因及其编码的蛋白质在成年荣昌猪(90日龄)的不同组织器官中都有表达,但其表达水平存在明显的组织差异(图1)。在腿肌和心脏中,FATP1 mRNA表达水平最高,在背肌、背部皮下脂肪(背脂)、腹部内脏脂肪(腹脂)和肝脏中的表达水平其次,而在脾脏、肺脏和小肠中表达水平最低(图1A)。随后使用Western blotting方法检测FATP1蛋白在各个组织中表达情况的结果表明,同样是在肌肉组织(腿肌和背肌)中蛋白质表达水平最高(图1B)。综合上述2个检测结果发现,FATP1基因及其编码的蛋白质在成年猪的肌肉和心脏中表达水平最高,在肝脏和脂肪组织表达水平其次,在小肠和肺脏表达水平最低(图1C)。
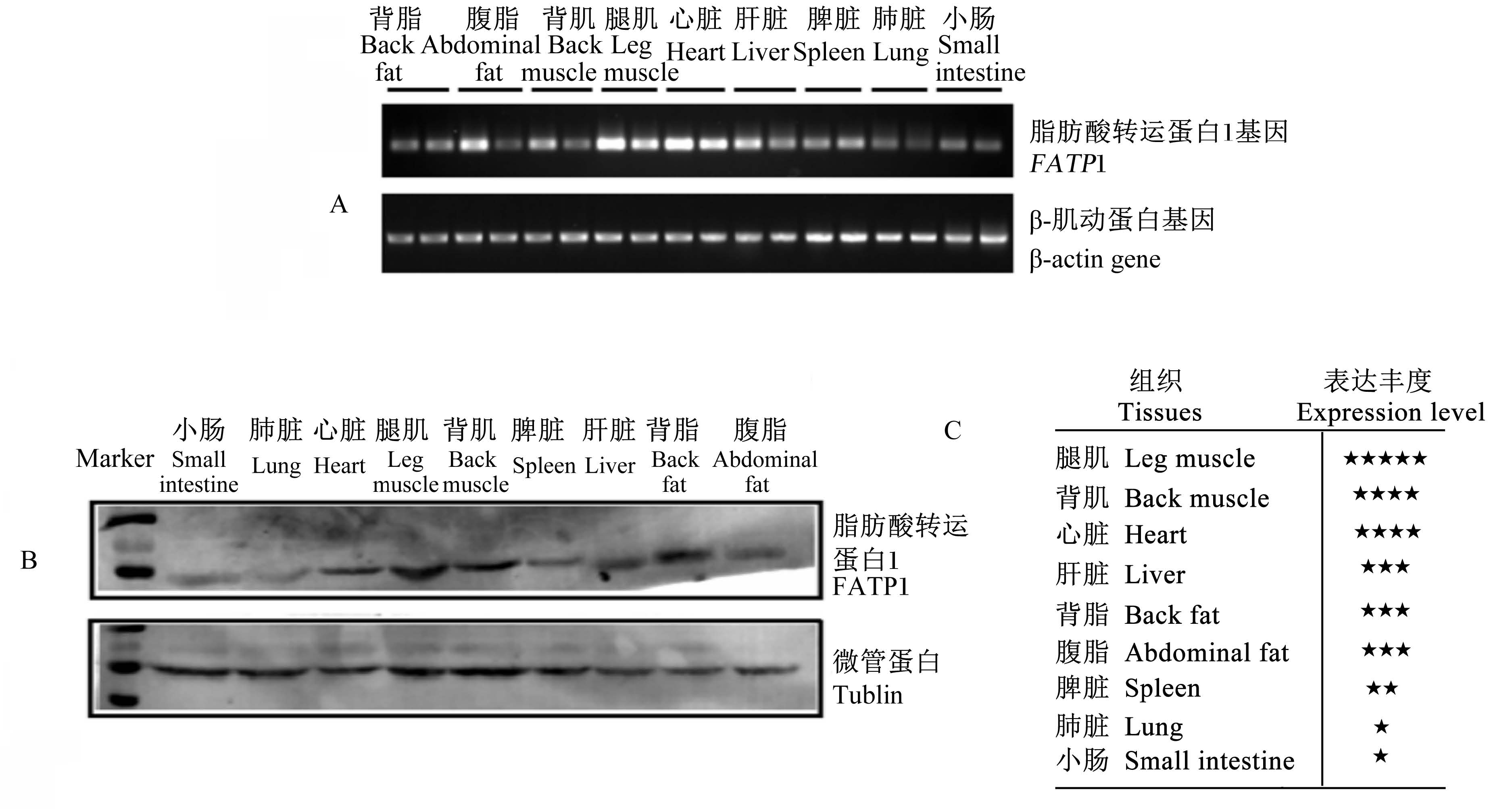 | A,FATP1 mRNA的组织表达 FATP1 mRNA expression level in the tissues;B,不同组织中的FATP1蛋白质水平FATP1 protein level in the tissues of pig;C,FATP1基因及其编码的蛋白质在不同组织间的表达差异比较 Expression levels comparison of FATP1 gene and its protein among different tissues。 图1 FATP1基因及其编码蛋白质在荣昌猪不同组织中表达水平 Fig. 1 Expression levels of FATP1 gene and its protein in different tissues of Rongchang pigs |
荧光定量PCR检测结果表明FATP1 mRNA在荣昌猪肌肉组织中的表达水平随着仔猪的生长呈现逐渐增高的趋势(表1)。50日龄以后的仔猪背肌中FATP1 mRNA表达水平开始显著高于1日龄仔猪(P<0.05),并达到一个较为稳定的水平。而在猪的腿肌中,FATP1 mRNA表达水平从90日龄开始显著高于1日龄(P<0.05),并维持较高水平。
| 表1 FATP1基因在荣昌猪发育过程肌肉中的表达变化 Table 1 Expression change of FATP1 gene in the muscle of Rongchang pigs during development |
如表2所示,荣昌猪背最长肌(背肌)的肌内脂肪和半腱肌(腿肌)的肌内脂肪含量均随着猪的生长而增加,并且在仔猪生长后期,肌内脂肪的沉积速度明显加快。与1日龄相比,150日龄时猪的背肌肌内脂肪含量约升高了3.0倍,而腿肌肌内脂肪含量约升高了2.6倍。以FATP1 mRNA表达水平和肌内脂肪含量做相关性分析,结果显示两者在荣昌猪的背肌和腿肌中均显著相关(P<0.05)。
| 表2 肌内脂肪含量与FATP1 mRNA表达水平的相关性 Table 2 Correlation between IMF content and FATP1 mRNA expression level |
脂肪酸的跨膜转运是脂肪代谢的核心问题之一,但长久以来存在很多争议的地方。由于细胞膜的磷脂双分子层结构,过去人们普遍认为游离脂肪酸能够轻易地以自由扩散的方式通过细胞膜[2]。虽然人们推测可能存在其他途径,但是由于缺少直接的证据而不能确认。随着分子生物学和细胞生物学技术手段的快速发展,最近10多年来,一些介导脂肪酸跨膜转运的蛋白质因子相继被发现和确认,它们包括:FATP1、脂肪酸结合蛋白(fatty acid binding protein,FABP)、脂肪酸移位酶(fatty acid translocase,FAT)、长链脂酰基辅酶A合成酶(long chain acyl coenzyme A synthetase,LACS)等[11, 12, 13]。这些膜蛋白和胞浆蛋白能够单独 地或者共同地通过结合和传递的方式把循环中的游离脂肪酸转运进细胞内部,或者把细胞内合成的脂肪酸转运到细胞外部。在这个蛋白质介导的脂肪酸转运体系里,FATP1似乎是最重要的一员,它既可以单独形成穿越细胞膜的通道,使脂肪酸直接通过细胞膜,又可以与FAT和FABP互作,共同协作来传递游离脂肪酸。
目前,关于FATP1的研究主要集中在人、细胞系或者一些模式生物上进行,如小鼠和斑马鱼等。相比而言,在传统家畜家禽上关于FATP1的研究还比较少。王彦[14]研究了FATP1基因在鸡上的表达模式并进行了单核苷酸多态性(SNP)分析,发现FATP1基因在不同鸡的品种间表达差异不显著(P>0.05),而不同的FATP1基因型与鸡的腹脂率、腿肌率、净膛重等屠宰性状具有显著的正相关(P<0.05)。罗轶[15]试验发现FATP1基因在鸡的胚胎期骨骼肌中表达水平显著高于其他组织(P<0.05),而到了发育后期则是在脑部和骨骼肌中的表达水平显著高于心脏、肝脏和脂肪组织(P<0.05),并且骨骼肌中FATP1基因的表达水平与肌内脂肪含量正相关(P<0.05),但与皮下脂肪厚度不相关(P>0.05)。华绪川等[16]针对FATP1基因5′调控区的多态性进行研究,发现FATP1-586位点的不同基因型与猪的背膘厚、板油重等脂肪性状具有密切关系(P<0.05)。本试验结果显示FATP1基因及其编码的蛋白质在荣昌猪体内广泛表达,在肌肉组织和心脏中的表达水平明显高于其他组织,而腿肌中的表达水平又明显高于背肌中的表达。与此结果相似,Wang等[7]检测发现FATP1基因在鸡上的表达具有年龄依赖性变化,并且在胸肌和腿肌中的表达水平显著高于其他组织(P<0.05)。Gallardo等[8]最近检测了FATP家族6个成员在猪上的表达特征,发现FATP1~6基因分别定位在猪的6个不同染色体上,家族成员的组织表达差异十分明显。以上可知,FATP1基因在动物的肌肉中普遍有高水平表达,这很有可能与肌细胞大量摄取脂肪酸进行氧化供能有关。此外,FATP1基因的表达水平和基因型的差异与肌内脂肪的形成和沉积具有密切联系,可以作为猪育种选育的一个分子标记。
肌内脂肪含量与肉的嫩度、系水力和风味密切相关,适宜的肌内脂肪含量能够提升猪肉品质。荣昌猪是我国西南地区的优良地方猪种,达上市体重的荣昌猪肌内脂肪含量一般能够达到3%~5%,是外种猪的数倍。本试验结果显示在荣昌猪的整个生长周期,FATP1及其编码的蛋白质在猪肌肉组织中都有较高的表达水平,推测其在荣昌猪高肌内脂肪沉积的产生和积聚过程中扮演了极为重要的角色,具体分子机制方面的研究目前正在深入开展。
4 结 论① FATP1基因及其编码的蛋白质在荣昌猪的肌肉组织中显著高表达。
② 随着荣昌猪的生长,FATP1基因在腿肌和背肌中表达水平逐渐升高,并从生长中期(90日龄)开始维持稳定的高水平。
③ 肌肉中FATP1基因的表达水平与猪的肌内脂肪含量呈显著正相关。
| [1] | SCHAAP F G,HAMERS L,VAN DER VUSSE G J,et al.Molecular cloning of fatty acid-transport protein cDNA from rat[J]. Biochimica et Biophysica Acta,1997,1354(1):29-34. ( 1) 1)
|
| [2] | DOEGE H,STAHL A.Protein-mediated fatty acid uptake:novel insights from in vivo models[J]. Physiology,2006,21:259-268. ( 2) 2)
|
| [3] | STAHL A.A current review of fatty acid transport proteins (SLC27)[J]. Pflügers Archiv,2004,447(5):722-727. ( 1) 1)
|
| [4] | HARASIM E,KALINOWSKA A,CHABOWSKI A,et al.The role of fatty-acid transport proteins (FAT/CD36,FABPpm,FATP) in lipid metabolism in skeletal muscles[J]. Postepy Higieny i Medycyny Doswiadczalnej,2008,62:433-441. ( 1) 1)
|
| [5] | BERGER J,TRUPPE C,NEUMANN H,et al.A novel relative of the very long-chain acyl-CoA synthetase and fatty acid transporter protein genes with a distinct expression pattern[J]. Biochemical and Biophysical Research Communications,1998,247(2):255-260. ( 1) 1)
|
| [6] | WATKINS P A,PEVSNER J,STEINBERG S J.Human very long-chain acyl-CoA synthetase and two human homologs:initial characterization and relationship to fatty acid transport protein[J]. Prostaglandins,Leukotrienes and Essential Fatty Acids,1999,60(5/6):323-328. ( 1) 1)
|
| [7] | WANG Y,ZHU Q,ZHAO X L,et al.Age-related expression profile of the SLC27A1 gene in chicken tissues[J]. Molecular Biology Reports,2011,38(8):5139-5145. ( 2) 2)
|
| [8] | GALLARDO D,AMILLS M,QUINTANILLA R,et al.Mapping and tissue mRNA expression analysis of the pig solute carrier 27A (SLC27A) multigene family[J]. Gene,2013,515(1):220-223. ( 2) 2)
|
| [9] | SONG Y Z,FENG J Y,ZHOU L H,et al.Molecular cloning and ontogenesis expression of fatty acid transport protein-1 in yellow-feathered broilers[J]. Journal of Genetics and Genomics,2008,35(6):327-333. ( 1) 1)
|
| [10] | 张海燕,姜学,尹靖东.猪肌内脂肪沉积的营养调控及候选基因的研究进展[J]. 中国畜牧杂志,2009,45(21):60-64. ( 1) 1)
|
| [11] | 齐仁立,黄金秀,杨飞云,等.脂肪酸转运蛋白家族及其介导的脂肪酸跨膜转运[J]. 动物营养学报,2013,25(5):905-911. ( 1) 1)
|
| [12] | POHL J,RING A,KORKMAZV,et al.FAT/CD 36-mediated long-chain fatty acid uptake in adipocytes requires plasma membrane rafts[J]. Molecular Biology of the Cell,2005,16(1):24-31. ( 1) 1)
|
| [13] | NICKERSON J G,ALKHATEEB H,BENTON C R,et al.Greater transport efficiencies of the membrane fatty acid transporters fat/cd36 and fatp4 compared with fabppm and fatp1 and differential effects on fatty acid esterification and oxidation in rat skeletal muscle[J]. The Journal of Biological Chemistry,2009,284(24):16522-16530. ( 1) 1)
|
| [14] | 王彦.鸡FATP1/FATP4基因的克隆、表达及其与屠体性状的关联分析[D]. 博士学位论文.雅安:四川农业大学,2009:8-21. ( 1) 1)
|
| [15] | 罗轶.鸡FATP1基因cDNA的克隆、组织表达及其生物信息学分析[D]. 硕士学位论文.雅安:四川农业大学,2008:12-30. ( 1) 1)
|
| [16] | 华绪川,张立凡,蔡兆伟,等.猪FATP1基因5'调控区多态性及其与脂肪性状的相关分析[J]. 江苏农业学报,2011,27(1):89-93. ( 1) 1)
|




