2. 河南农业大学生命科学学院, 郑州 450002;
3. CAAS-ICRAF农用林业与 可持续畜牧业联合实验室, 北京 100193;
4. 东北农业大学, 食品安全与营养协同创新中心, 哈尔滨 150030
2. College of Life Science, Henan Agricultural University, Zhengzhou 450002, China;
3. CAAS-ICRAF Joint Laboratory on Agroforestry and Sustainable Animal Husbandr, Beijing 100193, China;
4. Synergetic Innovation Center of Safety and Nutrition, Northeast Agricultural University, Harbin 150030, China
microRNAs(miRNAs)是一类小的非编码RNAs,它能够在转录后调节基因表达,从而影响多种生物学过程,包括细胞增殖[1]、分化[2]、凋亡[3]、发育[4]。microRNA-145(miR-145)由于其在肿瘤和癌症方面的抑制作用而引起人们的关注。在许多人类癌症中都观察到miR-145表达的下调,包括前列腺癌[5]、膀胱癌[6]、结肠癌[7]。2007年Gu等[8]首次在荷斯坦奶牛乳腺组织中发现了miR-145的存在。Wang等[9]在对不同泌乳阶段乳腺组织中miRNAs的表达谱进行检测时发现,miR-145在分娩前后,即泌乳启动阶段,表达变化差异显著。这提示bta-miR-145可能在奶牛泌乳启动或乳成分合成过程中发挥一定作用。
目前,对bta-miR-145靶基因的研究甚少,没有明确得到鉴定的靶基因的信息。为了研究bta-miR-145在泌乳过程中的功能,本研究首先使用TargetScan 6.2软件预测bta-miR-145潜在的靶基因,结果发现与乳蛋白合成相关的胰岛素样生长因子1受体(IGF1R)、胰岛素受体底物1(IRS1)和β-酪蛋白(CSN2)位列其中。Shi等[10]研究证明,hsa-miR-145可以通过靶向人的IGF1R和IRS1基因发挥功能。miRNAs常常靶向同一信号通路中的多个靶基因[11],IGF1R、IRS1和CSN2都位于胰岛素样生长因子1受体-磷脂酰肌醇3激酶-蛋白激酶B/哺乳动物雷帕霉素靶蛋白(IGF1R-PI3K-Akt/mTOR)信号通路。在正常情况下,PI3K-Akt/mTOR信号通路受上游酪氨酸激酶受体调节,尤其是IGF1R[12],而下游mTOR信号通路对乳蛋白合成起着核心作用[13]。因此,有必要开展bta-miR-145对IGF1R-PI3K-Akt/mTOR信号通路作用的研究。本试验选择原代奶牛乳腺上皮细胞为研究对象,通过转染bta-miR-145过表达模拟物(mimic)取得bta-miR-145过表达作用,转染bta-miR-145抑制表达模拟物(inhibitor)取得bta-miR-145抑制表达作用,研究bta-miR-145对IGF1R-PI3K-Akt/mTOR信号通路相关基因表达的影响,为bta-miR-145的功能研究奠定基础,同时为从miRNAs的角度研究奶牛的泌乳调控提供依据。
1 材料与方法 1.1 细胞处理将原代奶牛乳腺上皮细胞以1×105个/mL接种于6孔板,用DMEM/F12(Gibco公司)+10%胎牛血清(FBS,Gibco公司)培养基培养24 h。然后用DMEM/F12的无血清培养基处理12 h,再用诱导培养基,即在DMEM/F12基础培养基中添加1 μg/mL地塞米松(Sigma公司)、5 μg/mL催乳素(Sigma公司)、5 μg/mL胰岛素(Sigma公司)和100 ng/mL胰岛素样生长因子-1(IGF-1,Sigma公司),继续培养12 h,之后进行瞬时转染。
1.2 瞬时转染试验设置5个组,对照组为非转染空白对照;bta-miR-145过表达组(Mimic组),转染mimic 150 pmol/孔(上海吉玛公司);mimic阴性对照组 (Mimic-NC组),转染mimic-NC 150 pmol/孔(上 海吉玛公司);bta-miR-145抑制表达组(Inhibitor组),转染inhibitor 300 pmol/孔(上海吉玛公司);inhibitor阴性对照组(Inhibitor-NC组),转染inhibitor-NC 300 pmol/孔(上海吉玛公司),每组3个重复。以LipofectamineTM2000(Invitrogen公司)为转染试剂,转染的具体操作参照说明书。转染处理细胞24 h后,去除上清,磷酸盐缓冲液(PBS)清洗3遍,然后用Trizol试剂1 mL/孔裂解细胞,提取RNA。
1.3 样品RNA提取样品RNA的提取参考Trizol试剂盒说明书,具体的操作步骤为:每个直径为3.5 cm的培养板添加1 mL Trizol,反复吹打细胞,之后全部移入1.5 mL的离心管中,室温裂解细胞10 min;然后加氯仿0.2 mL,摇振15 s,置室温2~3 min,4 ℃以下1 000×g离心5 min,吸上层水相,移至另一离心管中,加0.5 mL异丙醇,置室温10 min;之后,4 ℃以下1 000×g离心5 min,弃上清,加1 mL 75%乙醇至离心管中,摇振,充分洗涤沉淀,4 ℃以下1 000×g离心5 min,再次弃上清,真空干燥,将沉淀重悬于无RNase的水中。
应用紫外分光光度计检测RNA的浓度,样品的1.8<(OD260 nm/OD280 nm)<2.0可用于后续的反转录反应。
1.4 反转录按照TaKaRa的PrimeScript RT reagent Kit With gDNA Eraser试剂盒说明书进行反转录操作。
首先,进行基因组DNA的去除反应,见表1。
| 表1 基因组DNA的去除反应 Table 1 Reaction of genome DNA removing |
将上述混合液标记为①,置于PCR仪上42 ℃ 2 min,4 ℃保存。接着,反转录操作见表2。
| 表2 反转录反应 Table 2 Reverse transcription reaction μL |
将上述混合液标记为②,置于PCR仪上,37 ℃ 15 min,85 ℃ 5 s,4 ℃保存。这样就得到了cDNA第一链,样品长期保存可放-20 ℃。
1.5 实时定量PCR引物设计与合成表3为本试验所检测基因在细胞信号通路中的作用。
| 表3 基因及所属的信号通路 Table 3 Genes and their signal pathways |
应用Primer Primier 5.0软件进行16个基因的引物设计,引物均由北京六合华大基因有限公司合成。引物序列如表4所示。
| 表4 引物序列 Table 4 Primer sequence |
根据TaKaRa的SYBR Green说明书进行实时定量PCR,见表5。
| 表5 实时定量 PCR体系 Table 5 Real-time qPCR system μL |
实时定量PCR在ABI 7500上进行,反应程序如下:95 ℃预变性30 s;95 ℃变性5 s,60 ℃延伸34 s,重复40个循环;增加熔解曲线。荧光定量的最后获得的循环阈值(Ct)用2-ΔΔCt方法进行数据计算,以甘油醛-3-磷酸脱氢酶(GAPDH)基因为内参。
1.7 潜在靶基因与bta-miR-145结合位点的分析对上述基因表达的结果进行分析,找到bta-miR-145过表达时有显著下调的基因与抑制表达时有显著上调基因的交集,此交集即为bta-miR-145潜在的靶基因。在NCBI核酸数据库中找到该基因的3′非翻译区(3′UTR)。通过 RNAhybrid数据库(http://bibiserv.techfak.uni-bielefeld.de/rnahybrid/)找到潜在的bta-miR-145结合位点,并分析结合位点的最小自由能。
1.8 数据统计数据采用SAS 9.0的one-way ANOVA程序进行统计分析。
2 结果与分析 2.1 bta-miR-145过表达对IGF1R-PI3K-Akt/mTOR信号通路相关基因表达的影响从表6可知,bta-miR-145过表达后引起蛋白激酶B3(Akt3)、真核生物翻译起始因子4E(EIF4E)基因mRNA表达量发生显著下调(P<0.05)。miRNA的过表达会引起它所靶向基因的mRNA表达下调[10],因此这个结果说明bta-miR-145可能靶向Akt3、EIF4E基因。
| 表6 bta-miR-145过表达对IGF1R-PI3K-Akt/mTOR信号通路相关基因表达的影响 Table 6 Effects of bta-miR-145 over-expression on IGF1R-PI3K-Akt/mTOR signal pathway related gene expressions |
从表7可知,bta-miR-145抑制表达后引起EIF4E、溶解物载体家族3成员2(SLC3A2)、溶解物载体家族7成员1(SLC7A1)基因mRNA表达量发生显著上调(P<0.05)。一种miRNA会引起它所靶向基因的mRNA表达下调,同样,如果抑制这个miRNA的表达,会相应引起它所靶向基因的mRNA发生相应上调[10]。表7的结果说明bta-miR-145可能靶向EIF4E、SLC3A2、SLC7A1基因。而薯球蛋白(TSC2)这个基因在Inhibitor组与对照组相比显著上调(P<0.05),但与Inhibitor-NC组相 比差异不显著(P>0.05),因此TSC2基因不能作为bta-miR-145的备选靶基因。
| 表7 bta-miR-145抑制表达对IGF1R-PI3K-Akt/mTOR信号通路相关基因表达的影响 Table 7 Effects of bta-miR-145 down-expression on IGF1R-PI3K-Akt/mTOR signal pathway related gene expressions |
从图1可知,bta-miR-145过表达引起显著下调的基因有:Akt3、EIF4E,bta-miR-145抑制表达引起显著上调的基因有:SLC3A2、SLC7A1、EIF4E,它 们的交集为EIF4E。根据miRNA在转录后调节 基因表达,可以引起靶基因mRNA降解的特性[10],EIF4E基因最有可能是bta-miR-145的靶标。
没有基因在bta-miR-145过表达时显著上调,抑制表达时显著下调。
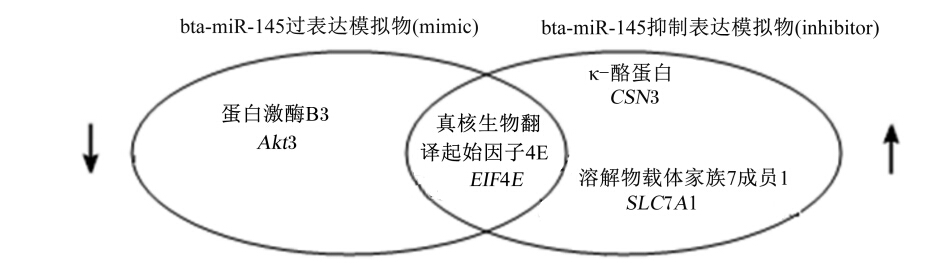 | 图1 bta-miR-145过表达和抑制表达后有显著影响的基因分析 Fig. 1 Analysis for significant effect of gene after bta-miR-145 over-expression and down-expression |
牛的EIF4E在NCBI中的序列号为:NM_174310.3,下载其3'UTR,长度为971 bp,将其输入到RNAhybrid数据库,分析结果见表8。
| 表8 潜在结合位点的最小自由能及其二级结构 Table 8 Minimum free energy and secondary structure of potential binding site |
由表8可知bta-miR-145与EIF4E的结合位点的最小自由能为-0.083 6 kJ/mol,一般认为最小自由能(△G)≤-0.062 7 kJ/mol是可以结合的[14]。
3 讨 论一些研究学者在做miRNA的靶基因研究时会采用芯片的检测方式,这种检测方式最大的优点是高通量,但是试验成本比较大[15]。本研究采用生物信息学分析、文献检索和实时定量PCR相结合的方式进行miRNA的靶基因研究,试验的成本低、针对性强。miRNA的作用方式主要是转录后调控,即引起靶基因mRNA的降解,或者翻译的抑制[2, 16]。本试验在mRNA水平主要检测bta-miR-145引起降解的部分靶基因。
常用的知名的miRNA靶基因预测软件主要包括TargetScan、TargetScanS、miRanda、PicTar、rna22,万季[17]对这些软件的敏感度、假阳性率、信噪比等进行测评,发现TargetScan的敏感度最高。因此,本研究选取TargetScan作为预测软件。由于没有专门用于牛物种的靶基因预测软件,我们收集了PubMed上的文献报道,来提高试验的可行性。Shi等[10]报道hsa-miR-145靶向人的IGF1R和IRS1基因。本试验中bta-miR-145对牛IGF1R和IRS1基因的mRNA表达没有显著的影响,说明bta-miR-145对这2个基因的mRNA没有明显的调节作用。
CSN2是牛奶中丰度最高的蛋白质之一,平均含量达到37%[18]。在牛乳腺上皮细胞中,CSN2基因的表达受泌乳类激素及启动子区多种调节元件的控制[18]。目前没有转录后水平,尤其是miRNA水平,调节CSN2基因表达的报道。鉴于CSN2的重要作用,根据TargetScan预测,本试验也研究了bta-miR-145对CSN2基因mRNA的调节作用,结果表明在mRNA水平bta-miR-145并没有调节CSN2基因的表达。
本试验的意外收获是发现了bta-miR-145过表达时显著下调而抑制表达时显著上调的基因——EIF4E。EIF4E是一种帽子结合蛋白,可以特异性地识别mRNA的5′端帽子结构,在真核生物翻译起始过程中发挥重要作用[19]。研究人员[20, 21]认为PI3K-Akt/mTOR信号通路调节可以通过EIF4E来提高mRNA的翻译起始效率。尽管EIF4E基因不在TargetScan 6.2预测的bta-miR-145的靶标范围,但是通过RNAhybrid数据库现bta-miR-145与EIF4E存在潜在结合位点,其结合位点的最小自由能小于-0.062 7 kJ/mol。Chen等[22]已用试验证实hsa-miR-145靶向人EIF4E基因。本试验结果表明bta-miR-145对牛EIF4E基因的mRNA表达有显著的调控作用,再根据结合位点的分析结果,EIF4E很有可能是bta-miR-145的靶基因。miRNA靶基因的确定需要进行一系列的生物学试验,本研究为后续bta-miR-145靶向EIF4E基因的研究奠定了基础,为bta-miR-145调控奶牛泌乳及乳蛋白合成提供了一定的依据。
4 结 论bta-miR-145过表达和抑制表达对IGF1R-PI3K-Akt/mTOR信号通路相关基因表达产生一定影响,但并没有引起bta-miR-145预测靶标IGF1R、IRS1、CSN2基因的mRNA发生显著变化;bta-miR-145过表达可引起EIF4E基因mRNA的显著下调,抑制表达引起EIF4E基因mRNA的显著上调,并且通过生物信息学分析发现牛EIF4E基因3′UTR上存在bta-miR-145的结合位点,以上结果提示EIF4E基因为bta-miR-145的潜在靶标。
| [1] | CHEN J F,MANDEL E M,THOMSON J M,et al.The role of microRNA-1 and microRNA-133 in skeletal muscle proliferation and differentiation[J]. Nature Genetics,2006,38(2):228-233. ( 1) 1)
|
| [2] | BARTEL D P.MicroRNAs:genomics, biogenesis,mechanism,and function[J]. Cell,2004,116(2):281-297. ( 2) 2)
|
| [3] | ZHANG B H,PAN X P,COBB G P,et al.MicroRNAS as oncogenes and tumor suppressors[J]. Developmental Biology,2007,302(1):1-12. ( 1) 1)
|
| [4] | AMBROS V,BARTEL B,BARTEL D P,et al.A uniform system for microRNA annotation[J]. RNA,2003,9(3):277-279. ( 1) 1)
|
| [5] | ZAMAN M S,CHEN Y,DENG G,et al.The functional significance of microRNA-145 in prostate cancer[J]. British Journal of Cancer,2010,103(2):256-264. ( 1) 1)
|
| [6] | CHIYOMARU T,ENOKIDA H,TATARANO S,et al.miR-145 and miR-133a function as tumour suppressors and directly regulate FSCN1 expression in bladder cancer[J]. British Journal of Cancer,2010,102(5):883-891. ( 1) 1)
|
| [7] | ARNDT G M,DOSSEY L,CULLEN L M,et al.Characterization of global microRNA expression reveals oncogenic potential of miR-145 in metastatic colorectal cancer[J]. BMC Cancer,2009,9(1):374. ( 1) 1)
|
| [8] | GU Z L,ELESWARAPU S,JIANG H L.Identification and characterization of microRNAs from the bovine adipose tissue and mammary gland[J]. Febs Letters,2007,581(5):981-988. ( 1) 1)
|
| [9] | WANG M,MOISÁ S,KHAN M J,et al.MicroRNA expression patterns in the bovine mammary gland are affected by stage of lactation[J]. Journal of Dairy Science,2012,95(11):6529-6535. ( 1) 1)
|
| [10] | SHI B,SEPP-LORENZINO M,PRISCO L,et al.MicroRNA 145 targets the insulin receptor substrate-1 and inhibits the growth of colon cancer cells[J]. Journal of Biological Chemistry,2007,282(45):32582-32590. ( 5) 5)
|
| [11] | CUI Q,YU Z,PURISIMA E O,et al.Principles of microRNA regulation of a human cellular signaling network[J]. Molecular Systems Biology,2006,2:46. ( 1) 1)
|
| [12] | HIXON M L,PACCAGNELLA L,MILLHAM R,et al.Development of inhibitors of the IGF-IR/PI3K/Akt/mTOR pathway[J]. Reviews on Recent Clinical Trials,2010,5(3):189-208. ( 1) 1)
|
| [13] | BIONAZ M, LOOR J J.Gene networks driving bovine mammary protein synthesis during the lactation cycle[J]. Bioinformatics and Biology Insights,2011,5:83-98. ( 1) 1)
|
| [14] | HOFACKER I L.Vienna RNA secondary structure server[J]. Nucleic Acids Research,2003,31(13):3429-3431. ( 1) 1)
|
| [15] | TANAKA T,HANEDA S,IMAKAWA K,et al.A microRNA,miR-101a,controls mammary gland development by regulating cyclooxygenase-2 expression[J]. Differentiation:Research in Biological Diversity,2009,77(2):181-187. ( 1) 1)
|
| [16] | BARTEL D P.MicroRNAs:target recognition and regulatory functions[J]. Cell,2009,136(2):215-233. ( 1) 1)
|
| [17] | 万季.microRNA靶标预测软件的测评及靶标基因特征分析[D]. 硕士学位论文.武汉:华中科技大学,2007:35-36. ( 1) 1)
|
| [18] | LEE P,CHUNG H K,LEE H G,et al.Cloning and characterization of 5'-untranslated region of porcine beta casein gene (CSN2)[J]. Domestic Animal Endocrinology,2008,35(3):245-53. ( 2) 2)
|
| [19] | FISCHER P M.Cap in hand:targeting eIF4E[J]. Cell Cycle,2009,8:2535-2541. ( 1) 1)
|
| [20] | DE BENEDETTI A,GRAFF J R.eIF-4E expression and its role in malignancies and metastases[J]. Oncogene,2004,23(18):3189-3199. ( 1) 1)
|
| [21] | JIA Y,POLUNOVSKY V,BITTERMAN P B,et al.Cap-dependent translation initiation factor eIF4E:an emerging anticancer drug target[J]. Medicinal Research Reviews,2012,32(4):786-814. ( 1) 1)
|
| [22] | CHEN Z,ZENG H Z,GUO Y,et al.miRNA-145 inhibits non-small cell lung cancer cell proliferation by targeting c-Myc[J]. Journal of Experimental & Clinical Cancer Research,2010,29:151. ( 1) 1)
|