胰高血糖素样肽-2(glucagon like peptide-2,GLP-2)通过特异性促进肠上皮细胞增殖、抑制肠上皮细胞凋亡[1]、抑制胃酸分泌[2]、降低肠道渗透性[3]、增加肠道血供[4]等促进损伤肠黏膜的结构恢复以及吸收功能和屏障功能的改善,且GLP-2的作用效果强于以往发现的其他非特异的肠生长因子。Pedersen等[5]证明猪胰高血 糖 素 样 肽-2(pGLP-2)与人胰高血 糖 素 样 肽 -2(hGLP-2)对肠道的作用效果相同,能够显著增加小鼠小肠的重量和长度以及回肠的横截面积。以上研究结果为pGLP-2治疗各种因素引起的仔猪肠道损伤和功能紊乱提供了理论依据[6]。但pGLP-2在体内的半衰期非常短,只有8.4 min,极易被血液中的二肽酰肽酶-Ⅳ(dipeptidyl peptidase-Ⅳ,DPP-Ⅳ)快速降解[5],为了维持一定的疗效需要大剂量频繁用药。聚乙二醇(polyethylene glyeol,PEG)修饰是延长多肽类药物半衰期的一个有效途径。Lee等[7]证明PEG修饰后GLP-1的半衰期延长,酶解稳定性提高。目前,关于PEG修饰GLP-2的研究,仅见本课题组[8]使用单甲氧基聚乙二醇琥珀酰亚胺丙酸酯(mPEG5k-SPA)对pGLP-2进行修饰,使用一步阳离子交换层析法成功分离得到的mPEG-Lys30-pGLP-2可防止酶的快速降解和缓解小鼠结肠炎性病变。鉴于pGLP-2对肠道修复的作用及机理尚不明确,且PEG-pGLP-2对小鼠结肠紧密连接蛋白和炎性因子基因表达的影响未见报道,本试验旨在通过给小鼠饮用葡聚糖硫酸钠(dextran sulfate sodium,DSS)建立小鼠结肠炎模型,研究PEG-pGLP-2对结肠炎小鼠肠道紧密连接蛋白和炎性因子基因表达的影响,为探明其作用机理提供试验依据。
1 材料与方法 1.1 试验材料pGLP-2-(1~35)(纯度大于98%)由上海吉尔生化有限公司合成。mPEG-SPA(分子质量为5 ku)购自北京凯正生物技术公司。CM Sepharose Fast Flow树脂购自瑞士GE医疗生物科技公司。相对分子质量为3 000的超滤离心管购自美国Millipore公司。DSS(相对分子质量为36 000~50 000)购自上海MP公司。RNA提取试剂RNAiso Plus、反转录试剂盒PrimeScript RT-reagent Kit和荧光定量试剂盒SYBR Premix Ex TaqTM均为TaKaRa公司产品。
1.2 PEG-pGLP-2的制备参考Qi等[8]的方法,1.2 mg/mL pGLP-2 (相对分子质量为3 990.1)溶解于50 mmol/L Tris-HCl缓冲液(pH 8.5),与mPEG-SPA以1 ∶ 6的摩尔比室温下反应30 min,1%的三氟乙酸(TFA)终止反应。PEG修饰pGLP-2的混合物用阳离子交换层析进行分离。柱子填料为CM Sepharose Fast Flow弱酸性阳离子交换树脂,平衡缓冲液为pH 4.0 20 mmol/L的醋酸缓冲液,洗脱液为pH 4.0 20 mmol/L的醋酸缓冲液+1 mol/L NaCl溶液。PEG修饰pGLP-2的混合物用5倍体积的平衡缓冲液以1 mL/min的速度洗涤后,用0~100%的洗脱液按同样的流速洗脱100 min,215 nm监测,收集各洗脱峰,用相对分子质量3 000的超滤离心管除去NaCl,冻干保存。
1.3 试验动物试验在浙江省农业科学院畜牧兽医研究所试验动物房进行。将24只18~20 g的BALB/C雄鼠按体重随机分为4组,每组6只,单笼饲养。自由采食,每日更换剩余鼠料,空调控温,饲养温度为(24±1) ℃,光照周期12 h明12 h暗,每2~3 d更换垫料1次。饮水组小鼠第1~10天每天自由饮用蒸馏水,DSS组小鼠第1~10天每天饮用3% DSS,DSS+pGLP-2组第1~10天每天饮用3%DSS,第8天腹腔注射30 μg的pGLP-2,DSS+PEG-pGLP-2组第1~10天每天饮用3%DSS,第8天腹腔注射30 μg的PEG-pGLP-2,每天观察小鼠的精神、活动、毛发、饮食及粪便状态。
1.4 测定指标与方法试验第11天,小鼠空腹12 h后称重,颈椎脱臼法处死小鼠,沿腹中线打开腹腔,取出0.5 cm的结肠放入RNA Locker中,用于总RNA的提取。总RNA的提取按照RNAiso Plus说明书操作,将提取得到的RNA溶解于焦碳酸二乙酯(DEPC)处理水中,分别取1 μL样品测定RNA的纯度,OD260/280=1.8~2.0。按照PrimeScript RT-reagent Kit说明书,37 ℃ 15 min、85 ℃ 5 s反转录至50 μL体系。引物序列见表1。按照SYBR Premix Ex TaqTM说明书中的两步法PCR扩增条件进行,95 ℃预变性30 s后,95 ℃ 5 s、62 ℃ 34 s,40个循环,添加熔解曲线检测发现熔解曲线为单峰,说明产物特异性高。取高浓度的cDNA用分子试验用水2倍逐级稀释至2-6,制作标准曲线,扩增效率为90%~110%(标准曲线见图1),故可以使用2-△△Ct法对不同组别间基因的mRNA相对表达量进行计算。每组6个结肠样品分别进行检测。
| 表1 实时定量PCR引物序列 Table 1 Real-time quantitative PCR primer sequences |
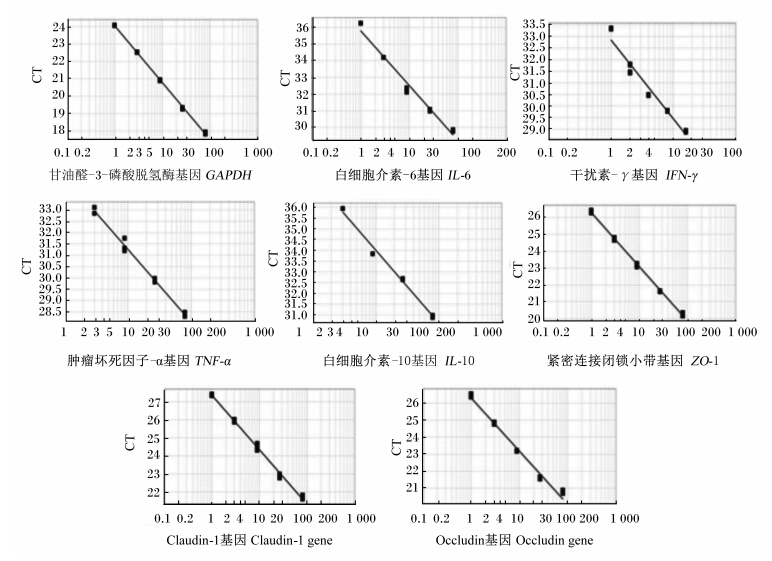 | 图1 目的基因和内参基因的扩增标准曲线 Fig. 1 Amplification standard curves of objective genes and reference genes |
采用SAS 6.12统计软件对数据进行单因素方差分析(one-way ANOVA)及Duncan氏法多重比较检验,试验数据以“平均值±标准差”表示。
2 结 果 2.1 小鼠临床表现饮用DSS的小鼠第3天体重开始下降,懒动,精神萎靡,毛发失去光泽,拱背,并且逐渐出现稀便,血便,试验第7天全部出现严重血便。DSS+pGLP-2组小鼠体重下降,稀粪血便也较严重。DSS+PEG-pGLP-2组小鼠随着治疗时间的延长症状有所缓解,采食量逐渐增加。对照组小鼠饮食活动正常,毛发有光泽,无便血。
2.2 炎性因子相关基因的mRNA相对表达量由表2可知,与饮水组相比,DSS组小鼠结肠白细胞介素-6(IL-6)、干扰素-γ(IFN-γ)和白细胞介素-10基因(IL-10)的mRNA相对表达量极显著升高(P<0.01);与DSS组相比,一次注射pGLP-2或PEG-pGLP-2可极显著抑制DSS引起的IL-6、IFN-γ和IL-10的mRNA相对表达量升高 (P<0.01)。肿瘤坏死因子-α基因(TNF-α)的mRNA相对表达量4个组之间没有显著差异(P>0.05)。
| 表2 PEG-pGLP-2对试验性结肠炎性因子相关基因mRNA相对表达量的影响 Table 2 Eeffects of PEG-pGLP-2 on gene mRNA expression levels of inflammatory cytokines in experimental colitis |
由表3可知,与饮水组相比,DSS组小鼠结肠ZO-1的mRNA相对表达量极显著降低(P<0.01)。与DSS组相比,一次注射pGLP-2对ZO-1的mRNA相对表达量没有显著影响(P>0.05);而 一次注射PEG-pGLP-2可以极显著增加ZO-1的 mRNA相对表达量(P<0.01)。claudin-1基因的mRNA相对表达量4个组之间没有显著差异(P>0.05)。DSS组和饮水组occludin基因的mRNA相对表达量没有差异(P>0.05),注射pGLP-2和PEG-pGLP-2 occludin基因的mRNA相对表达量极显著低于饮水组(P<0.01)。
| 表3 PEG-pGLP-2对试验性结肠紧密连接蛋白基因的mRNA相对表达量的影响 Table 3 Effects of PEG-pGLP-2 on gene expression of tight junction proteins in experimental colitis |
DSS是一种由蔗糖合成的、有抗止血和抗凝血作用的肝素样硫酸多糖体,相对分子质量5 000~1 400 000不等,为白色粉末状物,极易溶于水。DSS结肠炎模型由日本学者Ohkusa[9]于1985年首次制造成功,自此以后使用小鼠DSS结肠炎模型研究人类溃疡性结肠炎成为热点。影响DSS造模的因素主要包括DSS浓度、给药时间、DSS相对分子质量和动物种属等[10]。较为常用的方法是给小鼠饮用3%~5%的DSS溶液,症状表现包括腹泻、粪便隐血、体重下降、进食量减少、活动度减弱、毛色变差,甚至死亡等。
但DSS结肠炎模型的确切机制尚未明确,目前的研究主要认为可能与DSS增加肠道通透性、破坏肠黏膜屏障、上调某些细胞因子、激活某些通路或肠道菌群失调等有关[10]。Yan等[11]给C57BL/6小鼠饮用3.5% DSS的第1天炎性细胞因子TNF-α、白细胞介素-1β(IL-1β)、IFN-γ、IL-10和白细胞介素-12基因(IL-12)的mRNA相对表达量就显著增加,且随着DSS饮用天数的延长而其表达量不断增加,在不饮用DSS后一段时间仍能维持较高表达的水平。紧密连接是肠黏膜机械屏障的重要组成部分,主要由跨膜蛋白和胞质蛋白组成,其中跨膜蛋白包括occludin、claudin、连接黏附分子等;胞质蛋白主要为ZO家族,与紧密连接结构的其他蛋白以及细胞骨架相连。紧密连接具有物质大小和电荷选择性,是决定肠道通透性的关键因素,维持紧密连接形态和功能的完整性对保护肠黏膜屏障、防止细菌移位有着重大的意义。Mennigen等[12]证明BALB/c小鼠用3.5%的DSS处理7 d后结肠occludin、ZO-1、claudin-1和claudin-4的蛋白质水平显著下降,但对claudin-2、-3和-5没有显著影响,认为DSS结肠炎肠道上皮屏障功能的损伤与紧密连接蛋白的减少以及重新分配有关。Poritz等[13]则发现3% DSS处理1 d后小鼠结肠检测不到ZO-1蛋白,处理3 d后肠道通透性增加,处理7 d后claudin-1蛋白水平翻倍,认为DSS引起的ZO-1蛋白的快速减少增加了肠道的通透性,进而加剧了肠道的炎症反应,认为DSS结肠炎小鼠肠道紧密连接蛋白的改变不是由于炎症引起的,其发生要先于炎症反应,且紧密连接蛋白的改变加剧了结肠的炎性浸润。本试验给予20 g左右的BALB/C小鼠3% DSS自由饮用10 d建立结肠炎模型,DSS组小鼠均不同程度地出现了粪便糊肛、血便、体重下降等现象,表明造模成功;在3% DSS处理10 d后结肠ZO-1的mRNA相对表达量极显著下降,IL-6、IFN-γ和IL-10的mRNA相对表达量极显著升高。Poritz等[13]发现3% DSS诱导小鼠7 d后claudin-1基因的表达量翻倍增长,炎性因子TNF-α也能够显著诱导上皮细胞合成claudin-1[14],这表明claudin-1作为肠道黏膜屏障的组成部分,在机体处于炎症的情况下还有尚不知晓的作用。本试验发现DSS小鼠结肠occludin和claudin-1基因的mRNA表达量没有显著变化,推测DSS结肠炎肠道上皮屏障功能的损伤与紧密连接蛋白的重新分配有关。
Drucker等[15]首次报道了GLP-2具有特异性地促进肠黏膜生长与损伤后修复的作用。随后大量试验[1, 2, 3, 4]验证了该结论,且认为GLP-2的作用效果强于以往发现的其他非特异的肠生长因子,但GLP-2在体内易被降解,严重制约了其应用。在小鼠和大鼠上的试验[16, 17, 18]证明GLP-2需要每天2次持续注射6~14 d才能起到应有的肠道损伤修复作用。例如,Boushey等[16]连续6 d,每天2次注射80 μg/kg的h[Gly2]GLP-2可缓解小鼠的炎性反应。Drucker等[17]连续10 d,每天2次注射17.5 μg/kg的h[Gly2]GLP-2可缓解小鼠的肠黏膜损伤和降低炎性因子的表达。Alavi等[18]连续14 d每天静脉注射50 μg/kg GLP-2可缓解大鼠的肠黏膜损伤和降低炎性因子的表达。而这样的注射频率若应用至仔猪上,将会加剧“仔猪断奶综合征”的应激,严重阻碍了pGLP-2在仔猪肠道损伤保护中的应用。
PEG修饰是延长多肽类药物半衰期的一个有效途径。PEG是一种pH中性、无毒、水溶性较高的亲水聚合物,其重复单位为氧乙烯基,端基为2个羟基,呈线性或支链状结构。PEG与分子质量小的多肽非必需基团共价结合时,作为一种屏障,不仅保护了多肽不易被蛋白酶水解,同时阻止了抗原与抗体的结合而抑制免疫反应的发生,减少肾小球的过滤,且由于其良好的溶解性,相对分子质量范围宽等优点,均有利于延长药物在体内的半衰期[19, 20]。鉴于PEG修饰pGLP-2未见报道,本团队率先提出了开展PEG化pGLP-2的研究思路[8]。修饰位点及修饰剂的选择是PEG修饰的核心,由于pGLP-2的N端组氨酸残基对受体识别和保持生物活性十分重要[5],申请人分析了pGLP-2的氨基酸组成,设想在pGLP-2的Lys30进行的PEG修饰,并辅以对pH、PEG分子质量以及其他条件的控制,以期能够最大限度地平衡pGLP-2的生物活性与酶解稳定性,延长pGLP-2在体内的半衰期,减少注射次数。前期试验[8]已经证明一次注射Lys30-PEG-pGLP-2能够显著抑制DSS引起的结肠炎性评分和髓过氧化物酶(MPO)活性的增加。与此结果相一致,本试验发现一次注射PEG-pGLP-2可以极显著抑制DSS引起的结肠ZO-1 mRNA相对表达量的降低,且可以极显著抑制DSS引起的结肠炎性因子IL-6、IFN-γ和IL-10的mRNA相对表达量的升高。紧密连接复合体由occludin、claudin及膜周蛋白JAM和ZO蛋白以及相关激酶组成。ZO-1蛋白将occludin、claudin蛋白与细胞骨架相连,在组装成熟的紧密连接结构和维持紧密连接复合体的完整性方面发挥重要的作用。本试验发现,注射PEG-pGLP-2可增加ZO-1 mRNA相对表达量至正常饮水组的水平,而注射同剂量的pGLP-2其ZO-1 mRNA相对表达量仍与DSS组相同,表明了pGLP-2经PEG修饰后其肠道修复效果要优于pGLP-2。但pGLP-2与PEG-pGLP-2对肠道炎性因子的作用效果相同,因此推测紧密连接蛋白ZO-1表达的变化可能在pGLP-2及其长效化产物对DSS结肠炎小鼠肠道特异性的修复过程中起到重要作用。
4 结 论① BALB/C小鼠自由饮用3% DSS 10 d可成功建立结肠炎模型。
② 一次注射PEG-pGLP-2可以抑制DSS引起的结肠ZO-1 mRNA相对表达量的降低和炎性因子IL-6、IFN-γ和IL-10的mRNA相对表达量的升高。
③ 紧密连接蛋白ZO-1表达的变化可能在pGLP-2及其长效化产物对DSS结肠炎小鼠肠道特异性的修复过程中起到重要作用。
| [1] | TSAI C H,HILL M,ASA S L,et al.Intestinal growth-promoting properties of glucagon-like peptide 2 in mice[J]. American Journal of Physiology:Endocrinology and Metabolism,1997,273(1 Pt 1):E77-E84. ( 2) 2)
|
| [2] | WOJDEMANN M,WETTERGREN A,HARTMANN B,et al.Inhibition of sham feeding-stimulated human gastric acid secretion by glucagon-like peptide 2[J]. The Journal of Clinical Endocrinology & Metabolism,1999,84(7):2513-2517. ( 2) 2)
|
| [3] | BENJAMIN M A,MCKAY D M,YANG P C,et al.Glucagon-like peptide-2 enhances intestinal epithelial barrier function of both transcellular and paracellular pathways in the mouse[J]. Gut,2000,47(1):112-119. ( 2) 2)
|
| [4] | GUAN X,STOLL B,LU X,et al.GLP-2-mediated up-regulation of intestinal blood flow and glucose uptake is nitric oxide-dependent in TPN-fed piglets[J]. Gastroenterology,2003,125(1):136-147. ( 2) 2)
|
| [5] | PEDERSEN N B,HJOLLUND K R,JOHNSEN A H,et al.Porcine glucagon-like peptide-2:structure,signaling,metabolism and effects[J]. Regulotary Peptides,2008,146(1/2/3):310-320. ( 3) 3)
|
| [6] | BURRIN D G,STOLL B,GUAN X.Glucagon-like peptide 2 function in domestic animals[J]. Domestic Animal Endocrinology,2003,24(2):103-122. ( 1) 1)
|
| [7] | LEE S H,LEE S,YUS Y,et al.Synthesis,characterization,and pharmacokinetic studies of PEGylated glucagon-like peptide-1[J]. Bioconjugate Chemistry,2005,16(2):377-382. ( 1) 1)
|
| [8] | QI K K,WU J,WAN J,et al.Purified PEGylated porcine glucagon-like peptide-2 reduces the severity of colonic injury in a murine model of experimental colitis[J]. Peptide,2014,52(2):11-18. ( 4) 4)
|
| [9] | OHKUSA T.Production of experimental ulcerative colitis in hamsters by dextran sulfate sodium and changes in intestinal microflora[J]. Japanese Journal of Gastroenterology,1985,82(5):1327-1336. ( 1) 1)
|
| [10] | 温红珠,郝薇薇,李佳,等.葡聚糖硫酸钠结肠炎模型影响因素的研究进展[J]. 世界华人消化杂志,2011,19(36):3666-3671. ( 2) 2)
|
| [11] | YAN Y,KOLACHALA V,DALMASSO G,et al.Temporal and spatial analysis of clinical and molecular parameters in dextran sodium sulfate induced colitis[J]. PLoS One,2009,4(6):e6073. ( 1) 1)
|
| [12] | MENNIGEN R,NOLTE K,RIJCKEN E,et al.Probiotic mixture VSL#3 protects the epithelial barrier by maintaining tight junction protein expression and preventing apoptosis in a murine model of colitis[J]. American Journal of Physiology,2009,296(5):G1140-G1149. ( 1) 1)
|
| [13] | PORITZ L S,GARVER K I,GREEN C,et al.Loss of the tight junction protein ZO-1 in dextran sulfate sodium induced colitis[J]. Journal of Surgical Research,2007,140(1):12-19. ( 2) 2)
|
| [14] | PORITZ L S,HARRIS L R,KELLY A A,et al.Increase in the tight junction protein claudin-1 in intestinal inflammation[J]. Digestive Diseases and Sciences,2011,56(10):2802-2809. ( 1) 1)
|
| [15] | DRUCKER D J,EHRLICH P,ASA S L,et al.Induction of intestinal epithelial proliferation by glucagons-like peptide 2[J]. Proceedings of the National Academy of Sciences of the United States of America,1996,93(15):7911-7916. ( 1) 1)
|
| [16] | BOUSHEY R P,YUSTA B,DRUCKER D J.Glucagon-like peptide 2 decreases mortality and reduces the severity of indomethacin-induced murine enteritis[J]. American Journal of Physiology- Endocrinology and Metabolism,1999,277(5 Pt 1):E937-E947. ( 2) 2)
|
| [17] | DRUCKER D J,YUSTA B,BOUSHEY R P,et al.Human GLP-2 reduces the severity of colonic injury in a murine model of experimental colitis[J]. American Journal of Physiology-Gastrointestinal and Liver Physiology,1999,276(1 Pt 1):G79-G91. ( 2) 2)
|
| [18] | ALAVI K,SCHWARTZ M Z,PALAZZO J P,et al.Treatment of inflammatory bowel disease in a rodent model with the intestinal growth factor glucagon-like peptide-2[J]. Journal of Pediatric Surgery,2000,35(6):847-851. ( 2) 2)
|
| [19] | VERONESE F M,PASUT G.PEGylation,successful approach to drug delivery[J]. Drug Discovery Today,2005,10(21):1451-1458. ( 1) 1)
|
| [20] | FEE C J,VAN ALSTINE J M.PEG-proteins:reaction engineering and separation issues[J]. Chemical Engineering Science,2006,61(3):924-939. ( 1) 1)
|




