动物肠道磷的低效利用和粪尿磷排泄对环境的污染,一直是养殖业面临的一个重要问题,深入了解磷在肠道内转运和吸收机制将有助于从根本上解决这个问题。小肠作为磷吸收的重要部位,猪有超过70%的无机磷(inorganic phosphorus,Pi)在小肠部位被吸收[1],其中钠离子依赖型Ⅱb磷转运蛋白(NaPi-Ⅱb)作为小肠内主要的钠依赖型磷吸收转运蛋白[2, 3],在Pi的主动吸收过程中起到了重要作用[4],低磷饲粮水平能促进NaPi-Ⅱb表达[5]和钠依赖型磷的主动吸收[6]。因此,深入研究NaP-Ⅱb表达的调控因子,对提高肠道磷的吸收利用率、降低动物磷排泄、减少环境污染具有重要意义。降钙素基因相关肽(CGRP)属于神经肽类物质,在胃肠都有分布,同小肠壁P物质(substance P,SP)一样,有调控磷吸收的作用。猪肠道上皮细胞(porcine intestinal epithelial cells,IPEC-1)具备典型猪小肠上皮细胞特性[7],是研究肠道营养吸收机制的理想模型。本研究选用IPEC-1为试验模型,旨在探讨不同浓度CGRP对猪小肠上皮细胞磷吸收和NaPi-Ⅱb表达的影响,为进一步研究动物磷吸收机制提供理论依据。
1 材料与方法 1.1 主要试剂DMEM/F12、胎牛血清(FBS)(Hyclone公司),ITS-G(Gibco),小鼠表皮生长因子(mEGF)、CGRP(Sigma公司),4-甲基偶氮唑盐(MTT)、二甲基亚砜(DMSO)(Amresco公司),测磷试剂盒(南京建成生物工程研究所),0.25%胰蛋白酶-乙二胺四乙酸、蛋白酶抑制剂苯甲基磺酰氟(PMSF)、RIPA裂解液、ECL化学发光试剂盒(碧云天生物技术研究所),SLC34A2 antibody兔抗人多克隆抗体(Gentax公司),过氧化物酶标记的羊抗兔免疫球蛋白G(IgG)抗体[Anti-Rabbit IgG (H+L) Antibody,Peroxidase labeled,KPL公司],α-微管蛋白(α-Tubulin)(H-300,Santa Cruz Biotechnology公司),marker蛋白(Blue Plus),总RNA提取试剂盒(北京天恩泽生物技术有限公司),反转录试剂盒PrimeScriptTM RT reagent Kit with gDNA Eraser(Perfect Real Time),RT-PCR试剂盒SYBR Premix Ex TaqTM(Tli RNaseH Plus)(TaKaRa公司)。
1.2 试验细胞与试验设计试验所用IPEC-1由中国科学院亚热带农业生态研究所赠。按照常规的细胞复苏和传代方法进行细胞培养,取第3~8代生长状态良好细胞进行试验。完全培养液:DMEM/F12+5% FBS+5 ng/mL mEGF+10 ng/mL ITS-G+1%双抗,CGRP用DMEM/F12分别稀释至1×10-11~1×10-7 mmol/L。按1×104个/mL接种于96孔板中,设置1个空白对照组(DMEM/F12)和5个CGRP组,每组6个重复,用MTT法测定细胞生长速度;按1×105个/mL接种于6孔板中,每个组6个重复,提取干预培养24 h后细胞总RNA,RT-PCR法测定NaPi-Ⅱb mRNA的相对表达量;按1×105个/mL接种于6 cm皿中,细胞生长至对数期后进行药物干预,提取24 h总蛋白,蛋白质印迹(Western blot)法测定NaPi-Ⅱb蛋白的表达,试验至少重复3次以上得到稳定结果。收集药物干预后的细胞上清液,用试剂盒检测上清液中磷含量。
1.3 MTT法测生长速度用不同浓度的CGRP培养96孔板中细胞,每隔24 h取出1个96孔板,每孔加入20 μL的MTT,继续于37 ℃,5% CO2培养箱中培养4 h,取出该培养板,弃上清,用PBS清洗2次,每孔加入150 μL DMSO,室温摇晃15 min溶解蓝紫色结晶物(甲瓒),读取490 nm波长处每孔的吸光度(OD)值,测定生长曲线。
1.4 细胞上清液磷含量测定均匀收集药物干预培养后的细胞上清液,-20 ℃保存。按照生化试剂说明书(南京建成生物工程研究所),采用比色法测定细胞上清液中磷含量,计算细胞上清液磷含量变化:
磷含量(mmol/L)=[测定管吸光度(OD)-空白管吸光度]/(标准管吸光度-空白管吸光度)×标准管浓度(mmol/L)×测前稀释倍数; 磷含量变化(mmol/L)=培养基磷含量-细胞上清磷含量。 1.5 总RNA的提取及cDNA的合成按照生化试剂盒方法提取细胞总RNA(北京天恩泽生物技术有限公司,CAT#:71201-50)。取少量RNA进行纯度检测,OD260/OD280值应在1.8~2.2之间,并用1%琼脂糖凝胶对RNA进行电泳检测,观察条带数目和亮度。剩余RNA按照试剂盒操作方法(TaKaRa公司,Code No,RR047A),合成cDNA第1条链,反转录产物-20 ℃保存备用。
1.6 RT-PCR检测目的基因NaPi-Ⅱb mRNA的表达参照TaKaRa RNA PCR试剂盒说明操作,25 μL扩增体系:12.5 μL SYBR,2.0 μL cDNA,1.0 μL(10 mmol/L)上游引物,1.0 μL(10 mmol/L)下游引物,8.5 μL dH2O;扩增条件:95 ℃ 30 s,95 ℃ 5 s,58 ℃ 30 s,72 ℃ 1 min(39个循环)。根据已知猪的NaPi-Ⅱb全长cDNA序列[8]设计猪NaPi-Ⅱb RT-PCR引物,内参基因β-肌动蛋白(β-actin)引物参考已知猪(Sus scrofa)的β-actin CDA(U07786)序列设计,使用Primer 5.0进行引物设计,引物合成由上海生物工程公司完成。NaPi-Ⅱb的引物序列: 上游,5’-CAGCCCGAAACAAGAGTATGAT-3’;下游,5’-TACAAACCATCCGTCCAACAG-3’;β-actin的引物序列:上游,5’-CTTCCTGGGCATGGAGTCCT-3’;下游,5’-CGTGTTGGCGTAGAGGTCCTT-3’。
1.7 蛋白样品的制备取出培养皿,先用预冷PBS清洗培养皿3次后,加入临时配制的RIPA(含1% PMSF)裂解液冰上裂解细胞20 min,然后用胞刮刀收集裂解的细胞碎片,转移至1.5 mL离心管,4 ℃ 12 000 r/min离心10 min,取上清,即为细胞总蛋白。取少量样品用Bradford法进行蛋白定量,测定蛋白样品浓度,将所有样品调至等浓度,和上样缓冲液混合均匀,100 ℃变性5 min,冷却后-20 ℃度保存,检测时解冻直接使用。
1.8 Western blot法检测目的蛋白用10%十二烷基硫酸钠-聚丙烯酰胺凝胶(SDS-PAGE)进行电泳,上层80 V,下层120 V,至溴酚蓝到达凝胶底部终止。室温恒流转膜90 min,将蛋白转移至PVDF膜上,随后用5%脱脂奶粉(1×TBST缓冲液稀释)37 ℃封闭蛋白膜1 h,然后与一抗兔抗人多克隆抗体(SLC34A2抗体,1 ∶ 200)4 ℃过夜孵育。经1×TBST缓冲液清洗3次,用碱性磷酸酶标记的羊抗兔IgG抗体[Anti-Rabbit IgG (H+L) Antibody,1 ∶ 1 000]室温孵育2 h,再清洗3次后加入ECL化学发光试剂,用化学发光检测仪(Image Quant LAS 4000 mini)对膜进行显影检测,同一样本用α-Tubulin(Santa公司,1 ∶ 1 000)作为内参。结果用Image J凝胶分析软件进行OD值分析。每个结果至少经过3次重复试验得到。
1.9 数据统计分析采用2-△△CT法计算mRNA相对表达量。用SPSS 19.0统计软件进行ANOVA单因素方差分析,Duncan氏法多重比较,试验数据用平均值±标准差表示,P<0.05为差异显著,P<0.01为差异极显著。
2 结果与分析 2.1 细胞形态学观察细胞复苏后,传代1~2次后细胞生长稳定,显 微镜下观察细胞贴壁生长,形态完整,细胞呈单层,呈多角形或卵石圆形,铺路石状分布。图1为用于干预试验对数生长期细胞,细胞铺满瓶底80%,边界清晰,没有重叠,生长良好。
 | 图1 猪小肠上皮细胞 Fig. 1 Porcine intestinal epithelial cells (100×) |
细胞接种后呈悬浮状态,4 h之后细胞基本贴壁,开始缓慢生长,细胞生长需经过潜伏期—指数增长期—停滞期,选取24~96 h细胞观察细胞的增殖情况,各CGRP浓度处理细胞生长趋势见表1。和对照组相比,添加不同浓度CGRP(1×10-7~1×10-11 mmol/L)后,在24~96 h内各时间点的吸光度值均没有显著差异(P>0.05),24~96 h内各时间点平均值分别为0.092±0.003、0.103±0.009、0.108±0.009、0.125±0.009,表明CGRP对猪小肠上皮细胞的生长没有显著影响。
| 表1 不同浓度CGRP对细胞生长趋势的影响(以MTT吸光度值表示) Table 1 Effects of different CGRP concentrations on cell growth tendency (expressed as MTT OD value) |
由表2可知,添加CGRP 24 h后细胞上清液中磷含量都极显著低于对照组(P<0.01),其中1×10-10 mmol/L组与1×10-9、1×10-11 mmol/L组间 差异显著(P<0.05),其他各组间差异极显著 (P<0.01)。CGRP浓度与磷含量变化呈极显著的二次曲线关系(P<0.01),其中y=-0.018+0.178m-0.023m2,R2=0.739,式中m=13+lgx,x为CGRP浓度(mmol/L);y为磷含量变化(mmol/L)。
| 表2 不同浓度CGRP对细胞上清中磷含量的影响 Table 2 Effects of different CGRP concentrations on phosphorus content in the cell supernatant mmol/L |
对CGRP干预24 h后细胞总RNA进行浓度测定,结果显示RNA OD值在1.9~2.1之间,1%琼脂糖凝胶电泳结果也显示28S和18S出现明显亮带(图2),说明RNA完整性好,纯度高,含量充足,可用于后续试验。
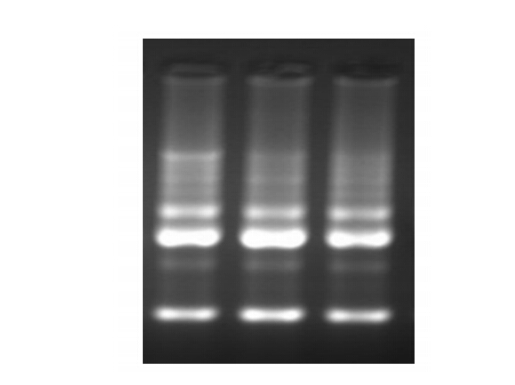 | 图2 猪小肠上皮细胞总RNA完整性检测 Fig. 2 Integrity testing of total RNA in |
不同浓度CGRP干预细胞24 h后,将小肠上皮细胞中NaPi-Ⅱb mRNA相对表达量和对应样品的β-actin表达量进行均一化处理,如图3所示,对照组(用A表示)及CGRP组(1×10-11~1×10-7 mmol/L,分别用B~F表示)NaPi-Ⅱb mRNA的相对表达量分别为1.005±0.080、1.662±0.177、1.628±0.212、2.200±0.190、1.959±0.196、1.628±0.185。和对照组相比,1×10-11~1×10-7 mmol/L CGRP组NaPi-Ⅱb mRNA相对表达量分别提高了65.48%、62.03%、119.00%、 95.05%、62.00%,差异极显著(P<0.01);1×10-9、1×10-8 mmol/L组和1×10-11、1×10-10、1×10-7 mmol/L组间差异极显著(P<0.01);其中1×10-9 mmol/L组促进作用最强,1×10-8 mmol/L组次之。
 | 图3 不同浓度CGRP对NaPi-Ⅱb mRNA表达的影响 Fig. 3 Effects of different CGRP concentrations on |
根据牛血清白蛋白(BSA)浓度(x,μg/μL)和OD值(y)得到标准曲线:y=1.656x+0.673,R2=0.987。计算出蛋白样品的浓度在3~5 μg/μL,总蛋白含量充足。不同浓度CGRP干预24 h后对小肠上皮细胞NaPi-Ⅱb蛋白表达的影响结果见图4,从左至右分别为对照组、1×10-11、1×10-10、1×10-9、1×10-8、1×10-7 mmol/L组(分别用 A~F表示)。和对照组相比,不同浓度CGRP组(除1×10-10 mmol/L组外)小肠上皮细胞中NaPi-Ⅱb蛋白相对表达量分别增加了10.36%、70.48%、80.29%、28.10%,由图4可知,1×10-11、1×10-9、1×10-8、1×10-7 mmol/L组CGRP均显著促进了NaPi-Ⅱb蛋白表达(P<0.05),且这4组之间均差异显著(P<0.05),其中1×10-8 mmol/L组促进作用最强,1×10-9 mmol/L组次之。
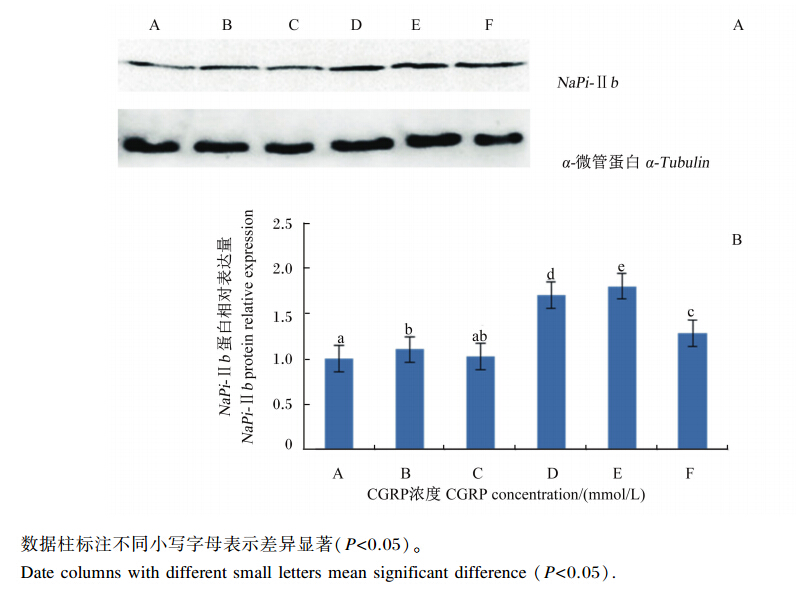 | 图4 CGRP干预对NaPi-Ⅱb蛋白表达的影响 Fig. 4 Effects of CGRP interfering on expression of NaPi-Ⅱb protein (n=3) |
细胞的体外培养作为一种研究动物磷吸收转运的有效方法,可以较好地模拟体内的生理环境,研究单因素对磷吸收的影响,更直观地观测细胞活动与药物干预的关系,大量研究者通过细胞的体外培养,研究了单因素对细胞增殖凋亡、生理功能及作用机理等的影响[9, 10, 11]。细胞的体外培养已广泛用于众多生命科学领域的研究,但是人工培养环境和体内复杂的生物环境差别较大,还需要结合体内试验进行验证。细胞的生长形态和生长趋势作为鉴定细胞生长状态的重要指标,可以反映药物对细胞的生长分化以及细胞活力的影响。光学显微镜下观察细胞形态是常用的鉴定细胞生长状态的方法[12],MTT法是一种常用的测定细胞存活和生长的方法,采用MTT法测定细胞增殖[13],主要是通过检测活细胞数量和新陈代谢程度,用以检测药物对细胞活力和生长是否有影响。试验结果显示,CGRP对小肠上皮细胞增殖无显著影响,可说明试验中细胞上清液磷含量的变化并非由细胞活力和数量改变而导致。
3.2 CGRP对磷吸收的影响磷的吸收主要发生在小肠,分为主动吸收和被动扩散2种形式。在低磷情况下,磷的吸收主要是依靠Na-Pi协同转运蛋白NaPi-Ⅱb完成,而NaPi-Ⅱb在小肠上皮细胞中的表达受到多种因素的影响。肠道的活动和分泌受到外界各种因素的共同调节,是一个由中枢神经、肠神经和自主神经共同支配的系统。CGRP为辣椒素敏感神经末梢释放的含37个氨基酸的神经肽[14],是目前已知的作用最强的舒血管物质,它广泛分布于中枢、外周神经系统及多种器官组织中[15],有舒张血管和收缩心肌[16],抑制血管平滑肌细胞增殖[17]和凋亡,参与调解神经和胃肠保护[18],调节细胞内的钙离子(Ca2+)浓度[19],参与骨折的愈合[20]等功能,同SP、血管活性肠肽(VIP)等一样属于胃肠肽类,这些介质相互影响,共同发挥作用,在调节肠道感觉、运动和内分泌等功能方面发挥了重要作用[21]。CGRP主要通过受体发挥其生物学作用[22, 23],而其受体广泛分布在哺乳动物的食管下括约肌、胃肠平滑肌、阑尾的纵行肌、肛门内括约肌以及整个消化道的黏膜层[24],这可能是CGRP能在小肠内调控磷吸收因素之一。然而对CGRP与小肠磷吸收方面的研究尚未见报道。本研究中,DMEM/F12培养液中磷来源有2种:无水磷酸二氢钠54.35 mg/mL与磷酸氢二钠71.02 mg/mL,实测磷含量为0.90 mmol/L,根据实测结果计算不同浓度CGRP培养前后细胞上清液中磷含量的变化,从细胞整体水平来反映磷的吸收情况,结果显示各试验浓度CGRP均极显著促进了磷的吸收,其中1×10-8 mmol/L组对磷吸收的促进作用最为显著,1×10-9 mmol/L组次之。
3.3 CGRP对NaPi-Ⅱb mRNA和蛋白表达的影响NaPi-Ⅱb作为小肠内主要的钠依赖型磷吸收转运蛋白,负责细胞内Pi的积累和维持细胞内外磷平衡[25],其表达受到多种因素的影响,包括日龄[26]、饲粮磷水平[27]、肠段[28]、雌二醇[29]、糖皮质激素[30]、1α羟基维生素D3(1α-OHD3)[31]、表皮生长因子(EGF)[32]、成纤维细胞生长因子23(FGF-23)[33]、甲状旁腺素(PTH)[34]、神经肽类[35]等。Xu等[29]在研究雌激素对NaPi-Ⅱb表达的影响中,用RT-PCR技术检测发现雌激素极显著促进了Caco-2中NaPi-Ⅱb mRNA表达,提高了基因启动子的活性,Western blot法检测结果显示,雌激素增加了小鼠小肠中NaPi-Ⅱb蛋白的表达,促进了磷在小肠的吸收,说明雌激素是通过诱导NaPi-Ⅱb协同转运蛋白基因的表达来促进小肠Pi吸收的。本研究中,以猪小肠上皮细胞为试验模型,检测了CGRP对NaPi-Ⅱb mRNA及蛋白表达的影响,结果表明,各浓度CGRP均极显著促进了NaPi-Ⅱb mRNA的表达,其中1×10-9 mmol/L组促进作用最强,1×10-8 mmol/L组次之;对NaPi-Ⅱb蛋白表达的影响以1×10-8 mmol/L组最显著,1×10-9 mmol/L组次之,且两者之间差异显著。早先的研究认为,蛋白的表达量、转录水平及转运活性一般呈线性对应关系,但是在Saddoris[36]研究发现,低磷饲粮提高了钠依赖性磷转运活性,NaPi-Ⅱb蛋白表达量增加了82%,而NaPi-Ⅱb转录活性并未出现相应的增加,由此认为,低磷饲粮引起的钠依赖性磷转运是一种转录后调控机制。Muscher[37]研究亦发现,低磷饲粮对山羊乳腺上皮细胞中NaPi-Ⅱb mRNA和蛋白表达的影响不一致。本试验中,经1×10-9 mmol/L CGRP处理后蛋白表达量对磷吸收的作用更为显著,1×10-8 mmol/L组CGRP对磷吸收和NaPi-Ⅱb蛋白表达的促进作用均高于1×10-9 mmol/L组,对NaPi-Ⅱb mRNA相对表达的促进作用则低于1×10-9 mmol/L组,可见CGRP对磷吸收的调控作用发生在转录后阶段的可能性更大。从整体来看,CGRP能通过诱导猪小肠上皮细胞中NaPi-Ⅱb的表达,促进细胞外液磷跨膜转运进入细胞内液,以1×10-8 mmol/L组的CGRP作用最为显著,说明在猪小肠上皮细胞中的跨膜运载机制中,CGRP在一定浓度范围内能促进NaPi-Ⅱb表达,进而调节钠依赖型磷的吸收。
4 结 论① 1×10-11~1×10-7 mmol/L CGRP对猪小肠上皮细胞生长没有显著影响。
② 1×10-11~1×10-7 mmol/L CGRP均极显著或显著促进了细胞对磷的吸收。
③ CGRP通过诱导NaPi-Ⅱb的表达促进了细胞对磷的吸收,以CGRP浓度为1×10-9、1×10-8 mmol/L效果较为显著。
| [1] | ALIMENTI R,ANTONUCCI G,BERNARDINI M P,et al.Nutritional research on toprina (yeasts cultivated on n-paraffins)[J]. Annali dell'Istituto Superior di Sanita,1979,15(3):649-689. ( 1) 1)
|
| [2] | 曹满湖,方热军,陈清华,等.NaPi-Ⅱ型协同转运蛋白与磷吸收的关系[J]. 兽药与饲料添加剂,2008,13(6):22-24. ( 1) 1)
|
| [3] | FORSTER I C,HERNANDO N,BIBER J,et al.Phosphate transport kinetics and structure-function relationships of SLC34 and SLC20 proteins[J]. Current Topics in Membranes,2012,70:313-356. ( 1) 1)
|
| [4] | REINING S C,LIESEGANG A,BETZ J,et al.Expression of renal and intestinal Na/Pi cotransporters in the absence of GABARAP[J]. Pflugers Arch:European Journal of Physiol,2010,460(1):207-217. ( 1) 1)
|
| [5] | SABBAGH Y,O'BRIEN P S,SONG W,et al.Intestinal Npt2b plays a major role in phosphate absorption and homeostasis[J]. Journal of the American Society of Nephrology,2009,20(11):2348-2358. ( 1) 1)
|
| [6] | 方热军,贺佳,曹满湖.日粮磷水平对肉鸡磷代谢及Na/Pi-Ⅱb基因mRNA表达的影响[J]. 畜牧兽医学报,2011,42(2):289-296. ( 1) 1)
|
| [7] | SCHIERACK P,NORDHOFF M,POLLMANN M,et al.Characterization of a porcine intestinal epithelial cell line for in vitro studies of microbial pathogenesis in swine[J]. Histochemistry and Cell Biology,2006,125(3):293-305. ( 1) 1)
|
| [8] | ZHIFENG X,FANG R J,HU L C,et al.Molecular cloning and functional characterization of swine sodium dependent phosphate cotransporter type Ⅱb (NaPi-Ⅱb) gene[J]. Molecular Biology Reports,2012,39(12):10557-10564. ( 1) 1)
|
| [9] | JIN C L,ZOIDIS E,GHIRLANDA C,et al.Dexamethasone and cyclic AMP regulate sodium phosphate cotransporter (NaPi-Ⅱb and Pit-Ⅰ) mRNA and phosphate uptake in rat alveolar type Ⅱ epithelial cells[J]. Lung,2010,188(1):51-61. ( 1) 1)
|
| [10] | WONG S H,GAO A,WARD S,et al.Development of a label-free assay for sodium-dependent phosphate transporter NaPi-Ⅱb[J]. Journal of Biomolecular Screening,2012,17(6):829-834. ( 1) 1)
|
| [11] | 陈俊才.不同锌源的吸收及其对小肠上皮细胞IEC-6凋亡影响的研究[D]. 硕士学位论文.雅安:四川农业大学,2012. ( 1) 1)
|
| [12] | 王静,张彦明,周宏超,等.猪小肠黏膜上皮细胞原代培养[J]. 动物医学进展,2009,30(8):46-49. ( 1) 1)
|
| [13] | 职爱民,左建军,黄志毅,等.猪小肠黏膜上皮细胞的分离及体外原代培养模型的建立[J]. 饲料工业,2010,31(1):10-13. ( 1) 1)
|
| [14] | MA H B.Calcitonin gene-related peptide(CGRP)[J]. Nature and Sciernce,2004,2(3):41-47. ( 1) 1)
|
| [15] | WISSKIRCHEN F M,GRAY D W,Marshall I.Receptors mediating CGRP-induced relaxation in the rat isolated thoracic aorta and porcine isolated coronary artery differentiated by h(alpha)CGRP(8-37)[J]. British Journal of Pharmacology,1999,128(2):283-292. ( 1) 1)
|
| [16] | LI D,LI N S,CHEN Q Q,et al.Calcitonin gene-related peptide-mediated cardioprotection of postconditioning in isolated rat hearts[J]. RegulPept,2008,147(1/2/3):4-8. ( 1) 1)
|
| [17] | CHATTERGOON N N,D'SOUZA F M,DENG W,et al.Antiproliferative effects of calcitonin gene-related peptide in aortic and pulmonary artery smooth muscle cells[J]. American Journal of Physiology:Lung Cellular and Molecular Physiology,2005,288(1):L202-L211. ( 1) 1)
|
| [18] | EVANGELISTA S.Role of calcitonin gene-related peptide in gastric mucosal defence and healing[J]. Current Pharmaceutical Design,2009,15(30):3571-3576. ( 1) 1)
|
| [19] | LI Y,TAN Y H,ZHANG G,et al.Effects of calcitonin gene-related peptide on the expression and activity of nitric oxide synthase during mandibular bone healing in rabbits:an experimental study[J]. Journal of Oral and Maxillofacial Surgery,2009,67(2):273-279. ( 1) 1)
|
| [20] | LERNER U H.Deletions of genes encoding calcitonin/alpha-CGRP,amylin and calcitonin receptor have given new and unexpected insights into the function of calcitonin receptors and calcitonin receptor-like receptors in bone[J]. Journal of Musculoskeletal & Neuronal Interactions,2006,6(1):87-95. ( 1) 1)
|
| [21] | YU L C,HOIU J F,FU F H,et al.Roles of calcitonin gene-related peptide and its receptors in pain-related behavioral responses in the central nervous system[J]. Neuroscience & Biobehavioral Reviews,2009,33(8):1185-1191. ( 1) 1)
|
| [22] | 徐琳,谭颖徽.受体活性修饰蛋白的研究进展[J]. 国外医学:生理、病理科学与临床分册,2005,25(1):18-20. ( 1) 1)
|
| [23] | 秦旭平,李元建.降钙素基因相关肽受体重构及其信号跨膜转导[J]. 中南医学科学杂志,2011,39(2):121-126. ( 1) 1)
|
| [24] | 冯国营,刘桂香.降钙素基因相关肽对胃肠作用的相关研究进展[J]. 滨州医学院学报,2008,31(4):291-294. ( 1) 1)
|
| [25] | WANG B,YIN Y L.Regulation of the type Ⅱb sodium-dependent phosphate cotransporter expression in the intestine[J]. Front Agriculture China,2009,3(2):226-230. ( 1) 1)
|
| [26] | XU H,BAI L,GHISHAN F K,et al.Age-dependent regulation of rat intestinal type Ⅱb sodium-phosphate cotransporter by 1,25-(OH)2 vitamin D3[J]. American Journal of Physiology:Cell Physiology,2002,282(3):C487-C493. ( 1) 1)
|
| [27] | 周晓.日粮磷水平对肉仔鸡小肠磷吸收的影响及机理[D]. 硕士学位论文.北京:中国农业科学院,2012:26-27. ( 1) 1)
|
| [28] | 孙杰.大白猪和五指山猪小肠钠依赖型磷转运吸收的比较研究[D]. 硕士学位论文.淄博:山东理工大学,2007:21. ( 1) 1)
|
| [29] | XU H,UNO J K,INOUYE M,et al.Regulation of intestinal NaPi-Ⅱb cotransporter gene expression by estrogen[J]. American Journal of Physiology:Gastroimestinal and Liver Physiology,2003,285(6):G1317-G1324. ( 1) 1)
|
| [30] | 项智峰.猪小肠NaPi-Ⅱb基因克隆和表达调控研究[D]. 博士学位论文.长沙:湖南农业大学,2013:67-68. ( 1) 1)
|
| [31] | 韩进城.1α-OHD3和植酸酶对肉鸡磷代谢的影响及肠道NaPi-Ⅱb基因表达调控[D]. 博士学位论文.杨凌:西北农林科技大学,2008:80-82. ( 1) 1)
|
| [32] | XU H,INOUYE M,HINES E R,et al.Transcriptional regulation of the human NaPi-Ⅱb cotransporter by EGF in Caco-2 cells involves c-myb[J]. American Journal of Physiology:Cell Physiology,2003,284(5):C1262-C1271. ( 1) 1)
|
| [33] | 郭晓强.成纤维细胞生长因子23和血鳞代谢[J]. 生命的化学,2007,27(2):149-151. ( 1) 1)
|
| [34] | FORSTER I C,TRAEBERT M,JANKOWSKI M,et al.Protein kinase C activators induce membrane retrieval of type Ⅱ Na+-phosphate cotransporters expressed in Xenopus oocytes[J]. The Journal of Physiology,1999,517(Pt2):327-340. ( 1) 1)
|
| [35] | MAY C A,FUCHS A V,MICHAEL S,et al.Characterization of nitrergic neurons in the porcine and human ciliary nerves[J]. Investigative Ophthalmology & Visual Science,2002,43(3):581-586. ( 1) 1)
|
| [36] | SADDORIS K L.Dietary factors affecting sodium-dependent phosphate uptake and gene expression of the NaPi-Ⅱb in the small intestine of weanling pigs[D]. Ph.D.Thesis.West Lafayette:Purdue University,2007. ( 1) 1)
|
| [37] | MUSCHER A,BREVES G,HUBER K.Modulation of apical Na+/Pi cotransporter type Ⅱb expression in epithelial cells of goat mammary glands[J]. Journal of Animal Physiology and Animal Nutrition,2009,93(4):477-485. ( 1) 1)
|




