在现代畜牧生产过程中,高密度、集约化生产带来的各种应激因素越来越受到人们的重视,其中高温带来的热应激是一种常见的危害畜牧业的不利因素。通过营养调控手段,缓解热应激对动物造成的负面影响,已受到越来越多的学者关注。
小鼠在急性热应激后,会出现急躁不安,心率加快,体表和直肠温度升高,身体水分蒸发加剧,进而导致脱水,血清渗透压升高,体重减少[1, 2, 3]。姜忠玲[4]利用化学恒温培养箱对小鼠实施持续42 ℃全身热应激,发现热应激后小鼠体重减轻,体表温度和直肠温度显著升高,睾丸和附睾组织丙二醛(MDA)含量以及活性氧自由基(ROS)、超氧化物歧化酶(SOD)和谷胱甘肽过氧化物酶(GSH-Px)活力升高。Kim等[5]研究发现,热应激后大鼠肝脏中脂肪酸合酶和氧化还原类酶活力以及脂质过氧化物相关的基因转录水平显著升高,MDA含量显著升高。本实验室研究发现,体表温度和直肠温度在热处理后都极显著高于热处理前;组织形态学观察发现,热处理导致小鼠肝脏组织充血和肝细胞水肿;小鼠肝脏MDA含量在热处理2 d较对照组显著升高,还原型谷胱甘肽(GSH)含量、GSH-Px活力和T-SOD活力在热处理4和12 d都有升高[6]。上述研究结果表明,小鼠热处理后,肝脏中产生了显著的氧化应激。
氧化应激是指机体在遭受各种有害刺激时,体内高活性分子如ROS和活性氮自由基产生过多,氧化速度超出氧化物的清除速度,氧化系统和抗氧化系统失衡,从而导致组织损伤。过多的自由基会攻击蛋白质、脂肪酸、磷脂和核酸等生物大分子,改变其生物学功能,使机体的正常代谢发生紊乱[7],如蛋白质肽链主链的氧化,肽键的断裂和侧链的氧化[8]。Kelch样ECH相关蛋白(Keap1)-转录因子E2相关因子2(Nrf2)/ARE信号通路被认为是抗氧化应答机制中最重要的一条信号通路[9, 10, 11]。Keap1-Nrf2/ARE信号通路在机体受到氧化应激时,调节体内的抗氧化酶基因表达,保护机体抵抗自由基的攻击,减少氧化损伤,对机体维持内环境的稳定具有重要作用。
叔丁基对苯二酚(tert-butylhydroquinone,tBHQ)是抗氧化蛋白强诱导剂,主要通过促进Nrf2蛋白入核,激活抗氧化蛋白基因的表达[12],从而发挥抗氧化作用。Nrf2下游靶基因主要包括辅酶Q氧化还原酶1(NQO1)、谷胱甘肽S-转移酶、葡糖醛酸基转移酶、血红素加氧酶1(HO-1)等[13, 14, 15]。近年研究表明,饲粮饲喂tBHQ可以提高大鼠肾脏组织抗氧化酶类基因表达,从而抑制顺铂诱导的肾毒性[16]。另外,饲粮添加tBHQ还可通过提高小鼠多巴胺能细胞内相关抗氧化保护蛋白的表达,从而抑制百草枯诱导的多巴胺能细胞退化[17]。本试验旨在饲喂 小鼠添加1% tBHQ的饲粮14 d,研究其是否可通过调控Keap1-Nrf2/ARE信号通路,增加动物机体的抗氧化水平,进而增强动物对热应激的抵抗能力。
1 材料与方法 1.1 材料tBHQ,购自Sinopharm ChemicalReagent公司,纯度为99%。总超氧化物歧化酶(T-SOD)、GSH、GSH-Px、过氧化氢酶(CAT)、MDA、铜,锌超氧化物歧化酶(Cu,Zn-SOD)测定试剂盒和苏木素-伊红(HE)染液均购自南京建成生物工程研究所;TaKaRa PrimeScript RT reagent Kit反转录试剂盒和TaKaRa SYBR Premix Ex TaqTM定量试剂盒为日本TaKaRa公司产品;小鼠Nrf2特异性抗体购自美国Santa Cruz公司;小鼠HO-1特异性抗体购自武汉博士德生物工程有限公司;免疫组织化学ABC染色试剂盒购自武汉博士德生物工程有限公司。
1.2 方法 1.2.1 试验设计50只6周龄雄性ICR小鼠[(35±1) g]随机分为2组,每组25只,tBHQ(-)组饲喂基础饲粮,tBHQ(+)组饲喂基础饲粮添加1% tBHQ的试验饲粮。1%的tBHQ添加量参考Li等[18]和Shih等[19]的研究结果设定。小鼠饲养在人工控制的环境中,12 h光照(07:00—19:00)和12 h黑暗,温度(23±2) ℃,湿度(50±10)%,每笼5只混合饲养,自由采食和饮水,按照南京农业大学试验动物常规饲养操作规程进行饲养。饲喂14 d后,小鼠进行连续8 d热应激处理,每天在相同时间(11:00—13:00)将小鼠置于恒温生化培养箱(温度42 ℃,相对湿度60%)中2 h。在热应激的8 d里,小鼠饲粮维持不变。
1.2.2 样品收集在热应激前(热应激0 d)和热应激1、2、4、8 d,每组随机取5只小鼠在热应激后马上进行颈椎脱臼处死,解剖小鼠,采集肝脏样品。
1.2.3 测定指标和方法 1.2.3.1 肝脏指数试验结束时,先称量小鼠活体重,小鼠颈椎脱臼处死后无菌摘取肝脏,用滤纸吸去血液,用眼科剪剪去脂肪和系膜后称重,计算肝脏指数。
肝脏指数(g/kg)=肝脏重量(g)/体重(kg)。 1.2.3.2 肝脏抗氧化指标称取肝脏组织0.10~0.15 g,按质量体积比加入9倍的生理盐水,用组织匀浆机10 000~15 000 r/min充分研磨,然后3 800 r/min离心15 min,吸取上清液备用。采用试剂盒测定MDA、GSH的含量和GSH-Px、T-SOD、Cu,Zn-SOD、CAT的活力。
1.2.3.3 肝脏组织形态取3 cm长的肝脏组织样,经4%多聚甲醛固定24 h后,梯度酒精脱水,二甲苯透明,石蜡包埋处理,切片,进行HE染色。
1.2.3.4 肝脏组织Nrf2和HO-1蛋白的定位采用免疫组织化学方法,切片经二甲苯脱蜡后,在过氧化氢(H2O2)中浸泡以灭活内源性过氧化物酶的活力;柠檬酸三钠缓冲液97 ℃水浴热修复。山羊血清封闭1 h后滴加Nrf2或HO-1多克隆抗体(1 ∶ 100),37 ℃孵育1 h。磷酸盐缓冲液(PBS)清洗后加入羊抗兔生物素标记二抗,37 ℃孵育1 h,PBS清洗后加入链霉亲和素-生物素复合物(SABC),37 ℃孵育30 min,二氨基联苯胺(DAB)显色5 min左右,苏木素复染1 min,中性树胶封片。对照切片以PBS代替一抗,其余步骤相同。
1.2.3.5 肝脏Nrf2及其调控基因表达量按照Trizol说明书提取肝脏组织的总RNA,提取的总RNA保存于-70 ℃超低温冰箱中,或立即用于反转录。反转录按照TaKaRa Prime Script RT reagent Kit反转录试剂盒说明书进行。利用2-△△Ct法对基因表达进行相对定量。实时定量PCR引物序列及参数见表1。
| 表1 实时定量PCR引物序列及参数
Table 1 Sequences and parameters of primers for real-time PCR
|
采用Excel对试验数据进行统计和整理,各组数据均采用平均值±标准误表示,采用GraphPad Prism 5对数据进行单因素方差分析(ANOVA),t检验法进行差异性比较,P<0.05为差异显著。
2 结 果 2.1 tBHQ对热应激小鼠体重和肝脏指数的影响由表2可知,在tBHQ(-)组,小鼠在热应激8 d体重显著低于热应激1和2 d(P<0.05);而在tBHQ(+)组,与热应激0 d相比,除了热应激4 d体重显著降低(P<0.05)外,其他时间点均无显著变化(P>0.05)。在tBHQ(-)组,与热应激0 d相比,热应激1和2 d的肝脏指数显著提高(P<0.05);但在tBHQ(+)组,小鼠的肝脏指数在热应激1 d显著高于热应激2、4和8 d(P<0.05)。
与tBHQ(-)组相比,tBHQ(+)组小鼠体重在各时间点均显著下降(P<0.05),肝脏指数只在热应激2 d显著下降(P<0.05)。
| 表2 tBHQ对热应激小鼠体重和肝脏指数的影响 Table 2 Effects of tBHQ on body weight and liver index of heat stressed mice (n=5) |
由表3可知,与热应激0 d相比,tBHQ(-)组热应激2和8 d,肝脏MDA含量显著增加(P<0.05),其他抗氧化指标均随热应激时间的延长先增高后降低;tBHQ(+)组MDA含量稳定维持在较低水平,其他抗氧化指标均随热应激时间的延长先降低后增高。与tBHQ(-)组相比:热应激0 d,tBHQ(+)组肝脏T-SOD活力显著升高(P<0.05);热应激1 d,tBHQ(+)组小鼠的肝脏MDA含量显著升高(P<0.05);热应激2 d,tBHQ(+)组小鼠的肝脏中MDA含量、Cu,Zn-SOD活力和CAT活力显著降低(P<0.05);热应激4 d,tBHQ(+)组GSH含量以及T-SOD、Cu,Zn-SOD、GSH-Px和CAT活力显著降低(P<0.05);热应激8 d,tBHQ(+)组MDA含量和CAT活力显著降低(P<0.05)。
| 表3 tBHQ对热应激小鼠肝脏抗氧化指标的影响 Table 3 Effects of tBHQ on antioxidant indices in liver of heat stressed mice (n=5) |
由图1可知,热应激0 d,tBHQ(-)组(图1-A)和tBHQ(+)组(图1-B)小鼠的肝脏组织细胞排列紧密,结构完整;而在热应激2 d,肝脏组织间裂纹增多,排列疏松,红细胞进入组织之间,组织间能看到多个红细胞分布,肝细胞水肿变大,tBHQ(-)组(图1-C)比tBHQ(+)组(图1-D)损伤情况更为严重。
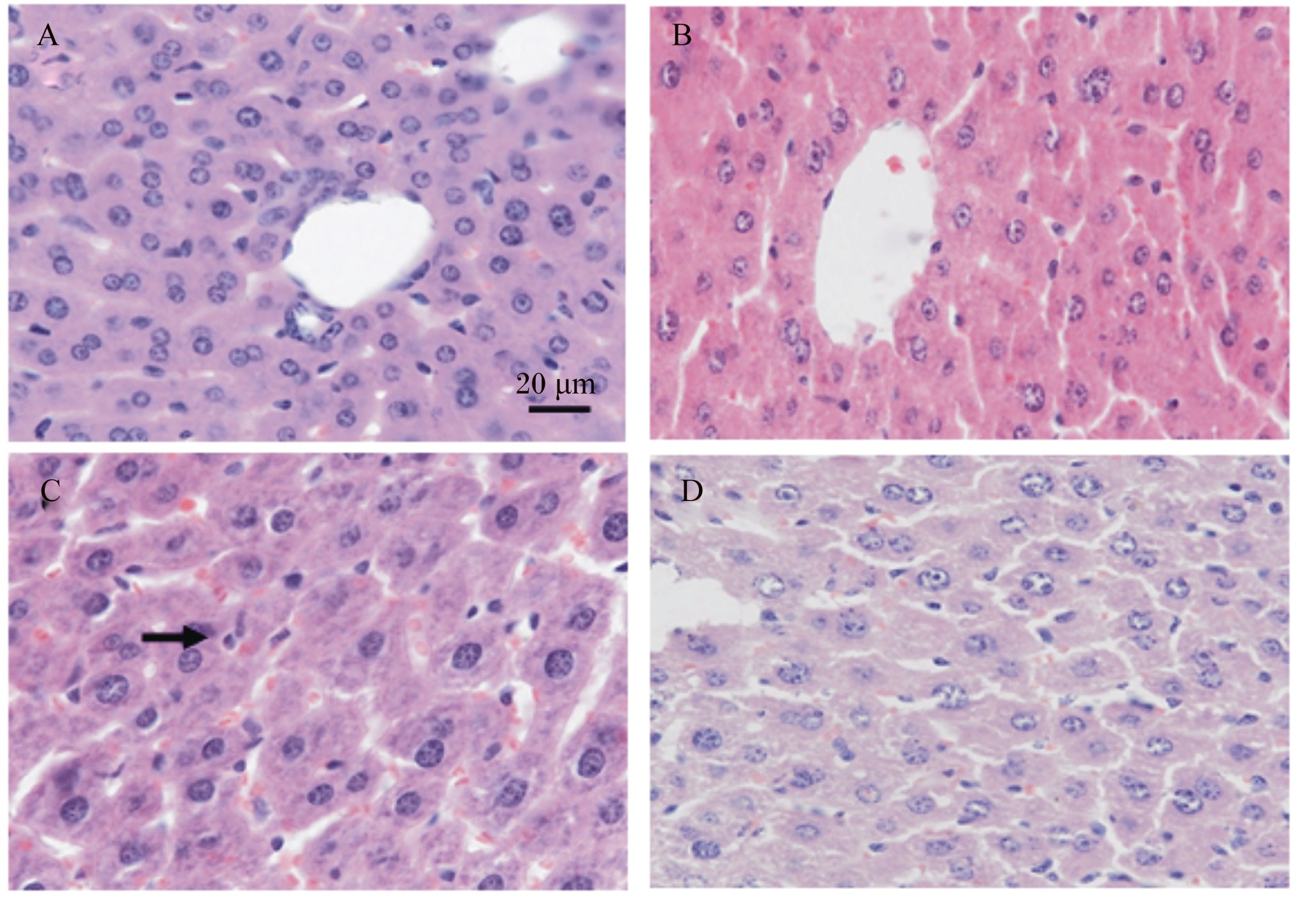 | A、C:tBHQ(-)组,分别为热应激0、2 d;B、D:tBHQ(+)组,分别为热应激0、2 d。→:红细胞。
A and C: tBHQ(-) group, under heat stress for 0 and 2 days, respectively; B and D: tBHQ(+) group, under heat stress for 0 and 2 days, respectively. →: red blood cell.
图1 热应激0和2 d小鼠肝脏组织HE染色
Fig. 1 HE stain of liver tissue of mice after 0 and 2 days of heat stress |
由图2可知,tBHQ(-)组在热应激0 d(图2-A)未检测到Nrf2蛋白在肝脏组织表达,而热应激1(图2-C)、2(图2-E)、4(图2-G)和8 d(图2-I)时都检测到Nrf2蛋白在肝细胞细胞质中的表达;而tBHQ(+)组在热应激前后都发现肝细胞细胞质中Nrf2蛋白的表达(图2-B、图2-D、图2-F、图2-H、图2-I)。
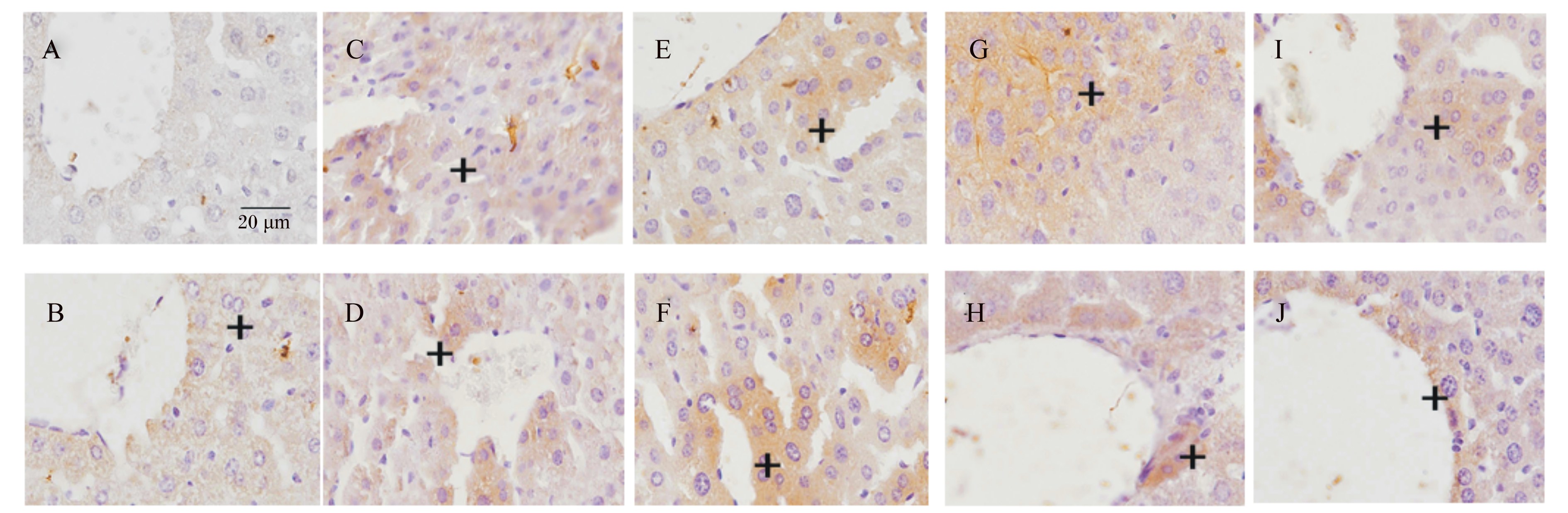 | A、C、E、G、I:tBHQ(-)组,分别为热应激0、1、2、4、8 d;B、D、F、H、J:tBHQ(+)组,分别为热应激0、1、2、4、8 d。+:阳性表达。下图同。
图2 tBHQ对热应激小鼠肝脏组织Nrf2蛋白表达的影响
Fig. 2 Effects of tBHQ on Nrf2 protein expression in liver of heat stressed mice |
由图3可知,tBHQ(-)组在热应激0(图3-A)、1(图3-C)、4(图3-G)和8 d(图3-I)都检测到HO-1蛋白在肝细胞细胞质中的表达;而tBHQ(+)组小鼠在热应激0(图3-B)、1(图3-D)和2 d(图3-F)发现了HO-1蛋白在肝细胞细胞质中的表达。
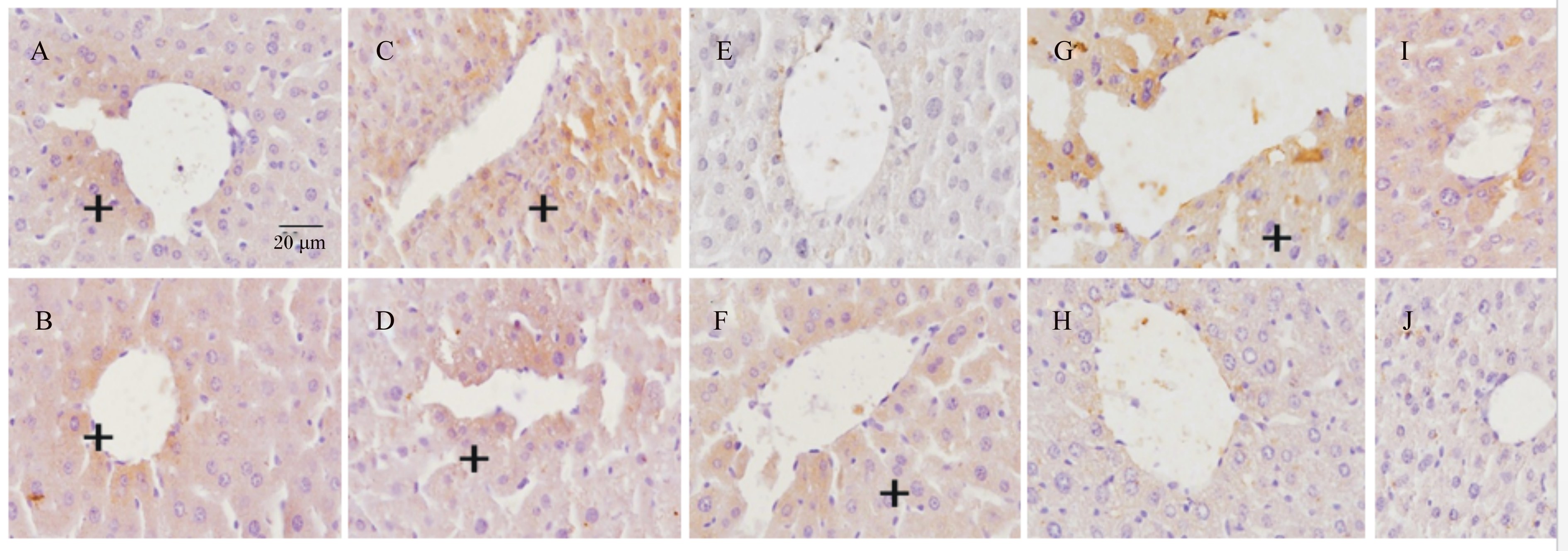 | 图3 tBHQ对热应激小鼠肝脏组织HO-1蛋白表达的影响
Fig. 3 Effects of tBHQ on HO-1 protein expression in liver of heat stressed mice |
由表4可知,与热应激0 d相比:tBHQ(-)组Keap1基因热应激后各时间点表达量显著降低(P<0.05),Nrf2基因热应激4 d,HO-1基因热应激1 d,NQO1和谷氨酰半胱氨酸合成酶催化亚单位(GCLC)基因热应激1和4 d表达量显著升高(P<0.05);tBHQ(+)组Keap1基因热应激4和8 d,Nrf2基因热应激1、2和8 d,HO-1基因热应激1和4 d,NQO1和GCLC基因热应激1 d表达量显著增加(P<0.05)。tBHQ(+)组与tBHQ(-)组相比,肝脏Keap1基因热应激4和8 d,Nrf2基因热应激1、2和8 d,HO-1基因热应激1和4 d,NQO1基因热应激0、1、2和8 d,GCLC基因热应激1 d的表达量均显著升高(P<0.05)。
| 表4 tBHQ对热应激小鼠肝脏Nrf2及其调控基因表达量的影响 Table 4 Effects of tBHQ on the expressions of Nrf2 and Nrf2-regulated genes in liver of heat stressed mice (n=5) |
Li等[20]研究表明,小鼠进行连续12 d每天2 h 42 ℃热处理,期间体表温度、直肠温度与热处理前相比显著升高,连续2 d热处理后导致小鼠血清皮质醇含量显著降低。本试验进行热应激处理时,小鼠刚开始时活动量增加,随着热处理时间的延长,小鼠开始变得安静,饮水增多,呼吸加快,说明小鼠确实受到了热应激,该热应激模型是成立的。Li等[20]研究发现,热处理8与12 d各项指标差异不显著,因此本试验只进行连续8 d热应激处理。试验过程中虽未能记录平均日采食量,但试验结束时发现tBHQ(+)组饲粮消耗明显少于tBHQ(-)组。推测这可能是由于tBHQ具有颜色和气味,使含有1% tBHQ的tBHQ(+)组饲粮不同与正常饲粮,这些可能影响了小鼠的采食量,导致tBHQ(+)组小鼠体重显著低于tBHQ(-)组。Shih等[19]研究结果显示,饲粮中添加1% tBHQ没有引起采食量的显著降低,这与本试验结果不符。经比较发现,Shih等[19]的试验中对照组饲粮中添加了丁基羟基茴香醚,丁基羟基茴香醚带有酚类的特异臭气和有刺激性的气味,这使对照组饲粮与tBHQ试验组饲粮保持类似气味和颜色。另外,Shih等[19]的试验中1% tBHQ预饲时间为7 d,而本试验预饲时间是14 d,因此饲喂tBHQ的时间也是体重显著下降的可能原因之一。
许多研究表明,热应激会造成肝脏组织的病变,对肝脏的正常功能产生负面影响。宁章勇等[21]将肉仔鸡置于34.5 ℃环境下,发现在热应激5 d后,肝脏组织血管充血,肝窦水肿增宽,从7 d开始肝细胞肿胀,出现水泡变性。本试验结果表明,热处理前肝脏组织细胞排列紧密,结构完整,热处理后肝脏组织中裂纹逐渐增多,排列疏松,血管增大,有的甚至破裂,红细胞进入组织,组织之间能看到多个红细胞分布,肝细胞水肿变大,与宁章勇等[21]在肉仔鸡上研究的结果基本一致。tBHQ(+)组小鼠只在热应激1 d时肝脏指数显著高于热应激前,而tBHQ(-)组小鼠热应激后肝脏指数在4 d时才恢复到正常水平。本试验还发现tBHQ(+)组小鼠热应激后肝脏损伤程度比tBHQ(-)组较轻微,热处理后,小鼠肝脏指数在1和2 d时显著升高,之后恢复到正常水平,这可能是由于热处理初期,肝脏内血管舒张,血压降低,有的甚至血管破裂,血液进入肝脏组织,使肝脏重量增大,造成肝脏指数增大。以上结果说明,饲粮添加tBHQ使小鼠肝脏指数迅速恢复到正常水平,提高了小鼠肝脏对热应激的抵抗能力。
Kim等[5]研究也表明,急性热应激后,大鼠肝脏MDA含量显著增加,微阵列分析发现与氧化应激和脂质过氧化反应相关的基因转录上调,脂质过氧化反应增强。本试验研究发现,热应激2和8 d时,tBHQ(+)组比tBHQ(-)组小鼠肝脏MDA含量都显著降低,说明tBHQ降低了小鼠肝脏脂质过氧化水平。Zhang等[22, 23]研究表明,急性热应激(动物暴露在40~42 ℃温度环境下)后,肝脏会产生一系列复杂的基因表达和生物适应性反应,产生氧自由基,造成氧化损伤和改变细胞内的信号转导,SOD和CAT活力也升高。Ando等[24]报道,热应激超过24 h会使大鼠和豚鼠肝脏中脂质过氧化水平和GSH-Px活力升高。本试验也发现,热应激4 d时tBHQ(+)组比tBHQ(-)组肝脏GSH含量以及GSH-Px、T-SOD、Cu,Zn-SOD活力都显著降低,说明tBHQ提高了小鼠肝脏抗氧化能力。
研究表明,IMR-32细胞经过tBHQ处理后,Nrf2的蛋白合成未显著增加,但是tBHQ稳定了Nrf2的结构,使Nrf2的半衰期由0.6 h上升到2.5 h。体外蛋白酶体活力检测表明,tBHQ没有蛋白酶体抑制剂的作用[25]。tBHQ不是靠抑制泛素酶体的活力,而是通过提高Nrf2的稳定性来增强Nrf2的活力。基础生理条件下,在细胞质中肌动蛋白结合蛋白Keap1与Nrf2相互作用,阻碍Nrf2入核。当Keap1基因的表达量降低时,Nrf2从Keap1中解离出来,转移入核,与核内抗氧化应答元件结合,激活下游基因的表达,调节抗氧化酶表达[26, 27]。本试验结果显示,热应激前,与tBHQ(-)组相比,tBHQ(+)组小鼠肝脏的GSH-Px和T-SOD活力显著升高,tBHQ(+)组小鼠肝脏的Keap1基因表达量显著降低,免疫组织化学染色发现肝细胞细胞质中有Nrf2和HO-1蛋白表达,这些结果说明饲粮添加tBHQ提高了小鼠肝脏的抗氧化水平。GSH-Px和T-SOD活力的升高可能是由于Keap1基因表达量下降和Nrf2稳定性增强引起的。
Paul等[28]研究发现,小鼠40 ℃水浴30 min后,睾丸中HO-1基因的表达量只在热应激后6 h时显著升高,其他时间与热应激前无显著差异;热应激后的HO-1蛋白含量与热应激前无显著差异。GCLC是合成GSH的限速酶亚基,GCLC基因表达量的增加有助于GSH的合成,NQO1也是体内重要的抗氧化酶。本试验结果显示,肝脏中Keap1和Nrf2基因的表达量没有很明显的相关性,具体机制还不明确,需要进一步研究。热应激4 d时,tBHQ(+)组小鼠肝脏中HO-1基因的表达量比tBHQ(-)组显著升高,与肝脏GSH含量以及GSH-Px、T-SOD和Cu,Zn-SOD活力变化相符。
小鼠预饲tBHQ饲粮可通过促进糖尿病小鼠肾小球中Nrf2蛋白的合成以及上调Keap1-Nrf2/ARE信号通路抗氧化基因HO-1和GCLC的转录,缓解高血糖症诱导的肾脏损伤[29]。另外,Nrf2+/-小鼠预饲tBHQ饲粮可增加纹状体、脑皮层和肝脏中谷胱甘肽S-转移酶和NQO1的活力,缓解3-硝基丙酸毒性作用,而Nrf2-/-小鼠预饲tBHQ饲粮未能缓解3-硝基丙酸毒性作用[19]。本试验结果表明,小鼠预饲tBHQ饲粮,热应激前肝细胞Nrf2蛋白有明显表达,并同时伴随着Nrf2基因表达量的上调。在热应激前,tBHQ(+)组小鼠肝脏就能检测到Nrf2蛋白,而tBHQ(-)组小鼠则没有,实时定量PCR结果同样显示tBHQ(+)组小鼠肝脏Nrf2基因表达量高于tBHQ(-)组。在热应激后,tBHQ(+)组小鼠肝脏Nrf2基因表达量高于tBHQ(-)组,但不存在时间相关性,在热应激小鼠肝脏Nrf2蛋白有明显表达,并且也诱导了下游抗氧化基因表达,tBHQ(+)组小鼠HO-1、NQO1和GCLC基因表达量显著高于tBHQ(-)组,也没有时间相关性。以上结果说明,预饲tBHQ可有效激活小鼠肝脏Keap1-Nrf2/ARE信号通路,并上调下游靶基因的表达。
4 结 论小鼠饲喂添加tBHQ的饲粮后,肝脏组织的病理损伤在热应激后变化不明显,肝脏指数迅速恢复到正常水平,说明饲粮添加tBHQ对肝脏具有一定的保护作用。饲粮添加1% tBHQ上调了小鼠肝脏组织Nrf2蛋白的表达以及Nrf2基因和其下游抗氧化基因的表达。tBHQ可能是通过激活Keap1-Nrf2/ARE信号通路来提高小鼠肝脏抗氧化水平的。
| [1] | HARIKAI N,SUGAWARA T,TOMOGANE K,et al.Acute heat stress induces jumping escape behavior in mice[J]. Physiology & Behavior,2004,83(3):373-376. ( 1) 1)
|
| [2] | ROBERTS W W,MOONEY R D,MARTIN J R.Thermoregulatory behaviors of laboratory rodents[J]. Journal of Comparative and Physiological Psychology,1974,86(4):693-699. ( 1) 1)
|
| [3] | ROBERTS W W.Differential thermosensor control of thermoregulatory grooming,locomotion,and relaxed postural extension[J]. Annals of the New York Academy of Sciences,1988,525:363-374. ( 1) 1)
|
| [4] | 姜忠玲.热应激对雄鼠生殖机能损伤的研究[D]. 博士学位论文.哈尔滨:东北农业大学,2006. ( 1) 1)
|
| [5] | KIM K J,HONG H D,LEE O H,et al.The effects of Acanthopanax senticosus on global hepatic gene expression in rats subjected to heat environmental stress[J]. Toxicology,2010,278(2):217-223. ( 2) 2)
|
| [6] | 王菲,黄毅,李延森,等.Keap1/Nrf2/ARE通路相关基因在热诱导的氧化应激小鼠肝脏中的表达[J]. 中国生物化学与分子生物学报,2014,30(3):284-290. ( 1) 1)
|
| [7] | TREVISAN M,BROWNE R,RAM M,et al.Correlates of markers of oxidative status in the general population[J]. American Journal of Epidemiology,2001,154(4):348-356. ( 1) 1)
|
| [8] | SCHUESSLER H,SCHILLING K.Oxygen effect in the radiolysis of proteins.Part 2.Bovine serum albumin[J]. International Journal of Radiation Biology and Related Studies in Physics,Chemistry,and Medicine,1984,45(3):267-281. ( 1) 1)
|
| [9] | DHAKSHINAMOORTHY S,LONG D J,JAISWAL A K.Antioxidant regulation of genes encoding enzymes that detoxify xenobiotics and carcinogens[J]. Current Topics in Cellular Regulation,2000,36:201-216. ( 1) 1)
|
| [10] | ZHANG D D.Mechanistic studies of the Nrf2-Keap1 signaling pathway[J]. Drug Metabolism Reviews,2006,38(4):769-789. ( 1) 1)
|
| [11] | KOBAYASHI M,YAMAMOTO M.Nrf2-Keap1 regulation of cellular defense mechanisms against electrophiles and reactive oxygen species[J]. Advances in Enzyme Regulation,2006,46(1):113-140. ( 1) 1)
|
| [12] | WALLACE S K,MOZAFFARIAN D.Trans-fatty acids and nonlipid risk factors[J]. Current Atherosclerosis Reports,2009,11(6):423-433. ( 1) 1)
|
| [13] | KEUM Y S,HAN Y H,LIEW C,et al.Induction of heme oxygenase-1 (HO-1) and NAD H:quinone oxidoreductase 1 (NQO1) by a phenolic antioxidant,butylated hydroxyanisole (BHA) and its metabolite,tert-butylhydroquinone (tBHQ) in primary-cultured human and rat hepatocytes[J]. Pharmaceutical Research,2006,23(11):2586-2594. ( 1) 1)
|
| [14] | LAMB J G,FRANKLIN M R.Early events in the induction of rat hepatic UDP-glucuronosyltransferases,glutathione S-transferase,and microsomal epoxide hydrolase by 1,7-phenanthroline:comparison with oltipraz,tert-butyl-4-hydroxyanisole,and tert-butylhydroquinone[J]. Drug Metabolism and Disposition:the Biological Fate of Chemicals,2000,28(9):1018-1023. ( 1) 1)
|
| [15] | NAKAMURA Y,KUMAGAI T,YOSHIDA C,et al.Pivotal role of electrophilicity in glutathione S-transferase induction by tert-butylhydroquinone[J]. Biochemistry,2003,42(14):4300-4309. ( 1) 1)
|
| [16] | PERÉZ-ROJAS J M,GUERRERO-BELTRÁN C E,CRUZ C,et al.Preventive effect of tert-butylhydroquinone on cisplatin-induced nephrotoxicity in rats[J]. Food and Chemical Toxicology,2011,49(16):2631-2637. ( 1) 1)
|
| [17] | LI H Y,WU S Y,WANG Z J,et al.Neuroprotective effects of tert-butylhydroquinone on paraquat-induced dopaminergic cell degeneration in C57BL/6 mice and in PC12 cells[J]. Archives of Toxicology,2012,86(11):1729-1740. ( 1) 1)
|
| [18] | LI Y S,PIAO Y G,NAGAOKA K,et al.Preventive effect of tert-butylhydroquinone on scrotal heat-induced damage in mouse testes[J]. Genetics and Molecular Research,2013,12(4):5433-5441. ( 1) 1)
|
| [19] | SHIH A Y,IMBEAULT S,BARAKAUSKAS V,et al.Induction of the Nrf2-driven antioxidant response confers neuroprotection during mitochondrial stress in vivo[J]. The Journal of Biological Chemistry,2005,280(24):22925-22936. ( 5) 5)
|
| [20] | LI Y S,HUANG Y,PIAO Y G,et al.Protective effects of nuclear factor erythroid 2-related factor 2 on whole body heat stress-induced oxidative damage in the mouse testis[J]. Reproductive Biology and Endocrinology,2013,11(1):23. ( 2) 2)
|
| [21] | 宁章勇,刘思当,赵德明,等.热应激对肉仔鸡呼吸、消化和内分泌器官的形态和超微结构的影响[J]. 畜牧兽医学报,2003,34(6):558-561. ( 2) 2)
|
| [22] | ZHANG H J,DRAKE V J,MORRISON J P,et al.Selected contribution:differential expression of stress-related genes with aging and hyperthermia[J]. Journal of Applied Physiology,2002,92(4):1762-1769. ( 1) 1)
|
| [23] | ZHANG H J,XU L,DRAKE V J,et al.Heat-induced liver injury in old rats is associated with exaggerated oxidative stress and altered transcription factor activation[J]. The Federation of American Societies for Experimental Biology,2003,17(15):2293-2295. ( 1) 1)
|
| [24] | ANDO M,KATAGIRI K,YAMAMOTO S,et al.Age-related effects of heat stress on protective enzymes for peroxides and microsomal monooxygenase in rat liver[J]. Environmental Health Perspectives,1997,105(7):726-733. ( 1) 1)
|
| [25] | LI J,JOHNSON D,CALKINS M,et al.Stabilization of Nrf2 by tBHQ confers protection against oxidative stress-induced cell death in human neural stem cells[J]. Toxicological Sciences,2005,83(2):313-328. ( 1) 1)
|
| [26] | 李煌元,石年.Keap1-Nrf2/ARE通路在分子毒理学中的研究进展[J]. 国外医学:卫生学分册,2006,33(3):129-135. ( 1) 1)
|
| [27] | 刘芳,杜志银,王应雄.Keap1在氧化应激方面的研究进展[J]. 中国临床药理学与治疗学,2010,15(5):596-600. ( 1) 1)
|
| [28] | PAUL C,TENG S,SAUNDERS P T.A single,mild,transient scrotal heat stress causes hypoxia and oxidative stress in mouse testes,which induces germ cell death[J]. Biology of Reproduction,2009,80(5):913-919. ( 1) 1)
|
| [29] | LI H,ZHANG L S,WANG F X,et al.Attenuation of glomerular injury in diabetic mice with tert-butylhydroquinone through nuclear factor erythroid 2-related factor 2-dependent antioxidant gene activation[J]. American Journal of Nephrology,2011,33(4):289-397. ( 1) 1)
|




