2. 生物饲料开发国家工程研究中心, 北京 100081
2. National Engineering Research Center of Biological Feed, Beijing 100081, China
现代肉鸡品种具有生长速度快,饲料转化率高的生物学特点,这一特点与其肠道具有较强的营养物质消化吸收能力密不可分。饲粮蛋白质是动物生长所需的重要营养素之一,大量研究表明,饲粮蛋白质在肉鸡肠道内的主要消化产物寡肽和氨基酸是通过位于肠上皮细胞刷状缘膜和基底膜的寡肽转运载体和各种氨基酸转运载体协同转运而被吸收的[1, 2]。其中,2/3的氨基酸是以小肽的形式被吸收,其余氨基酸以游离氨基酸的形式被吸收。小肽转运载体1(peptide transporter 1,PepT1)、B0系统中性氨基酸转运载体(system B0 neutral amino-acid transporter,B0AT)、兴奋性氨基酸转运载体3(excitatory amino-acid transporter 3,EAAT3)分别是位于肉鸡肠道上皮细胞刷状缘膜上的小肽、中性氨基酸及酸性氨基酸的转运载体。其中,PepT1是低亲和力、高容量的肽载体,以肠黏膜细胞H+梯度为动力转运大多数2肽和3肽,但不能转运游离氨基酸、4肽及以上的寡肽[3, 4];B0AT是Na+依赖性中性氨基酸转运载体,具有广泛的底物选择性,对亮氨酸、异亮氨酸、蛋氨酸和缬氨酸等大型脂肪族氨基酸转运效率较高,而对其他亲水性氨基酸的转运效率则较低[5];EAAT3又称EAAC1,是Na+依赖性酸性氨基酸转运载体,负责转运天冬氨酸和L-谷氨酸[6]。
研究表明,PepT1、B0AT、EAAT3在动物体内的表达受多种因素的影响,如品种[7]、发育阶段[8, 9]、肠段[10]、激素[11, 12, 13, 14, 15]、饲粮蛋白质水平及质量[16, 17]、限饲[18, 19, 20]等。其中,肠段和发育阶段是影响上述转运载体在动物体内表达的2个重要因素,一般认为,动物利用蛋白质氨基酸的能力随动物的发育阶段发生变化,且不同肠段对于氨基酸吸收能力不同,从分子水平研究肠道小肽、氨基酸转运载体mRNA的发育变化对于深入探讨肉仔鸡蛋白质氨基酸的吸收利用以及动物生产性能具有重要意义。但是,目前国内外关于肠段及发育阶段对肉仔鸡肠道PepT1、B0AT、EAAT3 mRNA表达影响的研究仍不完善,尤其是对B0AT、EAAT3表达影响的研究相对较少。因此,本试验以爱拔益加(AA)肉仔鸡为研究对象,对其肠道PepT1、B0AT、EAAT3 mRNA的表达差异和发育变化进行研究,以期获得AA肉仔鸡不同肠段及不同发育阶段PepT1、B0AT、EAAT3 mRNA表达发育规律,进而为AA肉仔鸡小肽、中性氨基酸以及酸性氨基酸营养的基因表达调控和合理的氨基酸配比提供理论依据。
1 材料与方法 1.1 试验动物与分组选取1日龄健康雄性AA肉仔鸡120只(购自北京华都肉鸡公司),按照平均体重一致原则分为8个组(笼),每个组15只鸡。
1.2 试验饲粮与饲养管理饲养试验在中国农业科学院南口中试基地进行,参照我国《鸡饲养标准》(NY/T 33—2004)和AA肉仔鸡商品代营养标准配制饲粮,基础饲粮组成及营养水平见表1。采用3层笼养,人工光照与自然光照相结合,每天光照23 h,自由饮水和采食,按AA肉仔鸡饲养手册进行常规管理及免疫。
| 表1 基础饲粮组成及营养水平(风干基础)Table 1 Composition and nutrient levels of basal diets (air-dry basis) |
分别于1、7、14、21、28、35、42日龄,每个组(笼)随机取1只接近平均体重的鸡,宰前不禁食。断颈屠宰,分离肠道,分别从十二指肠U状弯曲的起始处和结束处向下取3~5 cm肠段,作为十二指肠和空肠样品;从回盲韧带起始处向下取3~5 cm肠段作为回肠样品;沿纵向剖开,用4 ℃预冷灭菌磷酸盐缓冲液(PBS)冲洗,吸水纸吸干。用灭菌刀片迅速刮取肠道黏膜,放入1.5 mL离心管中,置液氮速冻,-70 ℃冷冻保存,待测。
1.4 肠道PepT1、B0AT、EAAT3 mRNA的相对表达量 1.4.1 总RNA的提取及反转录采用RNAprep pure动物组织总RNA提取试剂盒(北京天根生物科技公司)提取RNA,紫外分光光度计测定总RNA的浓度和纯度。用1.2%甲醛变性琼脂糖凝胶电泳,根据28S rRNA和18S rRNA的灰度比评定RNA的质量。
采用FastQuant cDNA第一链合成试剂盒(北京天根生物科技公司)进行反转录。以2 μg总RNA样品为模板,反转录为20 μL体系,严格按照试剂盒说明进行操作。
1.4.2 引物设计根据GenBank发表的β-肌动蛋白(β-actin)、PepT1、B0AT和EAAT3的基因序列,采用Primer 5.0软件设计引物(表2),由北京赛百盛基因技术有限公司合成。
采用SYBR Green实时荧光定量PCR方法,以β-actin rRNA作为内参,对PepT1、B0AT和EAAT3进行相对定量分析。实时荧光定量PCR试剂盒SYBR Premix Ex Taq购自康为世纪生物科技有限公司,在实时荧光定量PCR仪(Bio-Rad CFX96TMReal-Time PCR,美国)上进行。
实时荧光定量PCR反应体系为20 μL:Premix Ex TaqTM 10 μL,上、下游引物(10 μmol/L)各0.5 μL,cDNA模板2 μL,ddH2O 8 μL。反应条件:95 ℃ 10 min预变性;95 ℃ 20 s变性,60 ℃ 30 s退火,进行40个循环,60 ℃收集荧光。每个待测样品设置3个平行,取3个Ct值的平均值,以备后续公式计算。
1.5 数据分析采用2-ΔΔCt法计算目的基因的相对表达量,数据用SPSS 19.0 General Liner Model的Univariate方法进行双因素方差分析,对F检验达到显著水平的因子,进行LSD法多重比较,分析结果包括日龄、肠段以及“日龄×肠段”互作3个影响模型。不同肠段的PepT1、B0AT和EAAT3 mRNA表达的发育变化用ANOVA进行单因子方差分析,Duncan氏法进行多重比较检验。数据采用柱形图表示,误差线表示标准差,P<0.05表示差异显著。
2 结 果 2.1 AA肉仔鸡肠道PepT1 mRNA的发育变化由图1可见,十二指肠与空肠、回肠PepT1 mRNA表达的发育变化相似,但不完全相同。十二指肠PepT1 mRNA的相对表达量1~14日龄迅速上升达到峰值,14~35日龄相对稳定,稍有下降,42日龄回升;其中14~35日龄PepT1 mRNA的相对表达量无显著差异(P>0.05),与1~7日龄相比显著升高(P<0.05)。空肠PepT1 mRNA的相对表达量1~28日龄不断上升达到峰值,28~42日龄相对稳定;其中14~42日龄PepT1 mRNA的相对表达量显著高于1~7日龄(P<0.05),但21~42日龄之间无显著差异(P>0.05)。回肠PepT1 mRNA的相对表达量1~21日龄不断上升,21~42日龄趋于稳定;其中21~42日龄之间PepT1 mRNA的相对表达量无显著差异(P>0.05),但显著高于1~7日龄(P<0.05)。
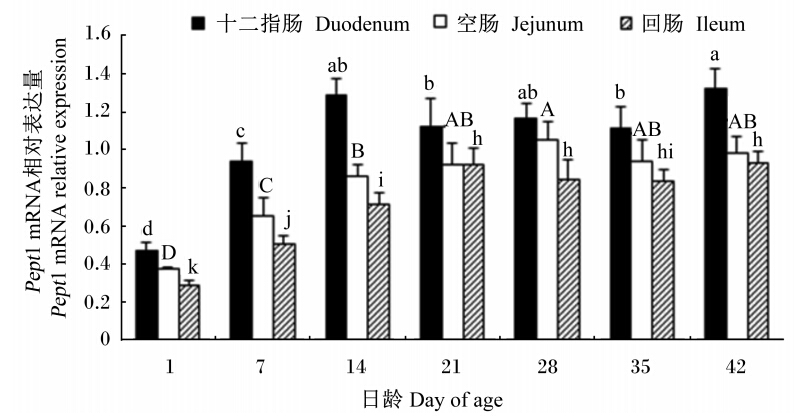 | 图1 AA肉仔鸡肠道PepT1 mRNA的发育变化Fig. 1 Ontogenetic changes of PepT1 mRNA in the intestine of AA broilers (n=8) |
由图2可见,十二指肠、空肠、回肠B0AT mRNA的相对表达量随日龄增加,其上升的速度、变化趋势不同。十二指肠B0AT mRNA的相对表达量1~14日龄下降,14~35日龄上升至最高水平,42日龄下降;其中14日龄B0AT mRNA的相对表达量最低,但与7日龄相比无显著差异(P>0.05),35日龄最高,显著高于其他日龄(P<0.05),是1日龄的1.44倍。空肠B0AT mRNA的相对表达量1~21日龄增加至峰值,28日龄开始下降,28~42日龄相对稳定;其中21日龄B0AT mRNA的相对表达量显著高于其他日龄(P<0.05),是1日龄的1.82倍。回肠B0AT mRNA的相对表达量1~7日龄迅速上调至最高,7~42日龄相对稳定;其中7~42日龄之间B0AT mRNA的相对表达量无显著差异(P>0.05),但显著高于1日龄(P<0.05),14日龄是1日龄的3.79倍。
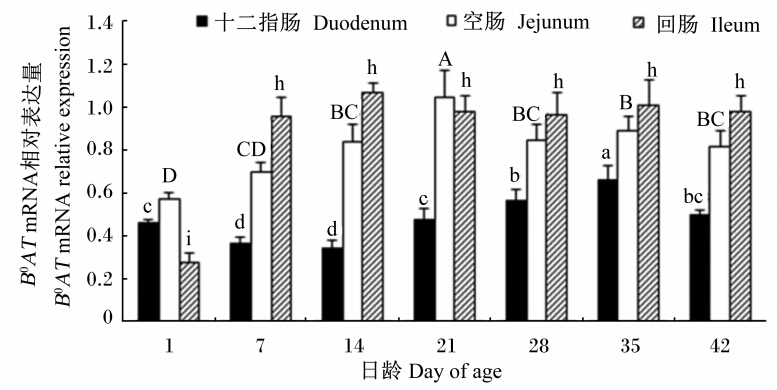 | 图2 AA肉仔鸡肠道B0AT mRNA的发育变化Fig. 2 Ontogenetic changes of B0AT mRNA in the intestine of AA broilers (n=8) |
由图3可见,十二指肠、空肠、回肠EAAT3 mRNA表达的发育变化不同。十二指肠EAAT3 mRNA的相对表达量1~7日龄迅速增加,7~21日龄下降,后期在一定范围内呈现波浪型变化;其中7、14、28、35日龄之间EAAT3 mRNA的相对表达量无显著差异(P>0.05),28日龄最高,是1日龄的1.82倍。空肠和回肠EAAT3 mRNA表达发育规律相似,空肠1~21日龄EAAT3 mRNA的相对表达量增加,21~42日龄相对稳定;其中14~42日龄EAAT3 mRNA的相对表达量显著高于1~7日龄(P<0.05),21日龄是1日龄的1.87倍。回肠1~14日龄EAAT3 mRNA的相对表达量增加,14~21日龄相对稳定;其中1日龄EAAT3 mRNA的相对表达量显著低于其他日龄(P<0.05),14日龄是1日龄的2.37倍。
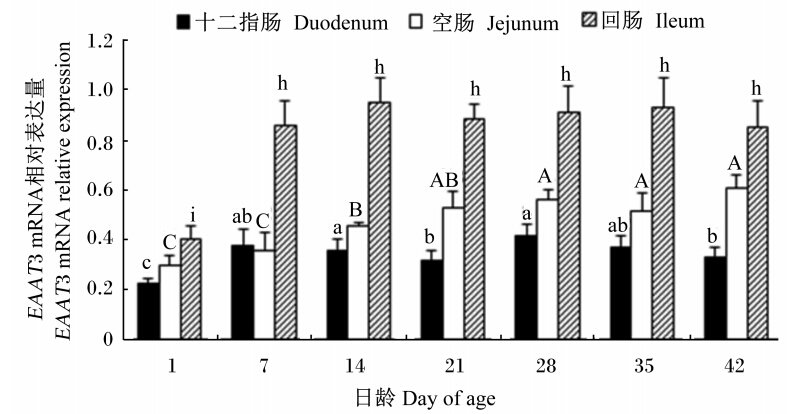 | 图3 AA肉仔鸡肠道EAAT3 mRNA的发育变化Fig. 3 Ontogenetic changes of EAAT3 mRNA in the intestine of AA broilers (n=8) |
由表3可以看出,PepT1 mRNA的相对表达量十二指肠最高,空肠次之,回肠最低。其中PepT1 mRNA的相对表达量十二指肠显著高于空肠、回肠(P<0.05),空肠显著高于回肠(P<0.05)。B0AT mRNA的相对表达量从十二指肠、空肠、回肠依次升高,其中回肠显著高于空肠、十二指肠(P<0.05),空肠显著高于十二指肠(P<0.05)。EAAT3 mRNA的相对表达量回肠最高,空肠次之,十二指肠最低,其中回肠显著高于空肠、十二指肠(P<0.05),空肠显著高于十二指肠(P<0.05)。
| 表3 肠段、日龄对PepT1、B0AT、EAAT3 mRNA的相对表达量的影响Table 3 Effects of intestinal segment and day of age on the relative expression of PepT1,B0AT and EAAT3 mRNA |
AA肉仔鸡十二指肠、空肠、回肠PepT1、B0AT、EAAT3 mRNA的相对表达量均存在极显著差异(P<0.000 1、P<0.000 1、P=0.000 4);不同日龄AA肉仔鸡肠道PepT1、B0AT、EAAT3 mRNA相对表达量存在极显著差异(P=0.000 1、P=0.000 1、P<0.000 1);PepT1和B0AT mRNA的相对表达量均存在“肠段×日龄”的互作效应(P=0.026 2、P<0.000 1),EAAT3 mRNA的相对表达量不存在“肠段×日龄”的互作效应(P=0.065 0)。
3 讨 论 3.1 AA肉仔鸡肠道PepT1 mRNA的表达差异与发育变化通过PepT1转运小肽是肠上皮吸收氨基酸的主要途径之一[21],这一途径能有效避免游离氨基酸吸收时氨基酸之间的相互竞争,因此,与氨基酸转运载体介导的转运相比,其转运速度更快,转运效率更高[22]。PepT1 mRNA主要在肠上皮刷状缘膜上表达,不同动物肠段表达差异性不同。小鼠十二指肠和空肠的相对表达量较高,回肠较低[4],猪空肠PepT1 mRNA的相对表达量较高,而反刍动物以空肠和回肠为主[23]。本试验结果发现,AA肉仔鸡肠道PepT1 mRNA的相对表达量在十二指肠最高,空肠次之,回肠最低。这与之前的研究结果基本一致[10,24]。PepT1 mRNA肠段的差异性表达可能反映了动物不同肠段对小肽的吸收状况。研究表明,猪空肠PepT1 mRNA的相对表达量最高[25],且猪肠道小肽的主要吸收部位是空肠[26],其PepT1 mRNA的肠道分布与小肽的主要吸收部位相一致,由此结合本试验结果可推测肉仔鸡小肽的主要吸收部位位于十二指肠。
动物PepT1 mRNA的表达随发育阶段表现出一定的规律。Miyamoto等[27]通过对小鼠PepT1 mRNA的表达发育规律的研究发现,小鼠生长前期相对表达量较高,到28日龄时量下降至成年鼠的表达水平。Gilbert等[28]对肉仔鸡的研究表明,PepT1 mRNA的相对表达量从18胚龄到14日龄呈直线增加,与本试验十二指肠、空肠、回肠PepT1 mRNA的相对表达量的发育规律具有相似性,均表现为生长前期增加,后期稳定。江勇[29]对肉仔鸡的研究表明,十二指肠PepT1 mRNA的相对表达量与空肠呈现相反的趋势,十二指肠呈上升趋势,而空肠呈下降趋势。王修启等[24]研究对岭南黄羽肉鸡和AA肉仔鸡PepT1 mRNA的发育性研究表明,PepT1 mRNA在十二指肠和空肠具有相同的发育模式,生长前期相对表达量增加,后期下降,造成这种差异的原因还需进一步研究。
AA肉仔鸡从出生起生长速度逐渐增加,5周龄左右生长速度达到最高[30]。本试验结果显示,肉仔鸡生长前期小肽转运载体mRNA的相对表达量逐渐增加,14日龄达到峰值。这一结果一方面从分子水平与肉仔鸡生长规律相印证;另一方面也可据此推测生长前期肉仔鸡主要通过调节营养物质转运载体转录水平的表达来满足动物对营养物质的需求,而14日龄之后则通过调节营养物质转运载体翻译水平的表达或者调节转运载体的活性来满足动物对营养物质的需求。
3.2 AA肉仔鸡肠道B0AT mRNA的表达差异与发育变化中性氨基酸主要通过肠黏膜细胞顶端的Na+/氨基酸共转运系统(尤其是系统B0),在Na+驱动作用下逆浓度梯度被吸收进入肠细胞。B0AT亚型载体的基因最先是从小鼠肾脏克隆得到[31],具有广泛的底物选择性,能转运大部分中性氨基酸,是色氨酸在肠道中唯一的转运载体[32]。B0AT mRNA主要在肾脏和肠道上皮刷状缘膜表达,研究表明B0AT mRNA的相对表达量在小鼠空肠和回肠较高,而十二指肠较低[33]。Gilbert等[28]研究发现,肉仔鸡回肠B0AT mRNA的相对表达量最高,空肠和十二指肠差异不显著。而本试验AA肉仔鸡回肠B0AT mRNA的相对表达量最高,空肠次之,十二指肠最低,且回肠、空肠B0AT mRNA的相对表达量是十二指肠的2倍左右(分别为2.09、1.91)。这与Gilbert等[28]的研究结果不完全一致,空肠B0AT mRNA的相对表达量显著高于回肠,这可能与研究的品种、饲粮组成和发育阶段不同有关。
目前国内外关于肉仔鸡肠道B0AT mRNA的表达发育规律的研究较少,Zeng等[9]对温氏土鸡和白洛克鸡种蛋的研究表明,B0AT mRNA的相对表达量随胚龄增加而上调;Gilbert等[28]对肉仔鸡肠道B0AT mRNA的表达发育规律研究也表明,从18胚龄到14日龄,肉仔鸡肠道B0AT mRNA的相对表达量随日龄呈直线增长。本试验结果表明,空肠和回肠B0AT mRNA的发育模式相似,均表现为生长前期增加,后期维持稳定,而十二指肠前期降低,后期升高。生长前期B0AT mRNA的相对表达量随日龄增加,这与PepT1 mRNA的发育规律一致。此外,各个肠段B0AT mRNA表达发育模式不一,也提示各肠段吸收中性氨基酸的能力不同。
3.3 AA肉仔鸡肠道EAAT3 mRNA的表达差异与发育变化EAAT3最先在家兔小肠分离得到,主要转运谷氨酸。研究表明EAAT3转运谷氨酸的主要作用是满足上皮细胞迅速增殖所需的代谢物质和能量[31],肠段EAAT3 mRNA的相对表达量差异导致不同肠段对谷氨酸的转运能力不同[34],本试验中AA肉仔鸡回肠EAAT3 mRNA的相对表达量最高,空肠次之,十二指肠最低,这与Gilbert等[28]的研究结果基本一致。此外,本试验还发现,肉仔鸡肠道EAAT3 mRNA的相对表达量远端显著高于近端,类似结果同样见于Romeo等[33]对小鼠的研究发现。
目前,国内外有关肉仔鸡肠道EAAT3 mRNA的表达发育规律的研究较少。Romeo等[33]对小鼠的研究表明,EAAT3 mRNA的相对表达量随日龄而增加,黎相广等[35]对温氏土鸡和白洛克鸡胚EAAT3 mRNA表达发育的研究表明,EAAT3 mRNA的相对表达量随胚龄而增加。本试验中,空肠和回肠发育模式具有相似性,前期随日龄增加,后期相对稳定。十二指肠1~7日龄EAAT3 mRNA的相对表达量上调,后期发育在一定范围内呈波浪型变化。一般而言,肠道发育前期生长速度较快,后期生长速度缓慢[36]。结合本试验结果我们推测,AA肉仔鸡生长前期机体通过调节EAAT3 mRNA的转录水平来满足肠道上皮黏膜细胞迅速增殖所需的底物和能量,14日龄达到表达峰值后,机体则通过调节EAAT3的翻译水平或EAAT3转运载体的活性来满足肠黏膜的代谢需要。
3.4 肠段、日龄对PepT1、B0AT、EAAT3 mRNA的 相对表达量的影响AA肉仔鸡PepT1、B0AT mRNA的相对表达量存在“肠段×日龄”互作效应,而EAAT3 mRNA的相对表达量不存在“肠段×日龄”互作效应,这与Gilbert等[28]的研究结果不一致,可能是由于饲粮、发育阶段等不同而导致的。由于缺乏相应抗体,本研究仅对PepT1、B0AT、EAAT3进行了mRNA水平的测定,至于蛋白质水平的表达和转运载体活性是否与mRNA水平同步,仍需要进一步的研究。
4 结 论① PepT1 mRNA的相对表达量在十二指肠最高,空肠次之,回肠最低;B0AT、EAAT3 mRNA的相对表达量在回肠最高,空肠次之,十二指肠最低。
② 肉仔鸡不同日龄PepT1、B0AT、EAAT3 mRNA的相对表达量差异显著;在不同肠段上,PepT1、B0AT、EAAT3 mRNA的相对表达量随日龄的变化均表现为前期升高,后期平稳的变化趋势。
③ PepT1、B0AT mRNA的相对表达量存在“肠段×日龄”互作效应,EAAT3 mRNA的相对表达量不存在“肠段×日龄”互作效应。
| [1] | MENTLEINl R.Cell-surface peptidases[J]. International Review of Cytology,2004,235:165-213. ( 1) 1)
|
| [2] | ALPERS D H.Digestion and absorption of carbohydrates and proteins[M]. New York:Raven Press,1987:1469-1487. ( 1) 1)
|
| [3] | BRANDSCH M,KNVTTER I,LEIBACH F H.The intestinal H+/peptide symporter PEPT1:structure-affinity relationships[J]. European Journal of Pharmaceutical Sciences,2004,21(1):53-60. ( 1) 1)
|
| [4] | DANIEL H.Molecular and integrative physiology of intestinal peptide transport[J]. Annual Review of Physiol,2004,66(1):361-384. ( 2) 2)
|
| [5] | BROER S.The role of the neutral amino acid transporter B0AT1 (SLC6A19) in Hartnup disorder and protein nutrition[J]. IUBMB Life,2009,61(6),591-599. ( 1) 1)
|
| [6] | KANAI Y,HEDIGER M A.The glutamate/neutral amino acid transporter family SLC1:molecular,physiological and pharmacological aspects[J]. Pflügers Archiv,2004,447:469-479. ( 1) 1)
|
| [7] | GILBERT E R,LI H,EMMERSON D A,et al.Dietary protein composition influences abundance of peptide and amino acid transporter messenger ribonucleic acid in the small intestine of 2 lines of broiler chicks[J]. Poultry Science,2010,89(8):1663-1676. ( 1) 1)
|
| [8] | HUMPHREY B D,STEPHENSEN C B,CALVERT C C,et al.Glucose and cationic amino acid transporter expression in growing chickens (Gallus gallusdomesticus)[J]. Comparative Biochemistry and Physiology Part A:Molecular and Integrative Physiology,2004,138(4):515-525. ( 1) 1)
|
| [9] | ZENG P L,LI X G,WANG X Q,et al.The relationship between gene expression of cationic and neutral amino acid transporters in the small intestine of chick embryos and chick breed,development,sex,and egg amino acid concentration[J]. Poultry Science,2011,90(11):2548-2556. ( 2) 2)
|
| [10] | 刘国华,蔡辉益,郑爱娟,等.半定量RT-PCR法评定鸡小肠肽转运载体cPepT1基因的表达[J]. 农业生物技术学报,2006,14(4):489-492. ( 1) 1)
|
| [11] | HU X F,GUO Y M,HUANG B Y,et al.Effect of corticosterone administration on small intestinal weight and expression of small intestinal nutrient transporter mRNA of broiler chickens[J]. Animal Science,2010,23(2):175-181. ( 1) 1)
|
| [12] | HANG C H,SHI J X,SUN B W,et al.Apoptosis and functional changes of dipeptide transporter (PepT1) in the rat small intestine after traumatic brain injury[J]. Journal of Surgical Research,2007,137(1):53-60. ( 1) 1)
|
| [13] | 孙炳伟,赵小辰,王广基,等.缺氧复氧损伤后小肠上皮细胞刷状缘二肽转运载体生物学功能的改变及生长激素的调控作用[J]. 解放军医学杂志,2003,28(11):1025-1027. ( 1) 1)
|
| [14] | MEREDITH D,BOYD C A R.Structure and function of eukaryotic peptide transporters[J]. Cellular and Molecular Life Sciences,2000,57(5):754-778. ( 1) 1)
|
| [15] | NIELSEN C U,AMSTRUP J,STEFFANSEN B,et al.Epidermal growth factor inhibits glycylsarcosine transport and hPepT1 expression in a human intestinal cell line[J]. American Journal of Physiology:Gastrointestinal and Liver Physiology,2001,281(1):G191-G199. ( 1) 1)
|
| [16] | CHEN H,PAN Y X,WONG E A,et al.Dietary protein level and stage of development affect expression of an intestinal peptide transporter (cPepT1) in chickens[J]. The Journal of Nutrition,2005,135(2):193-198. ( 1) 1)
|
| [17] | ZHANG S H,QIAO S Y,REN M,et al.Supplementation with branched-chain amino acids to a low-protein diet regulates intestinal expression of amino acid and peptide transporters in weanling pigs[J]. Amino Acids,2013,45(5):1191-1205. ( 1) 1)
|
| [18] | GILBERT E R,LI H F,EMMERSON D A,et al.Dietary protein quality and feed restriction influence abundance of nutrient transporter mRNA in the small intestine of broiler chicks[J]. The Journal of Nutrition,2008,138(2):262-271. ( 1) 1)
|
| [19] | DUARTE C R A,VICENTINI-PAULINO M L M,BURATINI J,Jr,et al.Messenger ribonucleic acid abundance of intestinal enzymes and transporters in feed-restricted and refed chickens at different ages[J]. Poultry Science 2011,90(4):863-868. ( 1) 1)
|
| [20] | IHARA T,TSUJIKAWA T,FUJIYAMA Y,et al.Regulation of Pept1 peptide transporter expression in the rat small intestine under malnourished conditions[J]. Digestion,2000,61(1):59-67. ( 1) 1)
|
| [21] | CHEN H,PAN Y,WONG E A,et al.Molecular cloning and functional expression of a chicken intestinal peptide transporter (cPepT1) in xenopus oocytes and Chinese hamster ovary cells[J]. The Journal of Nutrition,2002,132:387-393. ( 1) 1)
|
| [22] | RERAT A,SIMONES-NUNES C.Splanchnic fluxes of amino acids after duodenal infusion of carbohydrate solutions containing free amino acids or oligopeptides in the non-anaesthetized pig[J]. British Journal of Nutrition,1992,68(1):111-138. ( 1) 1)
|
| [23] | CHEN H,WONG E A,WEBB K B.Tissue distribution of peptide transporter mRNA in sheep,dairycows,pigs,and chickens[J]. Animal Science,1999,77(5):1277-1283 ( 1) 1)
|
| [24] | 王修启,邹仕庚,左建军,等.肉鸡肠道PepT1 mRNA表达的肠段差异性与发育性变化[J]. 畜牧兽医学报,2007,38(8):814-821. ( 1) 1)
|
| [25] | WINCKLER C,BREVES G,BOLL M,et al.Characteristics of dipeptide transport in pig jejunum in vitro[J]. Journal of Comparative Physiology B:Biochemical Systemic and Environmental Physiology,1999,169(7):495-500. ( 1) 1)
|
| [26] | 赵昕红,李德发,JOHNSON E W.仔猪小肠对二肽吸收特点的研究[J]. 中国畜牧杂志,1999,35(3):14-15. ( 1) 1)
|
| [27] | MIYAMOTO K,SHIRAGA T,MORITA K,et al.Sequence,tissue distribution and developmental changes in rat intestinal oligopeptide transporter[J]. Biochim Biophysica Acta:Gene Structure and Expression,1996,1305(1/2):34-38. ( 1) 1)
|
| [28] | GILBERT E R,LI H,EMMERSON D A,et al.Developmental regulation of nutrient transporter and enzyme mRNA abundance in the small intestine of broilers[J]. Poultry Science,2007,86(8):1739-1753. ( 6) 6)
|
| [29] | 江勇.肉仔鸡小肽转运载体的克隆表达及其转运调控研究[D]. 博士学位论文.北京:中国农业科学院,2008. ( 1) 1)
|
| [30] | 杨志刚.肉仔鸡氨基酸营养需要仿真模型的研究[D]. 博士学位论文.北京:中国农业科学院,2010. ( 1) 1)
|
| [31] | BRÖER A,LINGEl K,KOWALCZUK S,et al.Molecular cloning of mouse amino acid transport system B0,a neutral amino acid transporter related to Hartnup disorder[J]. Journal of Biological Chemistry,2004,279(23):24467-24476. ( 2) 2)
|
| [32] | JONAS A J,BUTLER I J.Circumvention of defective neutral amino acid transport in Hartnup disease using tryptophan ethylester[J]. Journal of Clinical Investigation,1989,84(1):200-204. ( 1) 1)
|
| [33] | ROMEO E,DAVE M H,BACIC D,et al.Luminal kidney and intestine SLC6 amino acid transporters of B0AT-cluster and their tissue distribution in Mus musculus[J]. American Journal of Physiology:Renal Physiology,2006,290(2):F376-F383. ( 3) 3)
|
| [34] | YOSHIDA A,TAKATA K,KASAHARA T,et al.Immunohistochemical localization of Na-dependent glucose transporter in the rat digestive tract[J]. The Histochemical Journal,1995,27(5):420-426. ( 1) 1)
|
| [35] | 黎相广,严会超,曾佩玲,等.温氏土鸡和白洛克鸡胚小肠EAATs mRNA表达差异及发育性变化[J]. 中国农业科学,2012,44(21):4474-4480. ( 1) 1)
|
| [36] | 黎观红,瞿明仁,晏向华,等.泰和鸡早期(0-12周龄)内脏器官生长发育规律的研究[J]. 经济动物学报,2005,9(1):35-38. ( 1) 1)
|




