2. 宁波卫生职业技术学院, 宁波 315010;
3. 宁波市海洋与渔业研究院, 宁波 315012
2. Ningbo College of Health Sciences, Ningbo 315010, China;
3. Ningbo Academy of Ocean and Fishery, Ningbo 315012, China
大黄鱼(Pseudosciaena crocea)为我国主要海产经济动物之一,其含有丰富的蛋白质、微量元素和维生素,肉质细嫩,营养丰富,是人类比较理想的动物性蛋白质[1]。目前,大黄鱼主要有2个养殖群体,分别为岱衢族大黄鱼和闽-粤东族大黄鱼,其中岱衢族大黄鱼产自浙江省岱山县境内的岱衢洋,两大养殖群体之间的差异尽管未达到亚种水平,但在一些形态指标上存在着显著差异[2]。与市场上的闽-粤东族大黄鱼相比,岱衢族大黄鱼头大、吻短、体形偏长,通体呈金黄或虎黄色,鱼鳞光泽,鳃丝清晰呈鲜红或紫红色,眼球饱满,在体色、体形和风味等方面具有优势,在市场上价格也较高。但是自1958—1974年数次对野生大黄鱼进行掠夺式捕捞后,岱衢洋海域的野生大黄鱼几乎绝迹[3]。为了弥补资源缺失,1985年我国人工大黄鱼育苗获得成功,并于1994年进行了大规模网箱养殖。2007年宁波市开始启动岱衢族野生大黄鱼种质库建设项目,在捕获8尾亲鱼的基础上,2011年底规模化生产出岱衢族大黄鱼340万尾[4]。养殖大黄鱼因脂肪含量太高而使肉质口感与野生大黄鱼相差悬殊,在养殖过程中,投喂的饵料类型往往影响大黄鱼的品质,其中鱼体主要营养成分和体色为大黄鱼品质的重要指标,能够直接反映养殖大黄鱼的品质。国内外对大黄鱼体成分的研究已有不少报道[5, 6, 7, 8, 9],但是针对岱衢族大黄鱼的研究较为稀少。本研究拟对投喂鲜杂鱼和配合饲料的岱衢族大黄鱼的鱼体和肌肉营养成分、体色和肉色进行比较,进而比较投喂这2种饵料对岱衢族大黄鱼品质的影响。
1 材料与方法 1.1 饵料营养成分鲜杂鱼饵料以青鲇鱼为主,水分含量为80%,干物质中粗蛋白质含量为28%,粗脂肪含量为16%。配合饲料组成及营养水平见表1,饲料类型为慢沉性颗粒饲料,由青岛七好生物科技有限公司制备。
| 表1 配合饲料组成及营养水平Table 1 Composition and nutrient levels of the formulated feed |
试验鱼4月龄开始进行试验,第1组在试验期间投喂鲜杂鱼,第2组在试验期间投喂配合饲料,投喂期为22个月。试验用岱衢族大黄鱼从宁波市海洋渔业研究院位于象山的大黄鱼养殖基地捕捞后,置于冰块中运送至实验室,从捕捞到样品处理时间不超过24 h。每组各取5尾进行全鱼营养成分分析,处理前用干燥的抹布抹干鱼体表面水分后,直接用绞肉机绞碎。大部分样品自封袋装好后立即保存于-20 ℃,少量样品单独密封包装用于干物质含量测定。每组另取5尾进行肌肉营养成分分析,取样方法为沿着脊椎骨将鱼体背部两侧的肌肉组织取下,再经绞肉机绞碎。大部分样品经自封袋装好立即置于-20 ℃保存,少量样品单独密封包装用于干物质含量测定。-20 ℃保存样品置真空冷冻干燥机进行48 h冷冻干燥后密封保存于-20 ℃,直至进行营养成分测定。每组再随机取6尾鱼进行体色和肉色测定,先进行体色测定,体色测定完成之后,取背部肌肉进行肉色测定。
1.3 营养成分测定粗灰分含量按照GB/T 5009.4—2010[10]的方法进行测定,粗脂肪含量采用索氏抽提法[11]、粗蛋白质含量采用凯氏定氮法[12]、水分含量采用直接干燥法[13]进行测定,氨基酸含量采用日立L-8900氨基酸分析仪按酸水解法[14]测定。
1.4 肉色和体色测定肉色和体色采用美能达CR-4100色差仪测定,体色测定部位如图1所示,分别为前背部、后背部和腹部。肉色测定采用背部肌肉来完成。色差仪使用前用白板进行校准,测定前或过程中避免外源灯光对色差仪产生影响。测定L、a、b值这3个指标,其中L值表示亮度(L=0,表示黑;L=100,表示亮),a值表示红绿(+a表示红色;-a表示绿色),b值表示黄蓝(+b表示黄色;-b表示蓝色)。
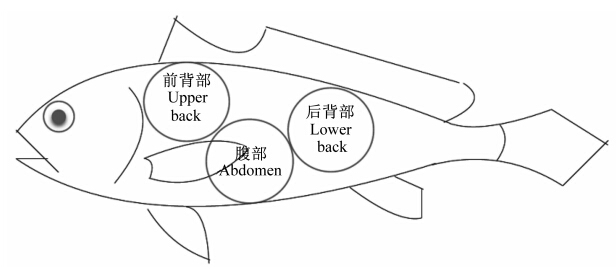 | 图1 大黄鱼体色测定部位Fig. 1 Positions of large yellow croakers for body color determination |
对于营养成分和氨基酸组成数据,以饵料类型作为因素,采用SAS 8.02软件的GLM程序进行单因素方差分析(one-way ANOVA);对于体色数据,以饵料类型和测定部位作为2个因素,采用SAS软件的GLM程序进行双因素方差分析(two-way ANOVA)。以Duncan氏法多组极差检验来验证不同组间的差异显著性,显著性水平为P<0.05,数据分析结果表示为平均值±标准误。
氨基酸评分(AAS)和化学评分(CS)按下列公式[15]进行:
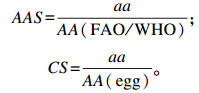
式中:aa为试验样品氨基酸含量(%,粗蛋白质基础,下同);AA(FAO/WHO)为FAO/WHO标准模式中同种氨基酸含量(%);AA(egg)为全鸡蛋蛋白质中同种氨基酸含量(%)。
2 结 果 2.1 投喂不同饵料大黄鱼的全鱼营养成分和氨基酸组成由表2可以看出,鲜杂鱼组和配合饲料组在全鱼干物质、粗蛋白质和粗灰分含量上无显著差异(P>0.05),在各氨基酸、总必需氨基酸、总呈味氨基酸和总氨基酸含量上也无显著差异(P>0.05),但是鲜杂鱼组的全鱼粗脂肪含量显著高于配合饲料组(P<0.05)。
| 表2 投喂不同饵料大黄鱼的全鱼营养成分和氨基酸组成Table 2 Nutritional components and amino acid composition of whole fish of large yellow croaker fed different diets |
全鱼的AAS和CS结果列于表3,鲜杂鱼组和配合饲料组之间各氨基酸的AAS和CS差别不大,且只有赖氨酸(Lys)的AAS大于1.00,鲜杂鱼组和配合饲料组分别为1.07和1.06,缬氨酸(Val)的AAS最低,鲜杂鱼组和配合饲料组分别为0.52和0.53。
| 表3 投喂不同饵料大黄鱼的全鱼氨基酸评分和化学评分(粗蛋白质基础)Table 3 AAS and CS of whole fish of large yellow croaker fed different diets (CP basis) |
由表4可以看出,配合饲料组的肌肉粗脂肪含量显著高于鲜杂鱼组(P<0.05),干物质和粗蛋白质含量在2组之间无显著差异(P>0.05);必需氨基酸中,配合饲料组的亮氨酸(Leu)、Lys和总必需氨基酸含量显著高于鲜杂鱼组(P<0.05);非必需氨基酸中,配合饲料组的谷氨酸(Glu)含量显著高于鲜杂鱼组(P<0.05);此外,总呈味氨基酸和总氨基酸含量也表现为配合饲料组显著高于鲜杂 鱼组(P<0.05)。
| 表4 投喂不同饵料大黄鱼的肌肉营养成分和氨基酸组成Table 4 Nutritional components and amino acid composition of muscle of large yellow croaker fed different diets |
肌肉的AAS和CS结果列于表5,配合饲料组各种氨基酸的AAS和CS均高于鲜杂鱼组,只有Lys和苯丙氨酸(Phe)+酪氨酸(Tyr)的AAS大于1.00,Val的AAS最低,鲜杂鱼组和配合饲料组分别为0.57和0.66。
| 表5 投喂不同饵料大黄鱼的肌肉氨基酸评分和化学评分(粗蛋白质基础)Table 5 AAS and CS of muscle of large yellow croaker fed different diets (CP basis) |
由表6可以看出,无论是体色还是肉色,鲜杂鱼组和配合饲料组在L、a、b值这3个指标上均无显著差异(P>0.05)。
| 表6 投喂不同饵料大黄鱼的体色和肉色Table 6 Body color and muscle color of large yellow croaker fed different diets |
大黄鱼不同部位的体色测定结果列于表7。大黄鱼腹部的L值要显著高于后背部和前背部(P<0.05),且后背部显著高于前背部(P<0.05),表明腹部颜色最亮,随后依次为后背部和前背部;大黄鱼腹部的a和b值显著高于前背部和后背部(P<0.05),表明腹部的颜色偏红黄。
| 表7 大黄鱼不同部位的体色Table 7 Body color in different positions of large yellow croaker |
本试验结果揭示配合饲料组全鱼的粗脂肪含量低于鲜杂鱼组,但是其肌肉的粗脂肪含量高于鲜杂鱼组,表明投喂配合饲料使得大黄鱼能更有效地把饵料中的油脂转化成肌肉组织中的脂肪,同时使内脏中的脂肪含量减少。有研究表明,饲料中较高的油脂含量会引起小鼠肌肉中的胰岛素抵抗作用,从而增加内脏中的脂肪含量,同时减少肌肉中的脂肪含量[18]。本试验所采用的鲜杂鱼所含有的油脂量要高于配合饲料,因此这可能是引起上述现象的原因。但由于所依据的研究以小鼠为试验动物,鉴于物种间的差异,是否大黄鱼和小鼠存在着同样的胰岛素抵抗规律需进一步的试验进行验证。
本试验所测得的全鱼粗蛋白质含量低于Tang等[19]所测得的结果,而所测得的全鱼粗脂肪含量则高于Tang等[19]所测得的结果。全鱼粗蛋白质和粗脂肪含量受多种因素影响,包括饵料成分、养殖环境、生长阶段和体重大小等,鉴于Tang等[19]的试验中缺少饵料成分和养殖环境的详细信息,因此仅能从体重大小分析产生差异的原因,本研究所采用大黄鱼平均体重为470(鲜杂鱼组)和468 g(配合饲料组),高于Tang等[19]的试验中所用大黄鱼(289和302 g),早期研究已经证实鱼体的粗蛋白质含量与体重成反比,而粗脂肪含量与体重成正比[20],本试验结果符合这一规律。
鲜杂鱼组和配合饲料组的全鱼必需氨基酸含量无显著差异,且AAS和CS指标接近,表明鲜杂鱼和配合饲料均能满足养殖岱衢族大黄鱼对必需氨基酸的需求。鲜杂鱼组和配合饲料组的AAS指标中只有Lys大于1.00(1.07 vs. 1.06),取得AAS最低值的氨基酸为Val,鲜杂鱼组和配合饲料组分别为0.52和0.53,其次为异亮氨酸(Ile),表明岱衢族大黄鱼Lys含量丰富,同时第一限制性氨基酸为Val,第二限制性氨基酸为Ile。
本试验测得的大黄鱼肌肉粗蛋白质含量若换算成湿重基础,则鲜杂鱼组和配合饲料组分别为17.1%和18.0%,粗脂肪含量换算湿重基础,则分别为6.5%和9.4%,接近吴靖娜等[21]所测得的17.4%的粗蛋白质含量,但低于其所测得的12.4%的粗脂肪含量。Tang等[19]也比较了饲喂鲜杂鱼和配合饲料对大黄鱼全鱼氨基酸组成的影响,得到了饲喂配合饲料能显著降低全鱼必需氨基酸含量的结论,但其对于肌肉氨基酸含量的影响并没有分析。本试验中,配合饲料组中肌肉总必需氨基酸含量显著高于鲜杂鱼组,表明配合饲料中的蛋白质能更好地被大黄鱼所利用。配合饲料组肌肉中各种氨基酸的AAS和CS均高于鲜杂鱼组,也表明其营养价值相对较高。Lys和Phe+Tyr的AAS均大于1.00,表明Lys、Phe+Tyr在岱衢族大黄鱼肌肉中含量较为丰富。AAS最低值出现在Val上,说明岱衢族大黄鱼肌肉中的第一限制性氨基酸为Val。
鱼类体色主要受色素细胞影响,硬骨鱼类的色素细胞可分为虹彩细胞、红色素细胞、黄色素细胞和黑色素细胞,每种细胞的结构、呈色物质和色素含量均不同,每种鱼特有的体色由不同的色素细胞组合在一起形成[22]。体色受多种因素影响,其中,饵料中所含有的类胡萝卜素直接影响着体色,本试验中所测得的鲜杂鱼组和配合饲料组大黄鱼的体色均无显著差异,表明这2种饵料对体色的影响差异不大或所含有的色素物质差异不足以影响大黄鱼体色。本试验中,投喂鲜杂鱼和配合饲料的2组大黄鱼的肉色也无显著差异,这可能是由于大黄鱼的肌肉中无色素沉积[19],从而不受饵料类型的影响。本试验结果还表明,大黄鱼体表不同部位颜色存在着显著差异,其中,与背部相比,腹部的颜色较亮,且偏红黄。Hearing[23]认为,体表含有较多的黑色素是体表颜色较暗的原因,大黄鱼背部比腹部暗,因此可推断背部比腹部含有更多的黑色素。与背部相比,腹部颜色偏红黄的原因可能是含有较多的红色素细胞和黄色素细胞。
4 结 论① 与投喂鲜杂鱼相比,投喂配合饲料显著降低了岱衢族大黄鱼全鱼的粗脂肪含量,但是提高了肌肉的粗脂肪含量,同时提高了肌肉中Leu、Lys、Glu、总必需氨基酸、总呈味氨基酸和总氨基酸的含量。
② 投喂鲜杂鱼和配合饲料对岱衢族大黄鱼体色和肉色无显著影响,但是岱衢族大黄鱼体表不同部位颜色存在着显著差异,与背部相比,腹部的颜色较浅,且偏红黄。
③ 本试验中,相较于鲜杂鱼,采用配合饲料养成的岱衢族大黄鱼肌肉具有更高的营养价值。
致谢: 感谢宁波市海洋与渔业研究院沈伟良博士在采样过程中给予的帮助。| [1] | 何志刚,艾庆辉,麦康森.大黄鱼营养需求研究研究[J]. 饲料工业,2010,31(24):56-59. ( 1) 1)
|
| [2] | 黄良敏,谢仰杰,苏永全.闽-粤东族与岱衢族养殖大黄鱼的遗传多样性研究[J]. 厦门大学学报:自然科学版,2006,45(6):836-840. ( 1) 1)
|
| [3] | 陈卫忠.东海区主要经济鱼类资源近况[J]. 海洋渔业,1994,16(4):163-165. ( 1) 1)
|
| [4] | 徐吟梅.岱衢族大黄鱼首次在宁波放流入海[J]. 现代渔业信息,2011,26(8):33. ( 1) 1)
|
| [5] | 全成干,王军,丁少雄,等.养殖大黄鱼生化组份的分析[J]. 台湾海峡,2000,19(2):197-200. ( 1) 1)
|
| [6] | 郑斌,徐君卓,刘士忠.大黄鱼肌肉和血液生化组分的分析[J]. 集美大学学报:自然科学版,2003,8(4):295-300. ( 1) 1)
|
| [7] | 段青源,钟惠英,斯列钢,等.网箱养殖大黄鱼与天然大黄鱼营养成分的比较分析[J]. 浙江海洋学院学报:自然科学版,2000,19(2):125-128. ( 1) 1)
|
| [8] | 徐继林,朱艺峰,严小军,等.养殖与野生大黄鱼肌肉脂肪酸组成的比较[J]. 营养学报,2005,27(3):256-258. ( 1) 1)
|
| [9] | 缪伏荣,刘景,王淡华,等.不同养殖模式大黄鱼肉质性状的分析研究[J]. 福建农业学报,2007,22(4):372-377. ( 1) 1)
|
| [10] | 中华人民共和国卫生部.GB/T 5009.4-2010食品中的灰分测定[S]. 北京:中国标准出版社,2010. ( 1) 1)
|
| [11] | 中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 6433-2006饲料中粗脂肪的测定[S]. 北京:中国标准出版社,2006. ( 1) 1)
|
| [12] | 中华人民共和国卫生部.GB/T 5009.5-2010 食品中的蛋白质测定[S]. 北京:中国标准出版社,2010. ( 1) 1)
|
| [13] | 中华人民共和国卫生部.GB/T 5009.3-2010食品中的水分测定[S]. 北京:中国标准出版社,2010. ( 1) 1)
|
| [14] | 国家质量技术监督局.GB/T 18246-2000饲料中氨基酸的测定[S]北京:中国标准出版社,2000. ( 1) 1)
|
| [15] | WANG Y Y,YU S L,MA G J,et al.Comparative study of proximate composition and amino acid in farmed and wild Pseudobagrus ussuriensis muscles[J]. International Journal of Food Science and Technology,2014,49:983-989. ( 1) 1)
|
| [16] | HARPER A.Amino acid scoring patterns[M/OL].HARPER A.Joint FAO/WHO/UNU expert consultation on energy and protein requirements.[M]. http://www.fao.org/docrep/MEETING/004/M3013E/M3013E00.HTM. ( 2) 2)
|
| [17] | GROPPER S S,SMITH J L.Advanced nutrition and human metabolism[M].6th ed.Stamford:Cengage Learning,2008:608. ( 2) 2)
|
| [18] | KIM J Y,NOLTE L A,HANSEN P A,et al.High-fat diet-induced muscle insulin resistance: relationship to visceral fat mass[J]. American Journal of Physiology:Regulatory,Integrative and Comparative Physiology,2000,279:2057-2065. ( 1) 1)
|
| [19] | TANG H G,WU T X,ZHAO Z H Y,et al.Biochemical composition of large yellow croaker (Pseudosciaena crocea) cultured in China[J]. Journal of Food Quality,2008,31:382-393. ( 5) 5)
|
| [20] | BROWN M L,MURPHY B R.Relationship of relative weight (Wr) to proximate composition of juvenile striped bass and hybrid striped bass[J]. Transactions of the American Fisheries Society,1991,120:509-518. ( 1) 1)
|
| [21] | 吴靖娜,许永安,刘智禹.养殖大黄鱼鱼肉营养成分的分析及评价[J]. 营养学报,2013,35(6):610-612. ( 1) 1)
|
| [22] | 易新文.饲料营养影响大黄鱼(Pseudosciaena crocea R.)体色的初步研究[D]. 硕士学位论文.青岛:中国海洋大学,2012. ( 1) 1)
|
| [23] | HEARING V J.Biogenesis of pigment granules:a sensitive way to regulate melanocyte function[J]. Journal of Dermatological Science,2005,37(1):3-14. ( 1) 1)
|



