仔猪生产是猪生产中最关键的环节,是影响养猪生产效益的重要因素。近年来,随着仔猪早期断奶技术的推广应用,对仔猪饲养管理的要求也越来越高。由于仔猪的许多机能尚不成熟,早期断奶仔猪的生长性能受到限制,常常会表现出一系列的不良现象,如厌食或拒食、消化机能紊乱、腹泻水肿、饲料利用率低和生长迟滞等,导致“仔猪早期断奶综合征”,严重影响养猪产业[1]。谷氨酰胺(glutamine,Gln)作为断奶仔猪的一种条件性氨基酸,能有效缓解早期断奶仔猪的断奶应激,但因其价格昂贵,添加量多,实际生产中将大量增加成本[2]。牛磺酸(taurine,Tau)作为一种含量丰富的游离氨基酸(FAA),具有抗氧化、调节脂类代谢、保护细胞、提高机体免疫和促进肠道发育等功能,因其价格低廉,添加量少,在猫和家禽饲粮中已有应用[3]。因此,本试验在断奶仔猪饲粮中添加Tau和Gln,研究Tau对早期断奶仔猪生长性能和肠道健康的影响及其机制,对比Tau和Gln的添加效果,从而为进一步将Tau应用于早期断奶仔猪生产实践中提供理论依据。
1 材料与方法 1.1 试验材料Tau和Gln购自上海源聚生物科技有限公司,Tau(A3820)为药用级,纯度为99.0%;Gln(A0090)纯度>98.5%。血清钙(Ca)、磷(P)、总蛋白(total protein,TP)、白蛋白(albumin,ALB)、总胆固醇(total cholesterol,TC)、甘油三酯(triglycerides,TG)、丙二醛(malondialdehyde,MDA)、一氧化氮(nitric oxide,NO)、过氧化氢酶(catalase,CAT)、碱性磷酸酶(alkaline phosphatase,AKP)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)、丙氨酸转氨酶(alanine aminotransferase,ALT)、一氧化氮合酶(nitric oxide synthase,NOS)、抗超氧阴离子(anti superoxide anion,ASA)、乳酸脱氢酶(lactate dehydrogenase,LDH)、超氧化物歧化酶(superoxide dismutase,SOD)和谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)和总抗氧化能力(total antioxidant capacity,T-AOC)测定试剂盒均购自南京建成生物工程研究所;反转录试剂盒购自生工生物工程股份有限公司;Trizol、荧光定量PCR试剂盒和SYBR Green Ⅰ均购自Invitrogen(美国)公司。
1.2 试验设计与基础饲粮试验于西南大学动物科技学院动物饲养基地进行。采用单因素完全随机设计,选择(17±2)日龄断奶、平均体重为(5.17±0.04) kg的健康荣昌内三元“(长×大)×荣昌”早期断奶仔猪30头,随机分为3个组,每组10个重复,每个重复1头猪。对照组(CON组)饲喂基础饲粮,试验组分别在基础饲粮中添加0.1% Tau(T组)和1.0% Gln(G组)。CON和T组分别添加1.218 8%和1.147 6%丙氨酸以维持氮平衡。基础饲粮组成及营养水平见表 1。试验期17 d,其中预试期3 d。
|
|
表 1 基础饲粮组成及营养水平(干物质基础) Table 1 Composition and nutrient levels of the basal diet (DM basis) |
试验在全封闭猪舍进行,试验前对猪舍进行消毒,采用单栏饲喂,饲喂干粉料,每天喂料3次,自由采食和饮水。其他饲养管理措施、驱虫及免疫接种按猪场常规程序进行。
1.3 样品采集试验期间记录耗料量和腹泻情况;分别于试验第1和15天06:00喂料前空腹称重,计算平均日增重(ADG)、平均日釆食量(ADFI)、料重比(F/G)及腹泻率(diarrhea rate)。试验第15天早晨,从每组随机抽取5头猪,前腔静脉采血10 mL,静置1 h后于3 000 r/min、4 ℃离心8 min,移取血清,置于-20 ℃保存,用于血清指标和氨基酸含量测定。采血后,屠宰取空肠中段约1 cm的肠壁2段,用0.9% NaCl溶液将其冲洗干净,贴于滤纸上展平修剪,放入10%福尔马林溶液中固定,石蜡包埋,连续切片,测定小肠绒毛高度和隐窝深度;用载玻片轻轻刮取空肠和回肠黏膜,置于液氮中冷冻,-80 ℃保存,用于相关基因相对表达量的测定。
1.4 测定指标与方法 1.4.1 生长性能和腹泻率根据以下公式计算生长性能和腹泻率:

|
按照试剂盒说明书测定血清生化、脂类和抗氧化指标。血清氨基酸样品用4%磺基水杨酸稀释2倍,于16 000 r/min离心2 min,用0.22 μm滤膜过滤,采用日立L-8800型全自动氨基酸分析仪测定血清氨基酸含量。每个样品分析周期53 min,分析时有2个柱:分离柱(4.6 mm×60 mm),洗脱液流速0.4 mL/min,柱温70 ℃,柱压10.627 MPa;反应柱,茚三酮及茚三酮缓冲液流速0.35 mL/min,柱温135 ℃,柱压0.982 MPa。
1.4.3 肠道黏膜形态结构肠道黏膜形态结构参照Wang等[4]方法进行测定,简要程序如下:从固定液中取出样品,乙醇脱水,二甲苯透明,石蜡包埋,制作5 mm厚切片,苏木精-伊红(HE)染色后显微镜下观察。利用OPTPro图像处理软件进行绒毛高度和绒毛宽度等空肠黏膜形态结构指标的测定,双盲法读片,每张切片取5个视野进行观察。
1.4.4 肠道黏膜β-连环蛋白(β-catenin)和胰岛再生源蛋白-3γ(Reg-3γ)mRNA相对表达量用Total RNA Extractor(购自上海生物工程有限公司)提取空肠和回肠黏膜总RNA,OD260 nm/OD280 nm在1.8~2.0的样品进行下一步试验,用M-MLV First Strand cDNA Synthesis Kit(购自上海生物工程有限公司)进行反转录得到cDNA。
根据GenBank中猪的甘油醛-3-磷酸脱氢酶(GAPDH)、β-catenin和Reg-3γ基因序列,取保守区域设计引物,引物由生工生物工程股份有限公司合成,引物序列见表 2。荧光定量PCR反应体系:总体积为25 μL,其中Hotstart Fluo-PCR mix 12 μL,上、下游引物各1 μL(25 μmol/L),cDNA 1 μL,ddH2O 10 μL。荧光定量PCR反应条件:94 ℃预变性4 min,94 ℃变性30 s,63 ℃退火30 s,72 ℃延伸30 s,共35个循环。每个样品设3个重复。采用比较Ct法进行相对定量表达差异的计算方法,目的基因的表达量为2-ΔΔCt,ΔΔCt=(Ct目的基因-Ct内参基因)试验组-(Ct目的基因-Ct内参基因)对照组,2-ΔΔCt表示的是试验组目的基因的表达量相对于对照组的变化倍数。
|
|
表 2 引物序列 Table 2 Sequences of primer |
试验数据用Excel 2003和SAS 9.0软件进行整理和单因素方差分析(one-way ANOVA),差异显著者采用LSD法进行多重比较。P < 0.05为差异显著。
2 结果 2.1 生长性能和腹泻率由表 3可知,与对照组相比,试验第1~7天,T和G组早期断奶仔猪的腹泻率分别降低26.08%和39.14%;试验第8~14天,腹泻率分别降低29.65%和51.84%,G组效果优于T组。
|
|
表 3 Tau对早期断奶仔猪腹泻率的影响 Table 3 Effects of taurine on diarrhea rate of early-weaned piglets |
由表 4可知,各组早期断奶仔猪的初重无显著差异(P > 0.05);T和G组的平均日增重和平均日采食量显著高于对照组(P < 0.05),G组的平均日增重和平均日采食量比T组分别提高4.11%和3.38%,但差异不显著(P > 0.05);与对照组相比,T和G组的料重比均降低13.00%,但差异不显著(P > 0.05)。
|
|
表 4 Tau对早期断奶仔猪生长性能的影响 Table 4 Effects of taurine on growth performance of early-weaned piglets |
由表 5可知,各组早期断奶仔猪的血清ALB含量、AST和AKP活性差异显著(P < 0.05);其中,T组的血清ALB含量显著高于对照组和G组(P < 0.05);与对照组相比,T和G组的血清AST活性分别降低7.51%和11.17%,差异显著(P < 0.05),G组显著低于T组(P < 0.05);T和G组的血清AKP活性显著高于对照组(P < 0.05),T和G组之间无显著差异(P > 0.05)。T组的血清Ca含量分别比对照组和G组提高24.89%和14.12%,但差异不显著(P > 0.05)。与对照组相比,T和G组的血清P含量分别降低17.85%和12.50%,但差异不显著(P > 0.05)。
|
|
表 5 Tau对早期断奶仔猪血清生化指标的影响 Table 5 Effects of taurine on serum biochemical indexes of early-weaned piglets |
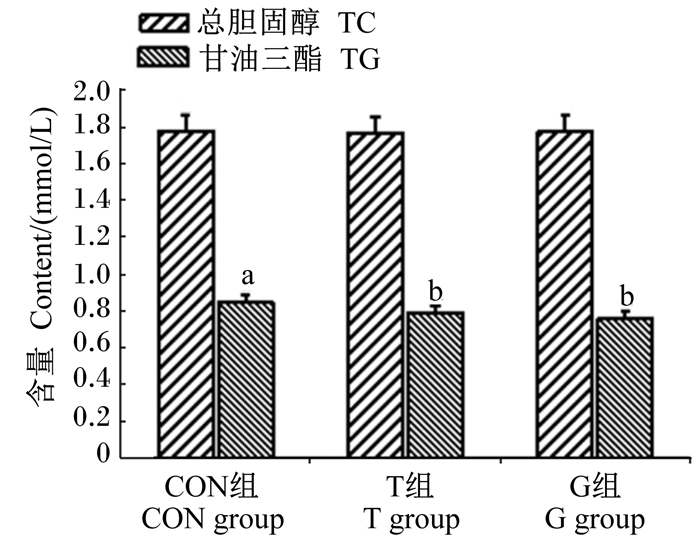
由图 1可知,各组早期断奶仔猪的血清TC含量无显著差异(P > 0.05);与对照组相比,T和G组的血清TG含量显著降低(P < 0.05),T和G组之间无显著差异(P > 0.05)。
|
数据柱标注不同小写字母表示差异显著(P < 0.05)。图 3同。 Value columns with different small letter superscripts mean significant difference (P < 0.05). The same as Fig. 3. 图 1 Tau对早期断奶仔猪血清脂类指标的影响 Figure 1 Effects of taurine on serum lipid indexes of early-weaned piglets |
由表 6可知,T组早期断奶仔猪的血清SOD活性显著高于对照组和G组(P < 0.05),G组和对照组之间无显著差异(P > 0.05);T和G组的血清CAT活性显著高于对照组(P < 0.05),G组效果最好;与对照组相比,T和G组的血清T-AOC分别提高7.37%和8.27%,NO含量分别降低8.60%和8.52%,MDA含量分别降低3.23%和5.53%,但差异均不显著(P > 0.05)。
|
|
表 6 Tau对早期断奶仔猪血清抗氧化指标的影响 Table 6 Effects of taurine on serum antioxidant indexes of early-weaned piglets |
由表 7可知,与对照组相比,除色氨酸(Try)、组氨酸(His)、异亮氨酸(Ile)、苯丙氨酸(Phe)、缬氨酸(Val)和谷氨酸(Glu)外,T和G组早期断奶仔猪的血清必需氨基酸(EAA)含量均呈升高趋势,血清非必需氨基酸(NEAA)含量均呈降低趋势。各组的血清赖氨酸(Lys)、蛋氨酸(Met)、精氨酸(Arg)、半胱氨酸(Cys)、亮氨酸(Leu)、苏氨酸(Thr)、丙氨酸(Ala)、天冬氨酸(Asp)、甘氨酸(Gly)、脯氨酸(Pro)和酪氨酸(Tyr)含量差异显著(P < 0.05)。饲粮中添加Tau对血清Lys、Met和Arg含量的提高效果显著优于Gln。
|
|
表 7 Tau对早期断奶仔猪血清氨基酸含量的影响 Table 7 Effects of taurine on serum amino acid contents of early-weaned piglets |
由表 8可知,T和G组早期断奶仔猪的空肠绒毛高度和绒毛高度/隐窝深度显著高于对照组(P < 0.05),T和G组之间差异不显著(P > 0.05);与对照组相比,T和G组的空肠隐窝深度显著降低(P < 0.05),T和G组之间差异不显著(P > 0.05)。各组的回肠绒毛高度差异不显著(P > 0.05),但与对照组相比,T和G组分别提高6.19%和6.58%。
|
|
表 8 Tau对早期断奶仔猪肠道黏膜形态结构的影响 Table 8 Effects of taurine on intestinal mucosa morphological structure of early-weaned piglets |
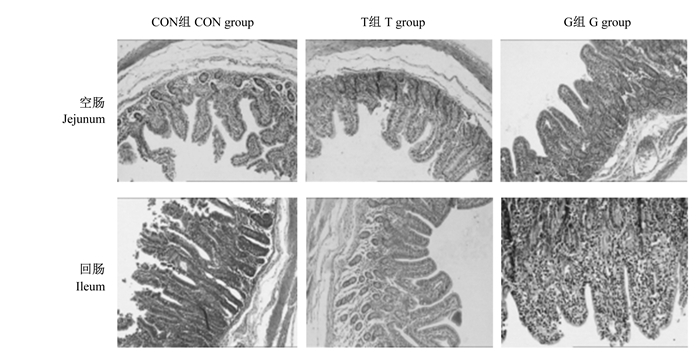
由图 2可知,早期断奶导致仔猪空肠和回肠绒毛明显变短,生理排列出现紊乱,绒毛顶端出现严重断裂,大片缺失,数量明显减少,部分细胞甚至坏死脱落形成糜烂,淋巴细胞浸润增加。与对照组相比,T和G组早期断奶仔猪的空肠和回肠绒毛排列整齐密集,轮廓清晰,断裂片段明显减少。
|
图 2 早期断奶仔猪空肠和回肠黏膜形态 Figure 2 The jejunum and ileum mucosa morphology of early-weaned piglets (40×) |
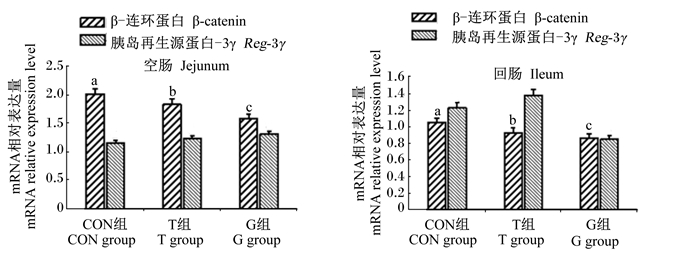
由图 3可知,各组早期断奶仔猪空肠和回肠黏膜的β-catenin mRNA相对表达量差异显著(P < 0.05);T和G组空肠和回肠黏膜的β-catenin mRNA相对表达量显著低于对照组(P < 0.05),G组最低。各组空肠和回肠黏膜的Reg-3γ mRNA相对表达量差异不显著(P > 0.05)。
|
图 3 Tau对早期断奶仔猪肠道黏膜基因mRNA相对表达量的影响 Figure 3 Effects of taurine on mRNA relative expression levels of intestinal mucosa genes of early-weaned piglets |
Liu等[5]报道断奶仔猪饲粮中添加Tau能提高其生长速度和饲料转化率。黄仁术等[6]报道饲粮中添加0.1% Tau后,断奶仔猪第1周的生长性能显著提高,其中平均日增重提高6.63%,料重比降低1.10%,经济效益增加6.14%。Zhang等[7]在断奶仔猪饲粮中添加1% Tau后发现,与对照组相比,断奶后第10天试验组的料重比降低12.05%,采食量和日增重差异不显著,但有提高趋势;断奶后第20天试验组的日增重提高27.75%。李成宝等[8]报道饲粮中添加1% Gln有降低断奶仔猪腹泻率的趋势。刘悦[9]发现在断奶仔猪饲粮中添加低剂量的Tau能显著降低断奶仔猪的腹泻频率。本试验研究结果与上述试验结果相似,Tau提高断奶仔猪生长性能及降低腹泻率的原因可能是:Tau能够降低仔猪因断奶应激引起的胃肠道损伤,增强断奶仔猪自身的免疫功能和抵抗能力;Tau以牛磺胆酸的形式促进体内脂类代谢,且能够缓解体内因断奶应激引起的氧化应激,清除体内过氧化物;Tau促进机体内铁(Fe)、铜(Cu)和锌(Zn)等微量元素的吸收,直接或间接促进机体发育。
3.2 Tau对早期断奶仔猪血清指标的影响本试验结果表明,饲粮中添加Tau提高了早期断奶仔猪的血清Ca含量,Ca含量升高可能与血清ALB含量的升高有关,因为Ca能够与血清ALB结合,机体在应激状态下胞内Ca含量升高时,血清ALB作为Ca载体,与Ca结合并将其运出胞外,维持细胞Ca平衡[10]。本试验结果发现,饲粮中添加Tau能够显著降低血清AST活性。其机制可能是Tau能提高机体的抗氧化功能,降低细胞膜脂类反应水平,从而保护细胞膜的完整性,减少AST从组织细胞逸出。动物血清中的AKP由骨髓和肝脏产生,其含量的变化可以反映出动物机体骨髓和肝脏的生理功能状况,同时也是衡量动物机体健康的重要指标之一。本试验结果表明,与对照组相比,T和G组的血清AKP活性显著升高,且与血清P含量大致呈负相关,与刘洋景[11]报道相一致。这说明Tau能在一定程度上平衡断奶仔猪的骨骼营养,抑制成骨细胞活性,获得适宜的骨骼矿化,促进骨骼生长。陈静等[12]报道,随着动物年龄的增加,血清AKP活性降低,原因可能是AKP是成骨细胞的产物,当成骨细胞变为骨细胞时,其活性就会下降。
本试验通过对TC和TG的分析来研究早期断奶仔猪体内的脂类代谢情况,得出各组的血清TC含量差异不显著,T和G组的血清TG含量显著低于对照组,说明早期断奶仔猪饲粮中添加0.1% Tau可以在一定程度上调节脂类代谢,且效果与添加1.0% Gln相当。Tau调节脂类代谢的原因可能是:Tau可促进胆酸合成过程中的限速酶7α-羟化酶的合成,通过刺激胆酸合成加速体内TC和TG的清除;Tau通过上调低密度脂蛋白胆固醇受体(low density lipoprotein-cholesterol receptor,LDLR)表达或提高与LDLR结合能力的方式降低TG含量。曾得寿等[13]研究发现,饲粮中添加Tau能显著提高21日龄肉仔鸡胰脏和小肠内容物的脂肪酶活性。高春生等[14]报道Tau能够通过提高脂肪酶的活性影响鱼体的脂类代谢。
本试验结果表明,虽然各组早期断奶仔猪的血清GSH-Px活性差异不显著,但饲粮中添加0.1% Tau显著提高血清SOD和CAT活性,MDA含量呈下降趋势。Winiarska等[15]研究表明,Tau可提高兔血清及肝脏中SOD和GSH-Px活性,提高机体的抗氧化能力,降低血清MDA含量。王芙蓉等[16]报道,Tau可降低产蛋鹌鹑血清MDA含量,说明Tau具有减少过氧化脂质(LPO)、提高机体抗氧化能力的作用。郝中禹等[17]综述,Tau能降低细胞内MDA和活性氧含量,提高SOD和GSH-Px活性,与本试验研究结果相似。本试验结果表明,饲粮中添加Tau能够降低早期断奶仔猪的血清NO含量,Tau降低血清NO含量可能与Tau抑制NOS基因表达有关。Roy等[18]报道,Tau可通过DNA的转录因子切断NOS基因表达,降低NO含量,进而抑制应激诱导的炎症反应,最终保护细胞。
本试验结果表明,Tau能够提高血清EAA中Lys、Met、Arg、Cys和Leu含量,其中Tau对血清Lys、Met和Arg含量的提高效果显著优于Gln。血清Leu和Lys含量的增加可能与血清ALB含量的增加有关,因为ALB是肝脏中合成的一种重要蛋白质,是动物营养状况的重要指标,主要由Leu和Lys等氨基酸构成,ALB含量的增加常伴随着Leu和Lys含量的增加[19]。本试验也发现Tau可使早期断奶仔猪的血清ALB含量增加。郑萍等[20]报道,氧化应激状态下,组织代谢需要更多的氨基酸,增强组织对血浆EAA的吸收,断奶仔猪血清Met、Arg和Cys含量显著降低。本试验中,早期断奶仔猪的血清Met、Arg和Cys含量增加可能是因为Tau降低了仔猪机体的氧化应激,降低了组织对血清EAA的吸收,从而增加了血清Met、Arg和Cys含量。本试验结果还发现,饲粮中添加Tau显著降低早期断奶仔猪血清NEAA中Ala、Gly和Pro含量。Ala和Gly含量降低的原因可能是仔猪在断奶应激状态下组织代谢需要更多的氨基酸,增强了组织对血清EAA的吸收,而Tau与Ala和Gly的代谢无关[21]。而Pro作为Arg的代谢产物,其在血清中的含量受Arg合成量的影响,Arg含量显著升高,导致Arg的代谢产物含量降低,Pro含量随之降低[22]。
3.3 Tau对早期断奶仔猪肠道黏膜形态的影响本试验研究发现,饲粮中添加0.1% Tau或1.0% Gln均可显著提高空肠绒毛高度和绒毛高度/隐窝深度,显著降低空肠隐窝深度,添加0.1% Tau和1.0% Gln差异不显著,回肠绒毛高度呈升高趋势,T组的小肠黏膜肠上皮结构完整性明显高于对照组,表明Tau能够缓解仔猪因早期断奶导致的肠道应激。王建军[23]报道,Tau能够明显缓解炎症引起的小鼠小肠黏膜上皮细胞绒毛脱落和坏死,炎症细胞浸润明显减少,血浆和肠组织中NO和MDA含量降低,SOD活性升高。推测Tau可能通过降低肠道氧化应激保护肠黏膜,断奶仔猪腹泻率降低可能与此存在关联。此外,Tau缓解仔猪肠道断奶应激还可能通过抑制肠道内毒素移位,促进肠道相关基因的表达,从而保护肠道的完整性[24]。
3.4 Tau对早期断奶仔猪肠道黏膜相关基因表达的影响本试验结果显示,饲粮中添加Tau和Gln能够显著降低早期断奶仔猪空肠和回肠黏膜的β-catenin mRNA相对表达量。Tau降低β-catenin mRNA相对表达量可能与Tau能够提高机体的抗氧化性有关[25]。研究表明,Tau能够提高大鼠血清和组织中SOD、CAT和GSH-Px等抗氧化物的活性,抗氧化物可清除过氧化氢(hydrogen peroxide,H2O2)[26]。田黎明[27]研究发现,β-catenin mRNA相对表达量在H2O2诱导的人成纤维细胞的氧化模型中显著提高,抑制Wnt/β-catenin信号通路能够降低机体氧化应激反应。推测Tau可能通过降低肠道H2O2含量,从而影响Wnt/β-catenin信号通路的激活,β-catenin从复合物中释放量降低,β-catenin mRNA相对表达量也随之降低。Tau还能降低免疫抑制因子肿瘤坏死因子-α(TNF-α)含量[17],补充Tau可使血液中TNF-α含量降低[28]。范正伟[29]研究发现,TNF-α通过与细胞膜上的受体结合,进入细胞基质,维持β-catenin不被降解而进入细胞核,从而激活Wnt/β-catenin信号通路。推测Tau可能通过降低肠道的TNF-α含量,从而减少对Wnt/β-catenin信号通路的激活,β-catenin mRNA相对表达量降低。
4 结论① 饲粮中添加0.1% Tau或1.0% Gln均可显著提高早期断奶仔猪的平均日增重、平均日采食量、空肠绒毛高度和绒毛高度/隐窝深度,显著降低料重比。
② 饲粮中添加0.1% Tau或1.0% Gln可提高早期断奶仔猪的血清Ca、EAA含量及AKP、SOD和CAT活性,显著降低血清TG含量和小肠黏膜β-catenin mRNA相对表达量。
③ 饲粮中添加0.1% Tau或1.0% Gln能提高早期断奶仔猪的生长性能,促进肠道发育,1.0% Gln的效果略优于0.1% Tau。
| [1] |
HUR J, LEE J H. Development of a novel live vaccine delivering enterotoxigenic Escherichia coli fimbrial antigens to prevent post-weaning diarrhea in piglets[J]. Veterinary Immunology and Immunopathology, 2012, 146(3/4): 283-288. |
| [2] |
NORDGREN A, KARLSSON T, WIKLUND L. Glutamine concentration and tissue exchange with intravenously administered α-ketoglutaric acid and ammonium:a dose-response study in the pig[J]. Nutrition, 2002, 18(6): 496-504. DOI:10.1016/S0899-9007(02)00745-1 |
| [3] |
CHAMPION E E, MANN S J, GLAZIER J D, et al. Characterisation of long term cat placental explant cultures:uptake of taurine by system β[J]. Placenta, 2005, 26(8/9): 608-616. |
| [4] |
WANG W C, GU W T, TANG X F, et al. Molecular cloning, tissue distribution and ontogenetic expression of the amino acid transporter b0, + cDNA in the small intestine of Tibetan suckling piglets[J]. Comparative Biochemistry and Physiology Part B:Biochemistry and Molecular Biology, 2009, 154(1): 157-164. DOI:10.1016/j.cbpb.2009.05.014 |
| [5] |
LIU Y, MAO X B, YU B, et al. Excessive dietary taurine supplementation reduces growth performance, liver and intestinal health of weaned pigs[J]. Livestock Science, 2014, 168: 109-119. DOI:10.1016/j.livsci.2014.08.014 |
| [6] |
黄仁术, 彭志玲, 凌明亮. 牛磺酸在断奶仔猪高动物蛋白日粮中的添加效应[J]. 中兽医医学杂志, 2008, 27(6): 30-32. |
| [7] |
ZHANG B L, YU C N, LIN M, et al. Regulation of skeletal muscle protein synthetic and degradative signaling by alanyl-glutamine in piglets challenged with Escherichia coli lipopolysaccharide[J]. Nutrition, 2015, 31(5): 749-756. DOI:10.1016/j.nut.2014.11.010 |
| [8] |
李成宝, 王雷, 张俊梅, 等. 谷氨酰胺对断奶仔猪生长性能、血液生化指标及血浆氨基酸的影响[J]. 黑龙江畜牧兽医, 2017(5): 123-125. |
| [9] |
刘悦.牛磺酸对断奶仔猪生长性能、组织病理学和肠道健康影响的研究[D].硕士学位论文.雅安: 四川农业大学, 2014. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=J0121116
|
| [10] |
LAKSHMI DEVI S, ANURADHA C V. Mitochondrial damage, cytotoxicity and apoptosis in iron-potentiated alcoholic liver fibrosis:amelioration by taurine[J]. Amino Acids, 2010, 38(3): 869-879. DOI:10.1007/s00726-009-0293-0 |
| [11] |
刘洋景.牛磺酸对笼养后备蛋鸭的作用研究[D].硕士学位论文.哈尔滨: 东北农业大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10224-1012515470.htm
|
| [12] |
陈静, 刘显军, 边连全, 等. 谷氨酰胺对早期断奶仔猪血清GPT、AKP活性的影响[J]. 中国饲料, 2006(5): 14-15. DOI:10.3969/j.issn.1004-3314.2006.05.006 |
| [13] |
曾得寿, 高振华, 黄晓亮, 等. 牛磺酸对肉仔鸡生产性能、养分利用率及脂肪酶活性的影响[J]. 畜牧与兽医, 2008, 40(9): 17-21. |
| [14] |
高春生, 范光丽, 王艳玲. 牛磺酸对黄河鲤鱼生长性能和消化酶活性的影响[J]. 中国农业通报, 2007, 23(6): 645-647. |
| [15] |
WINIARSKA K, SZYMANSKI K, GORNIAK P, et al. Hypoglycaemic, antioxidative and nephroprotective effects of taurine in alloxan diabetic rabbits[J]. Biochimie, 2009, 91(2): 266-270. |
| [16] |
王芙蓉, 佟建明, 张晓鸣, 等. 牛磺酸对鹌鹑生产性能、免疫功能及抗氧化能力的影响[J]. 食品与生物技术学报, 2011, 30(2): 190-193. |
| [17] |
郝中禹, 杨加明, 肖克权, 等. 牛磺酸的生理功能及其在猪生产中的应用[J]. 动物营养学报, 2018, 30(6): 2050-2056. DOI:10.3969/j.issn.1006-267x.2018.06.005 |
| [18] |
ROY A, SIL P C. Taurine protects murine hepatocytes against oxidative stress-induced apoptosis by tert-butyl hydroperoxide via PI3K/Akt and mitochondrial-dependent pathways[J]. Food Chemistry, 2012, 131(4): 1086-1096. DOI:10.1016/j.foodchem.2011.09.057 |
| [19] |
DAI Z L, ZHANG J, WU G Y, et al. Utilization of amino acids by bacteria from the pig small intestine[J]. Amino Acids, 2010, 39(5): 1201-1215. DOI:10.1007/s00726-010-0556-9 |
| [20] |
郑萍, 余冰, 田刚, 等. 精氨酸对氧化应激仔猪生长性能和血浆游离氨基酸浓度的影响[J]. 中国畜牧杂志, 2012, 48(21): 38-42. DOI:10.3969/j.issn.0258-7033.2012.21.011 |
| [21] |
LI X L, REZAEI R, LI P, et al. Composition of amino acids in feed ingredients for animal diets[J]. Amino Acids, 2011, 40(4): 1159-1168. DOI:10.1007/s00726-010-0740-y |
| [22] |
MURPHY J M, MURCH S J, BALL R O. Proline is synthesized from glutamate during intragastric infusion but not during intravenous infusion in neonatal piglets[J]. The Journal of Nutrition, 1996, 126(4): 878-886. DOI:10.1093/jn/126.4.878 |
| [23] |
王建军.牛磺酸对不完全性肠梗阻大鼠肠屏障保护作用的研究[D].硕士学位论文.天津: 天津医科大学, 2008. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1406901
|
| [24] |
黄春喜, 袁建敏, 周向梅. 牛磺酸对断奶小鼠小肠发育的影响[J]. 中国农业大学学报, 2014, 19(4): 129-136. |
| [25] |
PINTO D, GREGORIEFF A, BEGTHEL H, et al. Canonical Wnt signals are essential for homeostasis of the intestinal epithelium[J]. Genes & Development, 2003, 17(14): 1709-1713. |
| [26] |
周伟伟, 卜仕金. 牛磺酸对大鼠体内抗氧化系统的影响研究[J]. 中国兽药杂志, 2006, 40(8): 13-15. DOI:10.3969/j.issn.1002-1280.2006.08.004 |
| [27] |
田黎明.β-catenin抗氧化应激所致人皮肤成纤维细胞衰老的机制研究[D].博士学位论文.长沙: 中南大学, 2011. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1918256
|
| [28] |
吕秋凤, 金淑清, 胡建民, 等. 牛磺酸对大鼠血压及血管活性物质的影响[J]. 沈阳农业大学学报, 2008, 39(2): 201-204. |
| [29] |
范正伟.探讨TNF-α与Wnt/β-catenin信号通路在小鼠原代前脂肪分化过程中相互作用机制[D].硕士学位论文.济南: 山东师范大学, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10445-1013216194.htm
|




