豆渣是生产豆浆、豆腐、豆粉等豆制品的副产物。研究表明,豆渣含有丰富的营养价值,其中蛋白质含量在20%左右[1]。豆渣属于非常规饲料,非常规饲料可以代替部分常规饲料,从而有效地节约奶牛饲养成本。由于豆渣含水量较高,不易储存,造成严重的资源浪费[2]。生产上会采用烘干等方式降低豆渣等湿饲料的含水量,从而便于储存和运输[3]。对饲料进行加热往往会伴随着美拉德反应的发生,且过度加热会破坏饲料内部蛋白质分子结构,降低饲料的营养价值[4]。用传统的化学方法对饲料进行营养价值测定既费时又费力。据报道,傅里叶变换红外光谱(FTIR)技术具有操作简单、扫描快速、用量少等特点[5]。近年来,国内外学者利用FTIR技术对饲料进行检测,探究饲料内部分子结构与其营养价值的内在联系,为快速、准确地预测饲料营养价值提供了可能。Khan等[6]通过傅里叶变换衰减全反射红外光谱(ATR-FTIR)技术得出不同方式热处理荠菜籽的蛋白质分子结构与其营养价值、瘤胃降解率及小肠消化率之间存在相关关系。Li等[7]通过ATR-FTIR技术得出生物能源加工引起的双低菜籽粕和豆粕蛋白质分子结构的变化与蛋白质的营养价值密切相关,酰胺Ⅰ带与酰胺Ⅱ带的峰面积比值和α-螺旋和β-折叠的峰高比值可以准确预测饲料总可降解粗蛋白质(CP)含量,α-螺旋和β-折叠的峰高比值可以准确预测小肠总可消化蛋白质含量。生产中对豆渣进行烘干没有明确的温度和时间,温度的高低及加热时间的长短都会影响豆渣的营养价值。因此,探究适宜的热处理温度的同时寻求一种能够快速反映豆渣营养价值及消化率热损害程度的敏感指标极其重要。FTIR技术是一种能够快速、直接、不破坏各种饲料样本固有的分子结构特征的分析技术[8]。酰胺Ⅰ带和酰胺Ⅱ带主要用于蛋白质结构的研究,酰胺Ⅰ带光谱区域主要位于1 600~1 690 cm-1,酰胺Ⅱ带光谱区域主要位于1 480~1 575 cm-1,饲料蛋白质酰胺Ⅰ带和酰胺Ⅱ带与蛋白质的质量、营养价值的利用、瘤胃消化特性密切相关[9-10]。本试验的目的是探究不同程度的热处理对豆渣营养价值、干物质(DM)和CP的瘤胃有效降解参数及小肠消化率的影响,同时利用FTIR技术对不同热处理的豆渣进行扫描,探求不同热处理对豆渣中蛋白质分子结构的影响及其与营养价值、DM和CP瘤胃有效降解参数及小肠消化率之间的相关关系,以期将得到的光谱信息作为热处理中一个敏感指标,简单、快速、无破坏性的分析豆渣的热损害程度,为生产中选择适宜的热处理温度提供理论支持。
1 材料与方法 1.1 试验样品采集与处理本试验于2017年5月在哈尔滨某饲料加工厂采集新鲜湿豆渣,测定其含水量为80%,并将采集到的新鲜豆渣进行不同温度(100、115、130 ℃)和不同时间(2、4、6 h)的热处理,共计9种不同程度热处理样品。取出样品冷却后,部分样品用粉碎机粉碎过1 mm孔筛,用于常规化学成分分析;再取部分样品粉碎过2 mm孔筛,用于瘤胃降解试验;剩余样品粉碎过0.25 mm孔筛,用于光谱分析。
1.2 试验动物与饲粮试验动物选用东北农业大学阿城试验基地的3头装有永久性瘤胃瘘管的健康荷斯坦奶牛(体重600 kg左右)进行瘤胃降解试验。试验期间每日饲喂2次(08:00和16:00),自由饮水。试验动物营养需要量参照奶牛营养需要NRC(2001)[11]标准进行配制,基础饲粮组成及营养水平见表 1。
|
|
表 1 基础饲粮组成及营养水平(风干基础) Table 1 Composition and nutrient levels of the basal diet (air-dry basis) |
CP、中性洗涤不溶蛋白(NDICP)和酸性洗涤不溶蛋白(ADICP)含量采用FOSS 8400全自动凯氏定氮仪进行测定。可溶性蛋白(SCP)含量按照Krishnamoorthy等[13]的方法进行测定。非蛋白氮(NPN)含量按照Licitra等[14]的方法进行测定。利用康奈尔净碳水化合物-净蛋白质体系(CNCPS)公式[15]求出蛋白质组分中快速降解部分,即为非蛋白氮(PA)、溶于缓冲液中的真蛋白质(PB1)、中速降解蛋白质(PB2)、缓慢降解蛋白质(PB3)、不可降解蛋白质(PC)的含量。
1.3.2 瘤胃尼龙袋法参照Peng等[16]的方法,准确称取7 g样品装入已称重的尼龙袋内(10 cm×20 cm,孔径40 μm),然后用橡皮筋扎紧袋口。试验选用3头装有永久性瘤胃瘘管的健康荷斯坦奶牛。将称好的尼龙袋随机放入规格为45 cm×45 cm的瘤胃网兜中,并用90 cm长的绳子固定在瘤胃瘘管上,分别培养0、4、8、12、16、24、36、48 h,每个时间点同一瘘管牛的尼龙袋个数均是3个。将取出后的尼龙袋,与0 h时间点尼龙袋一起用冷自来水冲洗,至水澄清为止,65 ℃烘干48 h至恒重,并记录残渣与尼龙袋的总重,然后粉碎过1 mm孔筛,保存于封口袋中待测。
1.3.3 改进三步体外法测定小肠消化率参照Gargallo等[17]改进三步体外法的原理和方法,称取7 g饲料原料放入尼龙袋,经瘤胃消化12 h后(同一饲料原料同一瘘管牛4个平行,共3头牛),取出尼龙袋,清洗至水清后将尼龙袋放在0.1%甲基纤维素溶液中,37 ℃振荡培养30 min,取出尼龙袋并清洗干净,于65 ℃烘箱内烘干至恒重(48 h),为瘤胃降解残渣样品,测定CP的含量。称取1 g残渣装入尼龙袋(5 cm×10 cm),封口,将尼龙袋装入DaisyⅡ培养瓶中,最多可放入30个尼龙袋。培养瓶中为2 L含有1 g/L胃蛋白酶(P-7000,Sigma)的pH=1.9的盐酸溶液,溶液提前预热。将培养瓶放在ANKOM DaisyⅡ体外模拟发酵培养箱,39 ℃旋转培养1 h。取出尼龙袋并清洗干净,加入2 L预热的含有3 g/L胰蛋白酶(P-7545,Sigma)和50 μg/L百里香酚的0.5 mol/L磷酸盐缓冲液。并将培养瓶放在ANKOM DaisyⅡ体外模拟发酵培养箱,39 ℃旋转培养24 h。取出尼龙袋并清洗至水清,65 ℃烘箱内烘至恒重(48 h),为模拟小肠消化后的残渣样品,测定CP的含量。
1.3.4 光谱数据的采集及分析在红外烤灯照射下,以溴化钾作为背景,将2 mg干燥的样品与200 mg溴化钾混合于玛瑙研钵中,充分研磨混匀后,用红外专用压片机(型号:769YP-15A粉末压片机)压成半透明薄片。然后利用FTIR仪(型号:岛津FTIR-8400S)对样品进行扫描,扫描波段在4 000~400 cm-1,分辨率为4 cm-1,扫描次数为128次,每个样品做5个重复,收集不同热处理豆渣的蛋白质分子结构光谱图。
1.4 数据分析与计算 1.4.1 瘤胃降解特性相关参数的计算
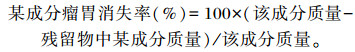
|
根据Ørskov等[18]提出的瘤胃动力学数学指数模型进行计算:
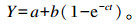
|
式中:Y为尼龙袋在瘤胃中滞留时间t后营养成分的瘤胃消失率(%);a为快速降解部(%);b为慢速降解部分(%);c为慢速降解部分的降解速率(%/h);t为瘤胃滞留时间(h),下式同。
饲料有效降解率(ED,%)的计算公式为:
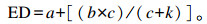
|
式中:k为瘤胃外流速率,为0.046 h-1[19]。
1.4.2 瘤胃非降解蛋白质的小肠消化率
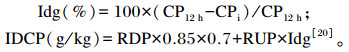
|
式中:CP12 h为瘤胃发酵后降解残渣样品中CP含量(g/kg);CPi为模拟小肠消化后残渣样品中CP含量(g/kg);Idg为瘤胃非降解蛋白质的小肠消化率(%);IDCP为小肠可消化CP含量(g/kg);RDP为瘤胃降解蛋白质含量(g/kg);RUP为瘤胃非降解蛋白质含量(g/kg)。
1.4.3 中红外光谱分析利用OMNIC 8.2软件对扫描后的样品红外光谱图进行处理和分析。先在OMNIC 8.2软件中找出蛋白质基线位置,确定出酰胺Ⅰ带区域(基线:ca.1 709~1 562 cm-1)、峰高(ca.1 635 cm-1);酰胺Ⅱ带区域(基线:ca.1 562~1 471 cm-1)、峰高(ca.1 629 cm-1),然后利用傅里叶自去卷积(FSD)和二阶导函数功能确定位于酰胺Ⅰ带中α-螺旋峰高(ca.1 655 cm-1)和β-折叠峰高(ca.1 621 cm-1)的位置,然后记录峰高和峰面积并进行统计分析。
1.4.4 数据统计与分析试验数据利用Excel 2010进行初步处理。然后采用SAS 9.4软件中的PROC MIXED程序对不同热处理豆渣的蛋白质化学成分、瘤胃降解特性、小肠消化率以及光谱数值进行数据分析。具体模型为:Yijk=u+Fi+Bj+Fi×Bj+eijk。
式中:Yijk是对自变量i、j、k的因变量;u是变量的平均值;Fi是温度效应(i=3;100、115、130 ℃);Bj是时间效应(j=3;2、4、6 h);温度与时间的交互作用Fi×Bj作为固定效应;eijk是误差效应。
Tuley-Karmaer检验用于比较不同温度和时间之间的差异,P < 0.05差异显著。再利用SAS 9.4中的PROC CORR对它们进行相关性分析(P < 0.01表示极显著相关,P < 0.05表示显著相关)。蛋白质的分子结构与其营养价值、瘤胃降解特性和小肠消化率之间的预测模型通过SAS 9.4中的PROC REG程序逐步回归。
2 结果 2.1 不同热处理对豆渣蛋白质成分和CNCPS蛋白质组分的影响由表 2可知,不同温度和时间对豆渣的蛋白质成分中SCP、NPN、NDICP含量和CNCPS蛋白质组分中PA、PB2、PB3含量均有显著影响(P < 0.05),并且2个因素之间存在显著的互作效应(P < 0.05)。在蛋白质成分中,随着温度的升高以及加热时间的延长,CP含量没有显著变化(P>0.05),SCP和NPN含量显著降低(P < 0.05),其变化范围分别为3.97% DM~5.76% DM、3.31% DM~4.70% DM。而ADICP含量呈现升高趋势(P>0.05),NDICP含量则显著升高(P < 0.05),其变化范围分别为1.01% DM~1.64% DM、5.80% DM~8.85% DM。在CNCPS蛋白质组分中,随着温度的升高以及加热时间的延长,PA和PB2含量呈现显著降低(P < 0.05),其变化范围分别为14.98% CP~20.92% CP、41.87% CP~48.56% CP。而PB3含量则显著升高(P < 0.05),PC含量呈现升高的趋势(P>0.05),其变化范围分别为21.29% CP~32.68% CP、4.50% CP~7.46% CP。
|
|
表 2 不同热处理对豆渣蛋白质成分和CNCPS蛋白质组分的影响 Table 2 Effects of different heat treatments on protein composition and CNCPS protein composition in okara |
|
|
表 5 不同热处理豆渣的蛋白质分子结构与其蛋白质成分和CNCPS蛋白质组分之间的相关关系 Table 5 Relationship between protein molecular structure and protein component, CNCPS protein component in different heat treated okara |
|
|
表 7 不同热处理豆渣的蛋白质分子结构与蛋白质营养价值之间的回归关系 Table 7 Regression relationship between protein molecular structure and protein nutritional value in different heat treated okara |
由表 3可知,经不同程度热处理豆渣的DM和CP瘤胃降解特性的差别不大。不同温度和时间对豆渣瘤胃中干物质的快速降解部分(DMa)、慢速降解部分的降解速率(DMc)含量及干物质有效降解率(DMED)有影响,并且2个因素之间存在显著的互作效应(P < 0.05)。随着温度的升高以及加热时间的延长,DMa含量和DMED显著减少(P < 0.05),其中100 ℃、2 h处理的豆渣DMa含量和DMED最高。干物质潜在可降解部分(DMd)含量和DMc显著降低(P < 0.05),其变化范围分别为96.30%~98.07%、2.95%~3.68%。而干物质的慢速降解部分(DMb)含量则呈现出升高的趋势(P> 0.05),其变化范围为89.37%~91.99%。
|
|
表 3 不同热处理对豆渣DM和CP瘤胃动态降解参数及瘤胃非降解蛋白质的影响 Table 3 Effects of different heat treatments on rumen degradation kinetics parameters of DM, CP and undegradable protein in okara |
|
|
表 6 不同热处理豆渣的蛋白质分子结构与其DM和CP瘤胃动态降解参数及瘤胃非降解蛋白质之间的相关关系 Table 6 Relationship between protein molecular structure and rumen kinetics degradation parameters of DM, CP and rumen undegraded protein in different heat treated okara |
不同温度和时间对豆渣瘤胃中粗蛋白质的快速降解部分(CPa)、小肠可消化粗蛋白质(IDCP)含量以及慢速降解部分的降解速率(CPc)有影响,并且2个因素之间存在显著的互作效应(P < 0.05)。随着温度的升高以及加热时间的延长,CPa、IDCP含量显著降低(P < 0.05),粗蛋白质有效降解率(CPED)、瘤胃非降解蛋白质的小肠消化率(Idg)呈现出降低的趋势(P>0.05)。粗蛋白质潜在可降解部分(CPd)含量呈现出降低的趋势(P>0.05),其变化范围为85.88%~88.40%。粗蛋白质的慢速降解部分(CPb)含量则呈现出升高的趋势(P>0.05),其变化范围为69.10%~72.52%。
2.3 不同热处理对豆渣蛋白质分子结构的影响由表 4可知,不同温度和时间对豆渣的蛋白质分子结构中酰胺Ⅰ带峰高、峰面积,酰胺Ⅱ带峰高、峰面积,α-螺旋、β-折叠的峰高以及α-螺旋和β-折叠的峰高比值均有影响,并且2个因素之间存在显著的互作效应(P < 0.05)。而不同温度和时间这2个因素对酰胺Ⅰ带与酰胺Ⅱ带峰面积比值、酰胺Ⅰ带与酰胺Ⅱ带峰高比值不存在互作效应(P>0.05)。随着温度的升高以及加热时间的延长,酰胺Ⅰ带峰高、峰面积,酰胺Ⅱ带峰高、峰面积,α-螺旋的峰高和β-折叠的峰高的光谱参数值显著降低(P < 0.05)。
|
|
表 4 不同热处理对豆渣蛋白质分子结构的影响 Table 4 Effects of different heat treatments on protein molecular structure in okara |
由表 5、表 6可知,不同热处理豆渣的蛋白质分子结构光谱参数与蛋白质营养价值之间存在一定的相关关系。其中,酰胺Ⅰ带峰高、峰面积,酰胺Ⅱ带峰高、峰面积,α-螺旋峰高、β-折叠峰高以及α-螺旋和β-折叠的峰高比值与CP(r=0.49~0.58,P < 0.01)、SCP(r=0.66~0.79,P < 0.01)、NPN(r=0.71~0.79,P < 0.01)、PA(r=0.71~0.78,P < 0.01)和PB2(r=0.58~0.69,P < 0.01)含量存在极显著正相关,与NDICP(r=-0.66~-0.77,P < 0.01)、ADICP(r=-0.53~-0.66,P < 0.01)、PB3(r=-0.67~-0.78,P < 0.01)、PC(r=-0.54~-0.67,P < 0.01)含量存在极显著负相关。而PB1含量(r=0.48~0.52,P < 0.05)与酰胺Ⅰ带峰高、峰面积,酰胺Ⅱ带峰高,α-螺旋峰高, β-折叠峰高存在显著正相关。
由表 6可知,酰胺Ⅰ带峰高、峰面积,酰胺Ⅱ带峰高、峰面积,α-螺旋峰高, β-折叠峰高以及α-螺旋和β-折叠的峰高比值与DMa(r=0.60~0.71,P < 0.01)、CPa(r=0.57~0.69,P < 0.01)、CPd(r=0.47~0.63,P < 0.01)含量,DMED(r=0.54~0.66,P < 0.01)、CPED(r=0.50~0.62,P < 0.01)、Idg(r=0.52~0.64,P < 0.01)及IDCP含量(r=0.57~0.70,P < 0.01)存在极显著正相关,与DMb含量(r=-0.55~-0.68,P < 0.01)存在极显著负相关。DMd含量(r=0.54~0.61,P < 0.01)与酰胺Ⅰ带峰高,酰胺Ⅱ带峰高、峰面积,α-螺旋峰高及α-螺旋和β-折叠的峰高比值存在极显著正相关。DMc(r=0.55~0.56,P < 0.01)与酰胺Ⅱ带峰高及α-螺旋峰高存在极显著正相关。CPb含量(r=-0.54~-0.59,P < 0.01)与酰胺Ⅰ带峰高、酰胺Ⅱ带峰高、α-螺旋峰高、β-折叠峰高以及α-螺旋和β-折叠的峰高比值存在极显著负相关。CPc(r=0.40~0.49,P < 0.05)与酰胺Ⅰ带峰高、峰面积,酰胺Ⅱ带峰高,α-螺旋峰高, β-折叠峰高以及α-螺旋和β-折叠的峰高比值存在显著正相关。
2.5 不同热处理豆渣的蛋白质分子结构与蛋白质营养价值之间的回归关系由表 7可知,利用FTIR技术所得多个蛋白质结构光谱参数可以作为重要参数对热处理后豆渣的蛋白质营养价值进行预测。其中,蛋白质二级结构中α-螺旋峰高作为预测因子对豆渣中CP(R2=0.33,P < 0.01)、NDICP(R2=0.60,P < 0.01)、ADICP(R2=0.43,P < 0.01)、SCP(R2=0.63,P < 0.01)、NPN(R2=0.62,P < 0.01)、PC(R2=0.44,P < 0.01)及DMb(R2=0.46,P < 0.01)含量进行预测。酰胺Ⅱ带峰高、峰面积可以共同作为预测因子估测PB2(R2=0.67,P < 0.01)、DMa(R2=0.62,P < 0.01)、CPa(R2=0.63,P < 0.01)、IDCP(R2=0.61,P < 0.01)含量以及DMc(R2=0.42,P < 0.01)、CPED(R2=0.57,P < 0.01)。DMED与酰胺Ⅰ带峰面积及酰胺Ⅱ带峰高、峰面积密切相关,拟合方程的R2为0.66。CPb含量与酰胺Ⅱ带峰面积及α-螺旋峰高密切相关,拟合方程的R2为0.46。Idg与酰胺Ⅱ带峰高、峰面积及β-折叠峰高密切相关,拟合方程的R2为0.63。
3 讨论 3.1 不同热处理对豆渣蛋白质成分和CNCPS蛋白质组分的影响美拉德反应主要指还原糖与氨基酸、蛋白质之间的复杂反应,多发生于食品和饲料的加工和储存过程中。影响美拉德反应的主要因素是温度和时间,并且随着温度升高或加热时间的延长,美拉德反应的程度越深[21]。根据Mckinnon等[22]的研究,加热对菜籽粕CP含量没有显著影响,却使SCP含量减少,NDICP、ADICP含量增加,ADICP含量的增加表明热损伤蛋白增多。本试验中随着温度的升高以及加热时间的延长,CP含量没有呈现出显著的变化趋势,NDICP和ADICP含量显著增加,SCP含量显著减少,与Mckinnon等[22]结论一致。在CNCPS蛋白质组分中,PC含量一般与木质素、单宁和热损伤蛋白质有关,这部分蛋白在瘤胃中不易被消化[15]。本试验研究表明,随着温度的升高以及加热时间的延长,豆渣中PB2含量显著降低,PB3和PC含量显著升高,会使豆渣在瘤胃中的降解率降低。
3.2 不同热处理对豆渣DM和CP瘤胃动态降解参数及瘤胃非降解蛋白质的影响研究表明,不同热处理程度会影响DM和CP的瘤胃降解特性[22-23]。加热导致豆渣中营养物质发生改变,从而导致DM和CP瘤胃有效动态降解参数也发生改变。由于加热发生美拉德反应使DM和CP的快速降解部分转化成慢速降解部分及不可降解部分, 且粗蛋白质不可降解部分与热损伤蛋白有关,热损伤蛋白质含量越高说明热损伤程度越深,不可降解部分的含量越高。加热使中性洗涤纤维与真蛋白质结合生成NDICP,从而降低CPED[22]。本试验得出加热会显著降低豆渣DMED和CPED,与Mckinnon等[22]、Arieli等[24]的研究结果一致。加热时发生的美拉德反应使CPED降低,瘤胃PC含量增加,进而到小肠中消化,但是过度加热会使饲料中Idg降低,使IDCP含量也降低[25]。本试验中,过度加热使Idg显著降低,与前人研究结果[22]一致。所以,合理的热处理对保护饲料蛋白质的营养价值和利用具有重要意义。
3.3 不同热处理对豆渣蛋白质分子结构的影响酰胺Ⅰ带和酰胺Ⅱ带是蛋白质谱带中最主要的2个谱带,酰胺Ⅰ带区域主要由80% C=O伸缩振动组成,酰胺Ⅱ带主要由60% N-H弯曲振动和40%C-N伸缩振动组成[9],酰胺Ⅰ带中出现的最典型的蛋白质二级结构是α-螺旋和β-折叠。饲料中蛋白质的营养价值与其蛋白质内部分子结构密切相关,而且蛋白质分子结构特点会反映饲料中蛋白质的利用价值[26-27]。热处理引起饲料内部蛋白质的分子结构变化(如酰胺Ⅰ带与酰胺Ⅱ带的峰面积比值和α-螺旋和β-折叠的峰高比值)改变蛋白质溶解度以及奶牛胃肠道微生物和蛋白质水解酶对蛋白质分子结构的利用,从而影响粗蛋白质的瘤胃降解率和小肠消化率[16]。在Samadi等[28]的研究中发现,干热(120 ℃、1 h)和湿热(120 ℃、1 h)处理仅对油菜籽α-螺旋和β-折叠的峰高比值有显著影响。Peng等[16]对荠菜籽进行干热和湿热处理发现,与对照组相比,湿热法使α-螺旋峰高、α-螺旋和β-折叠的峰高比值减少,干热法使α-螺旋峰高增加,而对α-螺旋和β-折叠的峰高比值没有显著影响。干热和湿热法对蛋白质酰胺Ⅰ带面积、酰胺Ⅱ带面积及β-折叠峰高均没有显著影响。湿热法比干热法能显著改变蛋白质分子结构、粗蛋白质瘤胃降解率和小肠消化率,且湿热法提高了饲料蛋白质的利用率。本试验发现随着温度的升高以及加热时间的延长,豆渣蛋白质酰胺Ⅰ带峰高、峰面积,酰胺Ⅱ带峰高、峰面积,α-螺旋的峰高和β-折叠的峰高显著降低。这说明饲料不同以及对饲料热处理的方式和程度不同导致饲料中蛋白质分子结构的变化存在差异。由此可见,研究蛋白质分子结构,对了解饲料的营养价值及其在瘤胃中的消化利用情况尤为重要。
3.4 不同热处理豆渣的蛋白质分子结构与蛋白质营养价值之间的相关关系根据报道, 蛋白质酰胺Ⅰ带与酰胺Ⅱ带与饲料的蛋白质营养价值和瘤胃降解特性存在相关关系,可以利用蛋白质光谱参数对饲料蛋白质的营养价值及瘤胃降解特性进行估测[29]。在李欣新[10]的研究中发现,酰胺Ⅰ带峰高、酰胺Ⅱ带峰高、α-螺旋峰高和β-折叠峰高与CP存在显著正相关,与ADICP、NDICP存在显著负相关,与本试验结果一致。本试验中酰胺Ⅰ带峰高、酰胺Ⅱ带峰高、α-螺旋峰高和β-折叠峰高与CNCPS蛋白质组分中PB1含量存在显著正相关,与PC含量存在显著负相关,Li等[7]得出了与本试验相同的结论。王晓帆等[30]在研究玉米青贮蛋白质分子结构与其瘤胃降解特性的关系中得出,α-螺旋和β-折叠的峰高比值与DMc、CPc和CPED之间存在显著正相关,与本试验结果一致。Khan等[6]用不同方式热处理荠菜籽中也证实了α-螺旋和β-折叠的峰高比值与CP、SCP、PA、PB1、CPa、IDCP含量及CPED之间存在显著正相关,与NDICP、PB3及CPb含量之间存在显著负相关,但是α-螺旋和β-折叠的峰高比值与NPN、ADICP及PC含量没有相关性,与PB2含量呈负相关,结果与本试验存在差异。原因可能是饲料热处理的方式不同导致饲料中蛋白质分子结构的不同,使蛋白质分子结构与其营养价值之间的相关性存在差异。上述试验结果说明蛋白质二级结构(α-螺旋和β-折叠)及其比例与饲料蛋白质的营养价值关系更为密切,能够对其营养价值进行更精准的预测。因此,利用光谱参数反映饲料在加热过程中营养成分和瘤胃降解情况的变化具有十分重要的意义,并且通过回归方程预测其营养价值是可行的。
4 结论① 不同程度热处理对豆渣的蛋白质分子结构、营养价值、瘤胃降解参数及小肠消化率均有影响。温度越高,豆渣的营养价值越低,在实际生产中应该选择较低的温度对饲料进行加热。
② 不同程度热处理豆渣的蛋白质分子结构光谱参数与其营养价值、DM和CP瘤胃降解特性及小肠消化率之间存在相关关系,并根据相关关系构建出回归方程。初步证明,通过FTIR技术得到的光谱信息可以作为热处理中一个敏感指标对豆渣的热损害程度进行简单、快速、无破坏性的分析。
| [1] |
陈晓柯, 常虹, 郭卫芸, 等. 豆渣的综合利用现状及其研究进展[J]. 河南农业科学, 2015, 44(12): 1-5. |
| [2] |
张永根, 薛世崇, 李洋, 等. 固态发酵豆渣生产反刍动物饲料工艺条件研究[J]. 东北农业大学学报, 2016, 47(5): 76-82. DOI:10.3969/j.issn.1005-9369.2016.05.011 |
| [3] |
张文佳.产朊假丝酵母和白地霉混合固态发酵豆渣生产反刍动物饲料的研究[D].硕士学位论文.哈尔滨: 东北农业大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10224-1015396959.htm
|
| [4] |
GONZÁLEZ-VEGA J C, KIM B G, HTOO J K, 等. 热处理豆粕饲喂生长猪的氨基酸消化率[J]. 中国饲料, 2015(24): 32-37. |
| [5] |
赵秀琴. 中红外光谱分析技术及研究进展[J]. 安庆师范学院学报(自然科学版), 2012, 18(4): 94-97. |
| [6] |
KHAN N A, PENG Q, XIN H, et al. Vibrational spectroscopic investigation of heat-induced changes in functional groups related to protein structural conformation in camelina seeds and their relationship to digestion in dairy cows[J]. Animal Production Science, 2014, 55(2): 201-206. |
| [7] |
LI X X, ZHANG Y G, YU P Q. Association of bio-energy processing-induced protein molecular structure changes with CNCPS-based protein degradation and digestion of co-products in dairy cows[J]. Journal of Agricultural and Food Chemistry, 2016, 64(20): 4086-4094. DOI:10.1021/acs.jafc.6b00688 |
| [8] |
XIN H S, DING X, ZHANG L Y, et al. Investigation of the spectroscopic information on functional groups related to carbohydrates in different morphological fractions of corn stover and their relationship to nutrient supply and biodegradation characteristics[J]. Journal of Agricultural and Food Chemistry, 2017, 65(20): 4035-4043. DOI:10.1021/acs.jafc.7b00231 |
| [9] |
CARBONARO M, NUCARA A. Secondary structure of food proteins by Fourier transform spectroscopy in the mid-infrared region[J]. Amino Acids, 2010, 38(3): 679-690. DOI:10.1007/s00726-009-0274-3 |
| [10] |
李欣新.双低菜粕和豆粕分子结构与营养特性和奶牛生产性能的关系[D].博士学位论文.哈尔滨: 东北农业大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10224-1017046885.htm
|
| [11] |
NRC. Nutrient requirements of dairy cattle[M]. 7th ed. Washington, D.C.: National Academy Press, 2001.
|
| [12] |
(美)国家科学研究委员会组织.奶牛营养需要[M].孟庆翔译.北京: 中国农业大学出版社, 2002.
|
| [13] |
KRISHNAMOORTHY U, SNIFFEN C J, STERN M D, et al. Evaluation of a mathematical model of rumen digestion and an in vitro simulation of rumen proteolysis to estimate the rumen-undegraded nitrogen content of feedstuffs[J]. British Journal of Nutrition, 1983, 50(3): 555-568. DOI:10.1079/BJN19830127 |
| [14] |
LICITRA G, HERNANDEZ T M, VAN SOEST P J. Standardization of procedures for nitrogen fractionation of ruminant feeds[J]. Animal Feed and Technology, 1996, 57(4): 347-358. DOI:10.1016/0377-8401(95)00837-3 |
| [15] |
SNIFFEN C J, O'CONNOR J D, VAN SOEST P J, et al. A net carbohydrate and protein system for evaluating cattle diets:Ⅱ.Carbohydrate and protein availability[J]. Journal of Animal Science, 1992, 70(11): 3562-3577. DOI:10.2527/1992.70113562x |
| [16] |
PENG Q H, KHAN N A, WANG Z S, et al. Moist and dry heating-induced changes in protein molecular structure, protein subfractions, and nutrient profiles in camelina seeds[J]. Journal of Dairy Science, 2014, 97(1): 446-457. DOI:10.3168/jds.2013-7298 |
| [17] |
GARGALLO S, CALSAMIGLIA S, FERRET A. Technical note:a modified three-step in vitro procedure to determine intestinal digestion of proteins[J]. Journal of Animal Science, 2006, 84(8): 2163-2167. DOI:10.2527/jas.2004-704 |
| [18] |
ØRSKOV E R, MCDONALD I. The estimation of protein degradability in the rumen from incubation measurements weighted according to rate of passage[J]. Journal of Agricultural Science, 1979, 92(2): 499-503. DOI:10.1017/S0021859600063048 |
| [19] |
高红, 郝小燕, 张广宁, 等. 应用体外产气法和尼龙袋法评价几种粮食加工副产物的营养价值[J]. 中国饲料, 2017(7): 14-19. |
| [20] |
赵连生, 牛俊丽, 徐元君, 等. 6种饲料原料瘤胃降解特性和瘤胃非降解蛋白质的小肠消化率[J]. 动物营养学报, 2017, 29(6): 2038-2046. DOI:10.3969/j.issn.1006-267x.2017.06.025 |
| [21] |
JAEGER H, JANOSITZ A, KNORR D. The Maillard reaction and its control during food processing.The potential of emerging technologies[J]. Pathologie Biologie, 2010, 58(3): 207-213. DOI:10.1016/j.patbio.2009.09.016 |
| [22] |
MCKINNON J J, OLUBOBOKUN J A, MUSTAFA A, et al. Influence of dry heat treatment of canola meal on site and extent of nutrient disappearance in ruminants[J]. Animal Feed Science and Technology, 1995, 56(3/4): 243-252. |
| [23] |
MCKINNON J J, OLUBOBOKUN J A, CHRISTENSEN D A, et al. The influence of heat and chemical treatment on ruminal disappearance of canola meal[J]. Canadian Journal of Animal Science, 1991, 71(3): 773-780. DOI:10.4141/cjas91-092 |
| [24] |
ARIELI A, BEN-MOSHE A, ZAMWEL S, et al. In situ evaluation of the ruminal and intestinal digestibility of heat-treated whole cottonseeds[J]. Journal of Dairy Science, 1989, 72(5): 1228-1233. DOI:10.3168/jds.S0022-0302(89)79227-4 |
| [25] |
王潍波, 赵国琦. 温度对糖处理大豆粕干物质消失率的影响[J]. 广东饲料, 2008, 17(8): 23-25. DOI:10.3969/j.issn.1005-8613.2008.08.007 |
| [26] |
YU P. Application of Advanced synchrotron radiation-based fourier transform infrared (SR-FTIR) microspectroscopy to animal nutrition and feed science:a novel approach[J]. British Journal of Nutrition, 2004, 92(6): 869-885. DOI:10.1079/BJN20041298 |
| [27] |
YU P Q, MCKINNON J J, CHRISTENSENC R, et al. Using synchrotron-based FTIR microspectroscopy to reveal chemical features of feather protein secondary structure:comparison with other feed protein sources[J]. Journal of Agricultural and Food Chemistry, 2004, 52(24): 7353-7361. DOI:10.1021/jf0490955 |
| [28] |
SAMADI, THEODORIDOU K, YU P Q. Detect the sensitivity and response of protein molecular structure of whole canola seed (yellow and brown) to different heat processing methods and relation to protein utilization and availability using ATR-FT/IR molecular spectroscopy with chemometrics[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2013, 105: 304-313. DOI:10.1016/j.saa.2012.11.096 |
| [29] |
XIN H S, YU P Q. Detect changes in protein structure of carinata meal during rumen fermentation in relation to basic chemical profile and comparison with canola meal using ATR-FT/IR molecular spectroscopy with chemometrics[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2013, 112: 318-325. DOI:10.1016/j.saa.2013.04.073 |
| [30] |
王晓帆, 张幸怡, 郝小燕, 等. 玉米青贮瘤胃降解特性与蛋白质分子结构的关系[J]. 动物营养学报, 2016, 28(6): 1924-1934. DOI:10.3969/j.issn.1006-267x.2016.06.036 |




