在许多国家,全株玉米青贮饲料是反刍动物饲粮中必不可少的组成部分,尤其是在我国,青贮玉米的种植面积达到玉米总种植面积的15%~20%,高达400万hm2左右。全株玉米青贮营养丰富、适口性好、易消化且保存期长,可增加奶牛产奶量,同时可实现一年四季均衡供应,保障奶业健康快速可持续发展[1-3]。研究表明,全株玉米青贮的品质不仅受玉米品种特性、收获时期、留茬高度和青贮前干物质(DM)含量直接影响[4],还与压实度、密封性以及青贮后管理等因素密切相关,其中,青贮密度对有机物的氧化有较大影响[5],同时其作为一个关键的参数影响着DM的保存[6]。生产中,规模化牧场在青贮制作过程中通常采用大型机械进行填装、压实作业,但青贮窖高度、容量、机械重量以及压实次序等因素均会影响青贮饲料的紧实度,同时难以量化装填密度,缺乏可供参考的适宜范围,尤其是对整窖青贮而言,随着装填深度的增加,上层、中层、下层的密度以及渗出液损失会有极大不同,从而导致产量和营养价值的不同[7-8]。此外,虽然在青贮装窖过程中采用重型压实机压实,但大部分牧场使用青贮黑白膜或者塑料薄膜进行封窖,只有极少数牧场采用隔氧膜密封,导致青贮窖表层物料因透气产生不同程度的变质。在青贮制作过程中,诸多因素均会导致窖内不同深度青贮品质的不同,且青贮质量的稳定是影响奶牛全混合日粮(TMR)一致性最重要的因素。本试验通过九点取样法采集黑龙江地区6家牧场大型青贮窖青贮样品,以上层、中层、下层为切入点,分析不同深度全株玉米青贮常规营养价值、发酵品质以及奶牛瘤胃降解率的差异, 旨在从牧场大型青贮窖青贮制作的实际操作角度出发,为合理生产和利用全株玉米青贮提供理论支持和实践指导。
1 材料与方法 1.1 试验材料全株玉米青贮样品采集于黑龙江地区牧场内大型青贮窖(n=6),青贮窖的规模见表 1。全株玉米青贮原料收割于籽粒乳熟后期至蜡熟前期,即1/3~3/4乳线阶段,其水分含量为65%~70%。青贮完成后,根据表 1中各青贮窖及物料堆放高度,自下而上平均分为3部分,其中由窖底至整体高度33.33%为下层,由33.33%至66.66%为中层,由66.66%至窖顶为上层。参照GB/T 14699.1—2005《饲料采样》[9],利用九点法采集样品,均匀混合,进行后续分析。
|
|
表 1 全株玉米青贮窖规模 Table 1 Scale of whole plant corn silage silo |
本试验采用单因素试验设计,设置上层、中层和下层3个组别。6家规模化牧场全株玉米青贮原料均由青贮收割机采集,切割长度为1.5 cm,采用重型推土机装填、压窖,利用黑白膜封窖,贮藏45 d后开封进行样品采集,用于后续指标测定。
1.3 常规营养价值评定青贮样品DM、粗蛋白质(CP)、粗脂肪(EE)、粗灰分等常规营养含量按照AOAC(2005)[10]方法进行分析;中性洗涤纤维(NDF)、酸性洗涤纤维(ADF)含量依照Van Soest分析体系中提供的方法采用纤维分析仪(ANKOM Fiber Analyzer,美国)进行测定[11];淀粉含量采用淀粉葡萄糖苷酶/α-淀粉酶方法进行测定,试剂盒(Megazyme K-TSTA,爱尔兰)采购自Megazyme公司;酸性洗涤不溶蛋白质(ADICP)含量测定方法为将测定ADF含量后剩余样品袋剪碎,无损移入CP消解管底部,进行消化和凯氏定氮,操作步骤同CP含量测定。
1.4 发酵指标测定取10 g新鲜样品,加入90 mL去离子水,充分混匀后于4 ℃下浸提24 h,通过4层纱布过滤,所得液体一部分采用Sartorius PB-10型酸度计(赛多利斯科学仪器北京有限公司)测定pH;另一部分用于氨态氮(NH3-N)、乙酸(AA)、丙酸(PA)、丁酸(BA)和乳酸(LA)含量测定。NH3-N含量采用苯酚-次氯酸钠比色法测定[12];AA、PA和BA含量采用气相色谱法(气相色谱仪为岛津GC-2010)测定[13];LA含量采用高效液相色谱法(液相色谱仪Waters-600)测定[14]。
1.5 微生物数量测定微生物数量采用平板计数法进行测定。取新鲜样品10 g无菌操作加入90 mL灭菌生理盐水中,充分振摇后,10倍系列稀释,制作10-1~10-5稀释度的菌悬液。乳酸菌、酵母菌和霉菌分别利用乳酸细菌培养基、马铃薯葡萄糖琼脂培养基和高盐察氏培养基进行培养。选择2~3个适宜稀释度的样品匀液,每个平皿加入100 μL,每个稀释度做3个平行。培养一段时间后,记录稀释倍数和相应菌落数,每个平板上的菌落数量在30~300个之间为有效,以菌落形成单位(CFU)表示[15-16]。以上培养基均在121 ℃灭菌20 min。
1.6 瘤胃降解率测定 1.6.1 试验动物及饲养管理2头安装永久性瘤胃瘘管的荷斯坦奶牛,体重(650±20) kg,每日饲喂2次(07:00和18:00),自由饮水。试验饲粮为裹包TMR,配方按照奶牛饲养标准配制,其组成及营养水平见表 2。
|
|
表 2 试验饲粮组成及营养水平(干物质基础) Table 2 Composition and nutrient levels of the experimental diet (DM basis) |
称取5 g粉碎经1 mm筛的全株玉米青贮风干样品,放入孔径为50 μm,长×宽为12 cm×8 cm的尼龙袋内,袋口用尼龙绳绑好。每4个袋夹在1根半软塑料管上,并用尼龙绳扎好。每头牛每个时间点设2个平行。晨饲前投入试验动物瘤胃中,分别于体内培养7、24、30和48 h后取出,于自来水下细流冲洗,直至尼龙袋中流出的水清澈明亮、无味为止。65 ℃烘干至恒重, 分别测定7 h淀粉含量以及24、30和48 h的DM、CP和NDF含量。方法同常规营养评定指标测定方法,并计算相应瘤胃降解率。
1.7 数据处理及统计分析采用SAS 9.2统计软件中的ANOVA过程进行单因素方差分析,平均值采用Duncan氏法进行多重比较,P < 0.05为差异显著。
应用Fzuuy数学中隶属函数法进行青贮发酵品质以及微生物数量的综合评判。其中,与发酵品质呈正相关的指标(淀粉、乳酸含量及乳酸菌数量)采用以下公式计算:
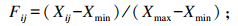
|
与发酵品质呈负相关的指标(pH、氨态氮、乙酸含量及酵母菌和霉菌数量)采用以下公式计算:
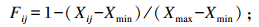
|
式中:Fij为第i个处理第j个指标的隶属度;Xij为第i个处理第j个指标测定值;Xmax、Xmin分别为所有供试对象中第j项指标的最大值、最小值。
2 结果与分析 2.1 青贮窖内不同深度全株玉米青贮的营养成分含量由表 3可知,青贮窖内不同深度的全株玉米青贮DM、NDF、ADF及淀粉含量均随青贮窖深度的增加而下降,但各营养成分含量差异均不显著(P > 0.05)。
|
|
表 3 青贮窖内不同深度全株玉米青贮的营养成分含量(风干基础) Table 3 Nutrient contents of whole plant corn silage at different depths in silage silo (air-dry basis) |
由表 4可知,青贮窖内,上层全株玉米青贮的pH最高,下层其次,中层最低,且上层分别与中层、下层存在显著性差异(P < 0.05),但中层和下层间差异不显著(P > 0.05);对于青贮窖内不同深度的全株玉米青贮的氨态氮/总氮,上层最高,且显著高于中层和下层(P < 0.05),但中层和下层间差异不显著(P > 0.05)。
|
|
表 4 青贮窖内不同深度全株玉米青贮的pH和氨态氮/总氮 Table 4 pH and NH3-N/total nitrogen of whole plant corn silage at different depths in silage silo |
由表 5可知,对于青贮窖内不同深度乳酸含量,中层最高,下层其次,上层最低,但各层间乳酸含量差异不显著(P > 0.05);对于不同深度的乙酸含量而言,上层最高,中层其次,下层最低,但各层间乙酸含量差异不显著(P > 0.05);对于乳酸/乙酸而言,各层间差异均不显著(P > 0.05);各层中均未检测到丁酸。
|
|
表 5 青贮窖内不同深度全株玉米青贮的有机酸含量(风干基础) Table 5 Organic acid contents of whole plant corn silage at different depths in silage silo (air-dry basis) |
由表 6可知,青贮窖中层全株玉米青贮中的乳酸菌数量最多,下层其次,上层最少,且上层乳酸菌数量显著低于中层、下层菌数量(P < 0.05),中层和下层间差异不显著(P > 0.05)。而青贮窖中酵母菌和霉菌数量的结果则与乳酸菌数量相反,上层最多,中层其次,下层的最少,且上层的酵母菌、霉菌数量均与中层、下层存在显著性差异(P < 0.05),但中层和下层间的酵母菌和霉菌数量差异不显著(P > 0.05)。
|
|
表 6 青贮窖内不同深度全株玉米青贮的微生物数量比较 Table 6 Comparisons of microbial population of whole plant corn silage at different depths in silage silo |
采用模糊数学隶属函数值法,以pH、淀粉、乳酸、乙酸、氨态氮含量及乳酸菌、酵母菌和霉菌数量这8个指标对青贮窖内不同深度的全株玉米青贮发酵品质及微生物数量进行综合评价。综合评价分值越高,代表全株玉米青贮的品质越好,反之越差。由表 7可知,青贮窖中层的全株玉米青贮的综合评价值最高,下层其次,上层最低。
|
|
表 7 青贮窖内不同深度全株玉米青贮发酵品质及微生物数量的隶属函数分析 Table 7 Analysis of membership function of fermentation quality and microbial population of whole plant corn silage at different depths in silage silo |
由表 8可知,青贮窖不同深度全株玉米青贮的DMD,在24、30和48 h时表现出相近的规律,主要表现为上层DMD最小,下层居中,中层最大,但随着降解时间的延长,不同深度全株玉米青贮的DMD变化幅度不同,其中在24 h时,各层间差异均不显著(P > 0.05),但达到30 h后,中层全株玉米青贮DMD显著高于上层(P < 0.05),但与下层差异不显著(P > 0.05)。对于NDFD,在24和30 h时,各层间全株玉米青贮的NDFD差异均不显著(P > 0.05),但在奶牛瘤胃内降解48 h后,中层和下层全株玉米青贮的NDFD均显著高于上层(P < 0.05),但中层和下层间差异不显著(P > 0.05)。对于CPD,在3个时间点各层间均无显著性差异(P > 0.05)。
|
|
表 8 青贮窖内不同深度全株玉米青贮瘤胃降解率(风干基础) Table 8 Rumen degradation rate of whole plant corn silage at different depths in silage silo (air-dry basis) |
本试验全株玉米青贮样品采集于黑龙江省齐齐哈尔地区的6家规模化牧场,虽然玉米种植地等自然因素会导致其营养水平产生一定的差异,但青贮收割时间、粉碎粒度、压窖方式等青贮制作工艺保持一致,使青贮前全株玉米原料的各营养水平之间无显著性差异。青贮制作过程中,随着重型机械挤压,上层物料的浸出液会流向下层,随着深度的增加,所流经的浸出液更多,因而导致下层DM损失更大。淀粉含量是评价全株玉米青贮饲料最重要的指标之一,在本试验中,上层淀粉含量高于下层,主要原因是随着装填高度升高,浸出液流失增大,青贮原料中能够被水溶解的淀粉等营养物质随着水分的下行从青贮窖底部流出,由于水分下行过程中不但把开始下行时所溶解的物质带走,而且在下行过程中还要带走其他深度的可溶物质,此外由于青贮窖中深度越深,发酵效果越好,微生物利用淀粉含量越高,最终使淀粉含量随青贮窖内深度增加呈逐步减少的现象,该结果与闫贵龙等[8]的结果相同。对于青贮窖内不同深度全株玉米青贮的CP和粗灰分含量无显著差异,可能是因为乳酸菌发酵对该指标不会产生显著性影响,且在风干基础条件下测定,避免了全株玉米青贮的浸出液中可溶性物质产生的影响,这与闫贵龙等[7]的研究结果一致。
3.2 青贮窖内不同深度全株玉米青贮的发酵品质及微生物数量综合评价青贮窖中深度越深,紧实度越高,氧气含量越低,乳酸菌增殖速度越快,因而发酵效果更好。在本试验中,中层、下层的pH较上层更低,且达到了显著水平,但中层和下层的pH之间无显著性差异,说明当压实密度达到一定时,发酵效果趋于稳定,这一结果与王旭哲等[18]研究结果相同。对于青贮窖不同深度的全株玉米青贮,上层氨态氮/总氮最高,与中层、下层间存在显著性差异,由于上层紧实度较中层、下层的紧实度小,氧气含量较高,发酵效果没有中层、下层效果好,有更多的好氧菌活动,因而上层产生较高的蛋白质分解量。全株玉米青贮中乙酸除了可直接反映青贮饲料品质有氧稳定性及保存性能,其生成量还与青贮饲料品质呈负相关[19],结果显示,随着青贮窖深度的增加,乙酸含量逐渐下降,说明下层全株玉米青贮的发酵品质优于上层;青贮窖中不同深度的全株玉米青贮样品中均未检测到丁酸,说明发酵效果良好。中层、下层乳酸菌数量显著高于上层,酵母菌和霉菌的数量也显著低于上层,表明中层、下层的发酵效果更好,主要是由于中层、下层的全株玉米在青贮制作过程中其紧实度高,氧气含量低,有利于乳酸菌快速成为优势菌群,使pH快速下降,抑制霉菌等微生物活动。
通过对不同深度全株玉米青贮发酵品质及微生物数量的隶属函数分析,可知中层的综合评价值最高,其整体发酵效果最好,下层其次,上层最低,发酵效果较差。因而通过本试验研究,在青贮窖中层、下层的全株玉米青贮发酵效果较好,上层的全株玉米青贮发酵效果较差。
3.3 青贮窖内不同深度全株玉米青贮瘤胃降解特性报道指出,青贮发酵有利于提高玉米秸秆的瘤胃降解率[20]。在本试验中,瘤胃降解30 h后,青贮窖中层全株玉米青贮的DMD显著高于上层,但与下层差异不显著,说明中层、下层发酵效果较好,可能是由于上层氧气含量较中层、下层高,影响其发酵品质,进而影响其DMD,该结果与闫贵龙等[7]的研究结果一致。对于青贮窖不同深度的全株玉米青贮的CPD在瘤胃内降解24、30和48 h后,差异均不显著,主要是因为全株玉米青贮中CP含量相对较低,乳酸菌发酵对该指标没有直接影响,且CP属于快速降解部分,因而上层、中层和下层的CPD差异不显著。研究认为,全株玉米青贮24、30和48 h的NDFD可作为其生物评价相关指标,因而在本试验中测定了上述3个关键时间点NDFD[21-23],结果表明全株玉米青贮在瘤胃内降解24 h后,上层的NDFD较高,但随着降解时间的延长,在瘤胃内降解48 h后,中层、下层的NDFD显著高于上层全株玉米青贮的NDFD,可能是由于全株玉米青贮中NDF含量较高,可达50%左右,在瘤胃中降解速率较慢,在瘤胃内24 h后NDF降解不完全,而随着降解时间延长,NDF被降解的更充分,进而显现出发酵效果越好的全株玉米青贮NDFD越高。全株玉米青贮中淀粉7 h的瘤胃降解率即可说明其淀粉消化情况,可将其作为生物评价相关指标,本试验结果显示不同深度的淀粉降解率无显著性差异,可能是因为淀粉属于快速降解部分,在瘤胃内易被降解吸收利用,7 h下淀粉可被降解1/2以上,因而7 h的淀粉降解率并未受到含量变化的影响。
4 结论大型青贮窖内不同深度全株玉米青贮质量存在差异,然而达到一定深度后,发酵品质趋于稳定,综合评价结果显示中层全株玉米青贮质量最佳。因而,在青贮制作过程中,应注重逐层压窖,推荐使用隔氧膜封窖。在取料过程中,上层、下层均匀取料,降低青贮饲料对饲粮配方一致性的影响。
| [1] |
张晓庆, 穆怀彬, 侯向阳, 等. 我国青贮玉米种植及其产量与品质研究进展[J]. 畜牧与饲料科学, 2013, 34(1): 54-57. DOI:10.3969/j.issn.1672-5190.2013.01.024 |
| [2] |
蒋万, 谢铁娜, 周玉香. 不同青贮玉米品种的生物产量及青贮料品质分析[J]. 黑龙江畜牧兽医, 2012(21): 77-79. |
| [3] |
郭勇庆, 曹志军, 李胜利, 等. 全株玉米青贮生产与品质评定关键技术——高成本玉米时代牛场技术与管理策略之一[J]. 中国畜牧杂志, 2012, 48(18): 39-44. DOI:10.3969/j.issn.0258-7033.2012.18.010 |
| [4] |
赵雪娇, 张立阳, 刘帅, 等. 留茬高度对不同品种全株玉米青贮品质的影响[J]. 动物营养学报, 2018, 30(8): 3239-3246. DOI:10.3969/j.issn.1006-267x.2018.08.043 |
| [5] |
GEYER S, HOFFMANN T. Metrological prerequisites for determination of silage density compacted in a bunker silo using gamma rays[J]. Agricultural Engineering International:The CIGR Journal, 2012, 14(4): 134-143. |
| [6] |
FRANCO R T, BUFFIÈRE P, BAYARD R. Ensiling for biogas production:critical parameters.A review[J]. Biomass and Bioenergy, 2016, 94: 94-104. DOI:10.1016/j.biombioe.2016.08.014 |
| [7] |
闫贵龙, 曹春梅, 刁其玉, 等. 夏季窖内不同深度全株玉米青贮品质和营养价值的比较[J]. 畜牧兽医学报, 2011, 42(3): 381-388. |
| [8] |
闫贵龙, 曹春梅, 刁其玉, 等. 青贮窖中不同深度全株玉米青贮品质和营养价值的比较[J]. 畜牧兽医学报, 2010, 41(6): 697-704. |
| [9] |
全国饲料工业标准化技术委员会.GB/T 14699.1—2005饲料采样[S].北京: 中国标准出版社, 2005.
|
| [10] |
AOAC International. Official methods of analysis of AOAC international[M]. 18th ed. Washington, D.C.: AOAC, 2005.
|
| [11] |
VAN SOEST P J, ROBERTSON J B, LEWIS B A. Methods for dietary fiber, neutral detergent fiber, and nonstarch polysaccharides in relation to animal nutrition[J]. Journal of Dairy Science, 1991, 74(10): 3583-3597. DOI:10.3168/jds.S0022-0302(91)78551-2 |
| [12] |
WEATHERBURN M W. Phenol-hypochlorite reaction for determination of ammonia[J]. Analytical Chemistry, 1967, 39(8): 971-974. DOI:10.1021/ac60252a045 |
| [13] |
SUN X Q, GIBBS S J. Diurnal variation in fatty acid profiles in rumen digesta from dairy cows grazing high-quality pasture[J]. Animal Feed Science and Technology, 2012, 177(3/4): 152-160. |
| [14] |
卢定强, 徐蓓, 李晖, 等. 反相高效液相色谱法同时测定乳酸及乳酸甲酯[J]. 精细化工, 2007, 24(2): 206-208. DOI:10.3321/j.issn:1003-5214.2007.02.027 |
| [15] |
中华人民共和国国家卫生和计划生育委员会.GB 4789.35—2016食品安全国家标准食品微生物学检验乳酸菌检验[S].北京: 中国标准出版社, 2016.
|
| [16] |
中华人民共和国国家卫生和计划生育委员会.GB 4789.15—2016食品安全国家标准食品微生物学检验霉菌和酵母计数[S].北京: 中国标准出版社, 2017.
|
| [17] |
国家科学研究委员会组织.奶牛营养需要[M]. 7版.孟庆翔译.北京: 中国农业大学出版社, 2001: 21-23.
|
| [18] |
王旭哲, 张凡凡, 唐开婷, 等. 密度对玉米青贮发酵品质、微生物和有氧稳定性的影响[J]. 中国草地学报, 2018, 40(1): 80-86. |
| [19] |
傅彤.微生物接种剂对玉米青贮饲料发酵进程及其品质的影响[D].硕士学位论文.北京: 中国农业科学院, 2005. http://cdmd.cnki.com.cn/Article/CDMD-82101-2005114817.htm
|
| [20] |
史海涛, 杨军香, 田雨佳, 等. 玉米秸秆营养价值的开发利用——未充分开发利用的廉价资源[J]. 中国奶牛, 2012(17): 3-11. DOI:10.3969/j.issn.1004-4264.2012.17.002 |
| [21] |
NEYLON J M, KUNG L K, Jr. Effects of cutting height and maturity on the nutritive value of corn silage for lactating cows[J]. Journal of Dairy Science, 2003, 86(6): 2163-2169. DOI:10.3168/jds.S0022-0302(03)73806-5 |
| [22] |
LYNCH J P, BAAH J, BEAUCHEMIN K A. Conservation, fiber digestibility, and nutritive value of corn harvested at 2 cutting heights and ensiled with fibrolytic enzymes, either alone or with a ferulic acid esterase-producing inoculant[J]. Journal of Dairy Science, 2015, 98(2): 1214-1224. DOI:10.3168/jds.2014-8768 |
| [23] |
GOESER J P, COMBS D K. An alternative method to assess 24-h ruminal in vitro neutral detergent fiber digestibility[J]. Journal of Dairy Science, 2009, 92(8): 3833-3841. DOI:10.3168/jds.2008-1136 |




