近年来,随着人们消费水平的不断提高,对肉制品、奶制品等畜产品需求增加,促使反刍动物养殖快速向集约化、规模化发展,大大提高了畜产品产量。与此同时,越来越多公共食品安全事件的出现,使人们更加关注畜产品的质量与安全,生产者们更加重视健康、高效的养殖方法,并且加大了对畜产品品质的检测。
最近,消费者对富含生物活性化合物的畜产品关注度越来越高,因为这些化合物可以影响人体健康[1-3]。在反刍动物畜产品中生物化合物的含量被认为与动物饲粮中的活性化合物含量紧密相关。青绿饲料是反刍动物重要的食物来源,其含有丰富的叶绿素、叶黄素、β-胡萝卜素、蛋白质和不饱和脂肪酸,动物采食后,这些物质会影响反刍动物的营养代谢和动物产品的感官特性[4-5]。
植物光合色素包括叶绿素、叶黄素、β-胡萝卜素等,具有抗氧化作用,其中一些色素也是人体必需的营养成分,例如叶黄素是视网膜组成成分[6],β-胡萝卜素是维生素A的合成原料[7]。植物色素具有提高免疫的功能,对反刍动物机体具有积极作用[8]。近期的一些研究也关注了叶黄素和β-胡萝卜素对反刍动物机体和动物制品的影响[9],然而,关于叶绿素对反刍动物的影响及其应用的研究较少。饲喂反刍动物青绿饲料时,其叶绿素的叶绿醇基与瘤胃微生物发生作用,代谢释放出植烷酸分子。植烷酸作为一种天然的配体,是过氧化物酶活性受体的激活物[10-11],具有抗脂肪酸氧化等功能,它不仅可以降低某些类型癌症的患病风险[12-14],也可预防某些代谢综合征的发生[2, 15]。最近植烷酸也被证实具有改善T细胞介导的作用和预防自身免疫性疾病的潜力[16]。随着植烷酸功能更多的发现,它将成为一种被重视的新型功能性脂肪酸[17]。有研究发现,在牛脂肪细胞中添加植烷酸后,可以显著提高脂肪细胞过氧化物酶体增殖激活物受体γ(PPARγ)mRNA的表达[18],这表明植烷酸能激活PPARγ,进而可以调控脂质和糖代谢[11],该报告也指出在反刍动物肝脏中存在较多的植烷酸[11]。植烷酸被认为对缓解脂肪肝、肥胖等生活习惯病具有明显效果[19]。值得注意的是,人类体内的植烷酸几乎全部来自于反刍动物产品,如奶制品、肉制品[20],它不能在哺乳动物体内合成[21]。探究畜产品中植烷酸的变动规律不仅对生产高质量畜产品有重要科学意义[22],而且也将有助于我们更加合理地摄取动物产品,对人类健康将起到更积极作用。综上,本文着眼于青绿饲料的叶绿素资源,结合国内外现有研究进展对牧草中叶绿素含量的动态变化、影响因素及其对反刍动物影响进行综述。
1 青绿饲料中叶绿素含量的动态变化 1.1 叶绿素的结构和种类叶绿素广泛存在于自然界中,其分子由2部分组成,其核心部分是一个具有光吸收功能的卟啉环,它的中心含有1个镁离子;另一部分是1个脂肪烃侧链,称为叶绿醇基,其游离态分子被称之为叶绿醇[23]。叶绿素种类包括叶绿素a、b、c、d、f以及原叶绿素和细菌叶绿素等[24-25]。叶绿素很不稳定,在光、酸、碱、氧化剂等条件下都会被分解。在酸性条件下,叶绿素分子易失去卟啉环中的镁离子成为脱镁叶绿素[26]。叶绿素不仅具有抗氧化功能,而且具有造血、提供维生素、解毒、抗病等多种用途,是人类重要的自然资源[27]。
1.2 叶绿素在青绿饲料中的变化光合作用的增强,会有效提升牧草中叶绿素的含量和牧草的产量[28-29]。氮元素是参与光合作用的重要元素之一[30],对牧草施加氮肥可以有效提升叶绿素的含量,这个现象已在多个试验结果中得到了验证[31-32],而且试验结果都表明了施加的氮肥量与牧草中叶绿素的含量成正相关。收割阶段影响牧草中氮含量,也影响叶绿素与叶绿醇的含量[31]。通过加施氮肥或早期收割的方法均可得到较高含量的叶绿素或叶绿醇,这有助于生产高附加值的牧草。叶绿素的分解受到温度、日照、水分等影响。研究表明,低温明显减缓叶绿素的分解,长时间日照对叶绿素的破坏程度较大,同时,研究者还发现白光和黄光会加速叶绿素的分解[33]。牧草干燥程度(水分含量)影响叶绿素含量。牧草在收割后自然干燥至70%水分时,叶绿素和叶绿醇含量没有发生明显变化,随着干燥时间的延长,牧草水分降至30%左右时,有50%以上的叶绿素和叶绿醇被分解[34]。可见,长时间的紫外线照射和牧草内部水分的流失,会导致大部分叶绿素和叶绿醇资源流失,进而使牧草的潜在营养价值降低。上述结果暗示了保持牧草中的高水分含量可以有效减缓收割牧草中叶绿素的分解,因此,在制作青贮饲料时(水分含量70%~75%),收割牧草中的叶绿素和叶绿醇资源还可以得到完好的保存。此外,不同牧草品种,叶绿素的含量也存在明显差异[35],经过对比了几项研究后发现,在相同栽培条件下,热带牧草中叶绿素含量高于一些温带牧草[32, 35-36]。
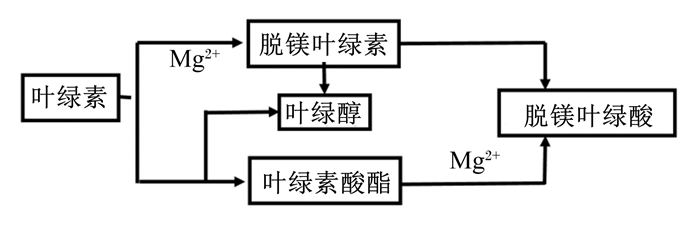
1.3 叶绿素在青贮过程中的代谢通常情况下,在植物落叶或老化的过程中,叶绿素有2种分解途径:一是在酸性条件下,叶绿素的中央镁离子被去除,叶绿素转化为脱镁叶绿素,进而转化为脱镁叶绿酸和叶绿醇;二是在叶绿素酶的作用下,叶绿素分解为叶绿醇和叶绿素酸酯,叶绿素酸酯再进一步释放镁离子,进而转化为脱镁叶绿酸[25],如图 1所示。
|
图 1 植物落叶或老化过程中叶绿素的基本代谢路径 Fig. 1 Decomposition pathways of chlorophyll in plants during leaves falling or aging |
叶绿素的稳定性受到pH的影响[13]。Lv等[31, 37]的试验中探究了黑麦草青贮中叶绿素的变动规律,结果显示,在青贮中没有检测到叶绿素酸酯,由此判定了青贮牧草中叶绿素的分解路径可能是单一的,此结果将有待于进一步探明。此外,青贮后,牧草中叶绿素的分解产物(如脱镁叶绿酸、叶绿醇)都受到了施肥水平和收割阶段的影响。值得注意的是,这项研究还发现了叶绿醇的含量在青贮后没有明显变动,并且不受发酵品质和添加乳酸菌的影响[37]。在青贮环境下,尽管约80%叶绿素被分解,但叶绿醇含量几乎没有变动。可见,青贮是一个有效保存叶绿醇资源的牧草加工手段,这有助于促进扩大粗饲料资源利用。
2 叶绿素在反刍动物中的应用反刍动物采食青绿饲料后,叶绿素的叶绿醇基在瘤胃中被释放后代谢成为植烷酸(3, 7, 11, 15-四甲基十六烷酸,PA)[38],并沉积到奶制品和肉制品中[39-40]。由于植烷酸的主要前体是叶绿素中的叶绿醇基,所以反刍动物产品中的植烷酸含量与所摄取的叶绿素或叶绿醇有着直接的关系[3, 41]。
研究发现,通过体外培养具有不同含量叶绿醇的青贮牧草,在瘤胃微生物作用下,产生植烷酸的含量较低,特别是转化比例,仅为17%~35%[42],值得注意的是,大部分的叶绿醇会残留下来,说明瘤胃微生物对叶绿醇的作用是有限的。Lee等[43]的研究中发现,在饲喂牛红三叶草后,十二指肠食糜中的植烷酸流量同比对照组偏低,这可能是多酚氧化酶抑制了叶绿素和叶绿醇在瘤胃内水解,导致生物氢化作用效率降低,但没有更多的证据解释这一现象。
植烷酸的含量是判定有机奶制品的重要营养学指标之一[44]。牛奶中植烷酸含量与饲喂奶牛的粗饲料比例之间存在着密切关联[45]。研究发现,饲养方式影响牛奶中植烷酸含量。研究者对比了有机饲养方式(饲养标准为85%的干草和青贮)和传统饲养方式(饲养标准为50%的青绿饲料和50%的精饲料)后的牛奶中植烷酸含量。结果显示,在有机饲养条件下,牛奶中植烷酸的含量是传统饲养条件下的2倍以上[3]。粗饲料类型也影响牛奶中植烷酸含量,给泌乳期奶牛分别投喂高比例青贮或干草,结果显示饲喂青贮条件下的牛奶中植烷酸含量显著高于饲喂干草的牛奶[46]。Wierzbicki等[47]饲喂奶牛高叶绿醇全混合饲料后,发现牛奶中植烷酸含量显著偏高,同时,在奶牛的粪便中也检测到了叶绿醇和植烷酸的存在。由此可见,植烷酸不能被动物全部吸收。通过计算发现,仅有约3%植烷酸沉积到牛奶中[48],这显示了叶绿醇的利用率较低,如何提升叶绿醇转化还需要深入研究。此外,经过对比了几项关于奶制品的研究后发现,牛奶中植烷酸含量存在差异[45-46],除了粗饲料中叶绿素和叶绿醇含量的差异,奶牛的品种和个体因素或饲养环境也可能影响牛奶中植烷酸的含量。在反刍动物体内,植烷酸大部分被小肠上皮细胞吸收,这与长链脂肪酸吸收机理相同[47],脂肪组织中的甘油三酯被认为是植烷酸及其衍生物的储存位点[17],而植烷酸在反刍动物机体内的排泄机制还尚不明确[48],这有待进一步探究。
3 未来研究方向我国热带地区纬度低、光照强,且牧草种类多、生物量大,为生产高叶绿素含量牧草提供了有利条件。叶绿素的含量受到牧草品种、栽培方法的影响。在未来研究中,首先要明确热带地区几种主要牧草中的色素变动规律,结合常规营养分析,通过合理的加工调制,最终生产出高附加值的健康牧草产品。另外,叶绿醇在瘤胃内的消化降解机制尚不清楚,瘤胃内的微生物结构和反应机理极为复杂,我们推测,叶绿醇转化为植烷酸的过程可能是多种瘤胃微生物和一些细菌、酶的共同作用产生的结果。瘤胃环境的差异可能对植烷酸产品造成一定影响,因此,必须进一步探究叶绿素或叶绿醇在瘤胃内的动态变化规律和微生物对其作用机理,以及植烷酸在反刍动物体内分布等。此外,正如上文所述,植烷酸沉积到牛奶的比例是很低的,而植烷酸在肉制品中的含量仍尚不清楚。因此,如何提升畜产品中植烷酸含量有待研究。
4 小结随着近年人们对健康的重视,消费者更加青睐绿色、健康的肉制品与奶制品。利用青绿饲料本身的潜在价值,通过高效科学的饲养方法可有效地提升畜产品质量,并且,在饲养过程中可以有效避免化学添加剂的过度使用,更加有利于扩大粗饲料资源的利用,与此同时,对降低生产成本、缓解环境压力具有重要意义。叶绿素来源于植物光合作用,是丰富的自然资源,深入探究植物中的叶绿素等资源的利用将是反刍动物营养研究的新方向,对牧草的合理利用、动物的高效养殖和绿色健康畜产品的生产有积极作用。
| [1] |
MARTIN B, CORNU A, NATHALIE K, et al.Milk indicators for recognizing the types of forages eaten by dairy cows[M]//HOCQUETTE J F, GIGLI S.Indicators of milk and beef quality.Wageningen, the Netherlands: Wageningen Academic Publishers, 2005: 127-136.
|
| [2] |
HELLGREN L I. Phytanic acid—an overlooked bioactive fatty acid in dairy fat?[J]. Annals of the New York Academy of Sciences, 2010, 1190: 42-49. DOI:10.1111/j.1749-6632.2009.05254.x |
| [3] |
SCHRÖDER M, YOUSEFI F, VETTER W. Investigating the day-to-day variations of potential marker fatty acids for organic milk in milk from conventionally and organically raised cows[J]. European Food Research and Technology, 2011, 232(1): 167-174. DOI:10.1007/s00217-010-1374-8 |
| [4] |
JENSEN S K, JOHANNSEN A K B, HERMANSEN J E. Quantitative secretion and maximal secretion capacity of retinol, β-carotene and α-tocopherol into cows' milk[J]. Journal of Dairy Research, 1999, 66(4): 511-522. DOI:10.1017/S0022029999003805 |
| [5] |
DEWHURST R J, SCOLLAN N D, LEE M R F, et al. Forage breeding and management to increase the beneficial fatty acid content of ruminant products[J]. Proceedings of the Nutrition Society, 2003, 62(2): 329-336. DOI:10.1079/PNS2003241 |
| [6] |
CHEW B P, WONG M W, WONG T S. Effects of lutein from marigold extract on immunity and growth of mammary tumors in mice[J]. Anticancer Research, 1996, 16(6B): 3689-3694. |
| [7] |
BROWN F. The tocopherol content of farm feeding-stuffs[J]. Journal of the Science of Food and Agriculture, 1953, 4(4): 161-165. DOI:10.1002/(ISSN)1097-0010 |
| [8] |
ZHANG L X, COONEY R V, BERTRAM J S. Carotenoids enhance gap junctional communication and inhibit lipid peroxidation in C3H/10T1/2 cells:relationship to their cancer chemopreventive action[J]. Carcinogenesis, 1991, 12(11): 2109-2114. DOI:10.1093/carcin/12.11.2109 |
| [9] |
XU C Z, WANG H F, YANG J Y, et al. Effects of feeding lutein on production performance, antioxidative status, and milk quality of high-yielding dairy cows[J]. Journal of Dairy Science, 2014, 97(11): 7144-7150. DOI:10.3168/jds.2014-8276 |
| [10] |
ZOMER A W M, VAN DER BURG B, JANSEN G A, et al. Pristanic acid and phytanic acid:naturally occurring ligands for the nuclear receptor peroxisome proliferator-activated receptor α[J]. Journal of Lipid Research, 2000, 41(11): 1801-1807. |
| [11] |
MCCARTY M F. The chlorophyll metabolite phytanic acid is a natural rexinoid-potential for treatment and prevention of diabetes[J]. Medical Hypotheses, 2001, 56(2): 217-219. DOI:10.1054/mehy.2000.1153 |
| [12] |
KWAN H Y, CHAO X J, SU T, et al. Dietary lipids and adipocytes:potential therapeutic targets in cancers[J]. The Journal of Nutritional Biochemistry, 2015, 26(4): 303-311. |
| [13] |
WRIGHT M E, ALBANES D, MOSER A B, et al. Serum phytanic and pristanic acid levels and prostate cancer risk in Finnish smokers[J]. Cancer Medicine, 2014, 3(6): 1562-1569. DOI:10.1002/cam4.2014.3.issue-6 |
| [14] |
LISKA J, MACEJOVA D, ONDKOVA S, et al. Morphology of 1-methyl-1-nitrosourea induced rat mammary tumours after treatment with precursor of phytanic acid or its combination with vitamin D analogue[J]. Endocrine Regulations, 2012, 46(1): 21-26. DOI:10.4149/endo_2012_021 |
| [15] |
GRIMALDI P A. Lipid sensing and lipid sensors:peroxisome proliferator-activated receptors as sensors of fatty acids and derivatives[J]. Cellular and Molecular Life Sciences, 2007, 64(19/20): 2305-2321. |
| [16] |
YANG Y H, GOCKE A R, LOVETT-RACKE A, et al. PPAR alpha regulation of the immune response and autoimmune encephalomyelitis[J]. PPAR Research, 2008, 2008: 546753. |
| [17] |
CHAMBRAUD B, RADANYI C, CAMONIS J H, et al. Immunophilins, Refsum disease, and lupus nephritis:the peroxisomal enzyme phytanoyl-CoA α-hydroxylase is a new FKBP-associated protein[J]. Proceedings of the National Academy of Sciences of the United States of America, 1999, 96(5): 2104-2109. DOI:10.1073/pnas.96.5.2104 |
| [18] |
GARCÍA-ROJAS P, ANTARAMIAN A, GONZÁLEZ-DÁVALOS L, et al. Induction of peroxisomal proliferator-activated receptor γ and peroxisomal proliferator-activated receptor γ coactivator 1 by unsaturated fatty acids, retinoic acid, and carotenoids in preadipocytes obtained from bovine white adipose tissue[J]. Journal of Animal Science, 2010, 88(5): 1801-1808. DOI:10.2527/jas.2009-2579 |
| [19] |
AN J Y, JHENG H F, NAGAI H, et al. A phytol-Enriched diet activates PPAR-α in the liver and brown adipose tissue to ameliorate obesity-induced metabolic abnormalities[J]. Molecular Nutrition & Food Research, 2018, 62(6): 1700688. |
| [20] |
VERHOEVEN N M, JAKOBS C. Human metabolism of phytanic acid and pristanic acid[J]. Progress in Lipid Research, 2001, 40(6): 453-466. DOI:10.1016/S0163-7827(01)00011-X |
| [21] |
CHE B N, KRISTENSEN T, NEBEL C, et al. Content and distribution of phytanic acid diastereomers in organic milk as affected by feed composition[J]. Journal of Agricultural and Food Chemistry, 2013, 61(1): 225-230. DOI:10.1021/jf304079r |
| [22] |
YOUNG F, THERKILDSEN M, EKSTRAND B, et al. Novel aspects of health promoting compounds in meat[J]. Meat Science, 2013, 95(4): 904-911. DOI:10.1016/j.meatsci.2013.04.036 |
| [23] |
林厦菁, 朱晓彤, 束刚, 王松波, 王丽娜, 高萍, 江青艳. 叶绿醇对小鼠生长性能和糖脂代谢的影响[J]. 畜牧与兽医, 2012, 44(增刊1): 212. |
| [24] |
黄持都, 胡小松, 廖小军, 等. 叶绿素研究进展[J]. 中国食品添加剂, 2007(3): 114-118. DOI:10.3969/j.issn.1006-2513.2007.03.023 |
| [25] |
MATILE P, HÖRTENSTEINER S, THOMAS H, et al. Chlorophyll breakdown in senescent leaves[J]. Plant Physiology, 1996, 112(4): 1403-1409. DOI:10.1104/pp.112.4.1403 |
| [26] |
蔡秋声. 叶绿素及其衍生物的特性和生理功能[J]. 粮食与油脂, 1997(3): 38-40. |
| [27] |
KOCA N, KARADENIZ F, BURDURLU H S. Effect of pH on chlorophyll degradation and colour loss in blanched green peas[J]. Food Chemistry, 2006, 100(2): 609-615. |
| [28] |
武维华. 植物生理学[M]. 第2版. 北京: 科学出版社, 2012.
|
| [29] |
张明生, 谢波, 谈锋, 等. 甘薯可溶性蛋白、叶绿素及ATP含量变化与品种抗旱性关系的研究[J]. 中国农业科学, 2003, 36(1): 13-16. DOI:10.3321/j.issn:0578-1752.2003.01.003 |
| [30] |
吕玉兰, 王跃全, 杨蓓, 等. 施氮对多花黑麦草叶片叶绿素和鲜草产量的影响[J]. 草业科学, 2013, 30(4): 606-609. |
| [31] |
LV R L, EL-SABAGH M, OBITSU T, et al. Effects of nitrogen fertilizer and harvesting stage on photosynthetic pigments and phytol contents of Italian ryegrass silage[J]. Animal Science Journal, 2017, 88(10): 1513-1522. DOI:10.1111/asj.2017.88.issue-10 |
| [32] |
何金环, 李凤铃, 王延方. 牧草叶绿素含量与蛋白质含量相关性的研究[J]. 河南农业科学, 2015, 44(2): 139-141. |
| [33] |
蒋彪, 潘永华, 龚国斌. 光照和温度对叶绿素成分影响的研究与探索[J]. 光电子技术, 2007, 27(4): 277-280. DOI:10.3969/j.issn.1005-488X.2007.04.017 |
| [34] |
LV R L, EL-SABAGH M, OBITSU T, et al.Effects of N fertilization levels and wilting periods on chemical composition and chlorophyll content of Italian ryegrass harvested at different stage[C]//Proceedings of the 5th China-Japan-Korea Grassland Conference.Changchun: Northeast Normal University, 2014. https://www.researchgate.net/publication/265687043_Effects_of_N_fertilization_levels_and_wilting_periods_on_chemical_composition_and_chlorophyll_content_of_Italian_ryegrass_harvested_at_different_stage
|
| [35] |
梁志霞, 宋同清, 曾馥平, 等. 氮素和刈割对桂牧1号杂交象草光合作用、产量和品质的影响[J]. 生态学杂志, 2013, 32(8): 2008-2014. |
| [36] |
李磊, 李向义, 林丽莎, 等. 两种生境条件下6种牧草叶绿素含量及荧光参数的比较[J]. 植物生态学报, 2011, 35(6): 672-680. |
| [37] |
LV R, EL-SABAGH M, OBISTU T, et al.Effects of ensiling with lactic acid bacteria or formic acid on functional component contents in ensiled Italian ryegrass grown with different fertilizer levels[C]//Proceedings of the 17th AAAP Animal Science Congress.Fukuoka, Japan: [n.s.], 2016.
|
| [38] |
SCHRÖDER M, VETTER W. GC/EI-MS determination of the diastereomer distribution of phytanic acid in food samples[J]. Journal of the American Oil Chemists' Society, 2011, 88(3): 341-349. DOI:10.1007/s11746-010-1682-y |
| [39] |
ACKMAN R G, HANSEN R P. The occurrence of diastereomers of phytanic and pristanic acids and their determination by gas-liquid chromatography[J]. Lipids, 1967, 2(5): 357-362. DOI:10.1007/BF02531848 |
| [40] |
WANDERS R J A, KOMEN J, FERDINANDUSSE S. Phytanic acid metabolism in health and disease[J]. Biochimica et Biophysica Acta:Molecular and Cell Biology of Lipids, 2011, 1811(9): 498-507. DOI:10.1016/j.bbalip.2011.06.006 |
| [41] |
LEIBER F, KREUZER M, NIGG D, et al. A study on the causes for the elevated n-3 fatty acids in cows' milk of alpine origin[J]. Lipids, 2005, 40(2): 191-202. |
| [42] |
LV R L, SATO M, EL-SABAGH M, et al.Effect of fertilization levels and harvesting stages of grass silages on ruminal phytanic acid production in vitro[C]//The 10th Korea Japan China Joint Symposium on Rumen Metabolism and Physiology.Sunchon, Korea: Sunchon National University, 2015. https://www.researchgate.net/publication/280737238_Effects_of_fertilization_levels_and_harvesting_stages_of_grass_silages_on_ruminal_phytanic_acid_production_in_vitro
|
| [43] |
LEE M R F, CONNELLY P L, TWEED J K S, et al. Effects of high-sugar ryegrass silage and mixtures with red clover silage on ruminant digestion.2.Lipids[J]. Journal of Animal Science, 2014, 84(11): 3061-3070. |
| [44] |
VETTER W, SCHRÖDER M. Concentrations of phytanic acid and pristanic acid are higher in organic than in conventional dairy products from the German market[J]. Food Chemistry, 2010, 119(2): 746-752. DOI:10.1016/j.foodchem.2009.07.027 |
| [45] |
BAARS T. Milk consumption, raw and general, in the discussion on health or hazard[J]. Journal of Nutritional Ecology and Food Research, 2013, 1(2): 91-107. DOI:10.1166/jnef.2013.1027 |
| [46] |
SCHRÖDER M, LUTZ N L, TANGWAN E C, et al. Phytanic acid concentrations and diastereomer ratios in milk fat during changes in the cow's feed from concentrate to hay and back[J]. European Food Research and Technology, 2012, 234(6): 955-962. DOI:10.1007/s00217-012-1710-2 |
| [47] |
WIERZBICKI A S, SANKARALINGAM A, LUMB P J, et al. Transport of phytanic acid on lipoproteins in Refsum disease[J]. Journal of Inherited Metabolic Disease, 1999, 22(1): 29-36. DOI:10.1023/A:1005486913371 |
| [48] |
TOREQUL ISLAM M, ALI E S, DE CARVALHO R M, et al. Phytanic acid, a daily consumed chlorophyll-yielded phytol bio-metabolite:a comprehensive review[J]. African Journal of Pharmacy and Pharmacology, 2016, 10(48): 1025-1033. DOI:10.5897/AJPP |




