2. 福建省畜牧总站, 福州 350003
2. Fujian Animal Husbandry Station, Fuzhou 350003, China
近年来,雏鹅内脏型痛风在全国范围内大面积爆发,此病多在10~14日龄集中发病,15日龄前后进入死亡高峰,发病率为30%~50%,死亡率高达50%[1],给养鹅业带来了极大的经济损失。内脏型痛风是禽类肾脏损伤所导致的高尿酸血症,并以尿酸盐的形式沉积在关节囊、关节软骨、关节周围、胸腹腔及各种脏器表面和其他间质组织中的一种疾病[2]。饲粮蛋白质水平过高时,特别是嘌呤核苷酸含量高的鱼粉、肉骨粉等饲料原料占比过大,禽类蛋白质代谢的终产物——尿酸生成增多[3],引发高尿酸血症;当血尿酸达到阈值时,尿酸盐就会在关节、软骨和内脏器官的表面沉积下来,诱发雏鹅痛风[4-5]。高钙是诱发禽类痛风的另一重要因素,往往是由于矿物质原料不合格或配制比例失衡所致,多造成高钙血症和代谢性碱中毒,同时碱性环境下易引起尿酸钙的沉积,堵塞肾小管[6]。肾组织钙化和肾小管堵塞造成的尿酸排泄障碍,最终会引起痛风和肾衰竭的发生。郭小权[7]使用高蛋白质饲粮和高钙饲粮成功复制了鸡内脏型痛风病例,证实了饲粮蛋白质和钙对禽痛风发生的重要影响。
饲粮对肾脏的影响很大程度上取决于肠道菌群的代谢活动[8-9]。肠道菌群失调可导致肠壁通透性增加,细菌和内毒素易位,进而诱发和加重多个远隔器官(如肾脏、肝脏等)的功能障碍[10]。在人类尿毒症、慢性肾病及痛风的研究中,肠道微生物的作用已被证实。在痛风患者的粪便菌群中拟杆菌属、紫单胞菌科、Erysipelatoclostridium及厌氧绳菌科等条件致病菌的数量增加,其肠道微生态系统受到损害[11]。同时,研究发现,调节肠道菌群分布可一定程度上缓解慢性肾脏病和终末期肾脏病患者病情,证实了修复肠黏膜生物屏障对痛风治疗的重要性[12]。因此,为证实肠道微生态平衡与肾脏健康在雏鹅痛风发生中的密切关系,本文研究了高蛋白质高钙饲粮对雏鹅内脏型痛风发生、肾脏功能及肠道微生物区系的影响,从新角度诠释“肠道-肾脏”健康的相互联系,为寻求有效的鹅痛风防治措施提供新方向。
1 材料与方法 1.1 试验设计和试验管理选取1日龄扬州白鹅雏鹅72只(公:母=1:1),随机分为4组,分别为对照组(control group,蛋白质水平16%、钙水平1%)、高蛋白质组(high protein group,蛋白质水平22%、钙水平1%)、高钙组(high calcium group,蛋白质水平16%、钙水平3%)、高蛋白质高钙组(high protein and calcium group,蛋白质水平22%、钙水平3%),每组18只。试验饲粮由江苏康迪富尔饲料有限公司配制提供,试验饲粮组成及营养水平见表 1。试验饲粮营养水平参照国内外雏鹅饲料营养标准及走访调查情况设置[13]。试验期共21 d。试验采取舍内双层笼养,自由采食,充足饮水,按正常免疫程序进行免疫接种。
|
|
表 1 试验饲粮组成及营养水平(风干基础) Table 1 Composition and nutrient levels of experimental diets (air-dry basis) |
试验期间,当雏鹅具有行动迟缓、缩颈、粪便发白等前期临床症状;剖检后表现为心包增厚,有白色结晶物附着或包被,肾脏苍白肿大、花斑肾,输尿管变粗,直肠末端内容物白色稀粪积聚,标记为“疑似发病”[2, 6]。试验结束时,计算各组发病率。试验中,记录发病期间(6~14日龄)平均采食量和3、10、15和21日龄体重,分析组间生长差异。
1.3 血清指标测定分别于试验第10、15、21天,每组随机挑选雏鹅6只,颈静脉采血,3 500 r/min离心15 min,收集血清,-80 ℃保存待测。血清尿酸含量采用酶比色法测定,血清肌酐含量采用肌氨酸氧化酶法测定,血清尿素氮含量采用脲酶法测定,血清黄嘌呤氧化酶(xanthine oxidase, XOD)活性采用酶比色法测定,试剂盒均购于南京建成生物工程研究所。一般来说,健康个体的血清尿酸溶解度为400 μmol/L左右(♂:416 μmol/L,♀:357 μmol/L),超出这个范围则会析出晶体。
1.4 盲肠食糜16S rRNA测序于试验第15天,每组随机挑选雏鹅6只,全身消毒,打开腹腔,收集盲肠食糜,放入无菌的2 mL离心管中,液氮速冻,-80 ℃冰箱保存待测。首先对盲肠食糜中的DNA进行提取(具体方法参照Omega公司生产的E.Z.N.A.TM Soil DNA Kit试剂盒提取)、PCR扩增和纯化,然后构建Miseq文库并进行测序(测序服务委托杭州联川生物科技有限公司)。Miseq测序完成后,利用overlap将双端数据进行拼接,并进行质控、嵌合体过滤,获得高质量的有效数据,并对最终获得有效数据进行97%的相似度聚类,获得最终的分类操作单元(operational taxonomic unit, OTU)丰度及代表序列,进一步进行多样性分析、物种分类注释和差异分析等。试验所得OUT核酸序列的GenBank登录号(accession No.)为MH196573~MH196855。试验通过Venn图展现不同样本之间共有或特有OTU,并基于OTU的统计结果,计算样品的alpha多样性(Shannon指数、Simpson指数和Chao1指数)。接着,使用最新的RDP和NT-16S数据库资源做物种分类及差异分析,以保证注释结果完整准确。最后,试验使用LEfSe(LDA effect size)分析寻找不同组间在丰度上有显著性差异的物种。
1.5 统计分析试验数据使用SPSS 16.0软件分析,对体重、血清指标等采用单因素方差分析进行统计,并使用LSD法多重比较组间差异。试验结果以平均值±标准误表示。
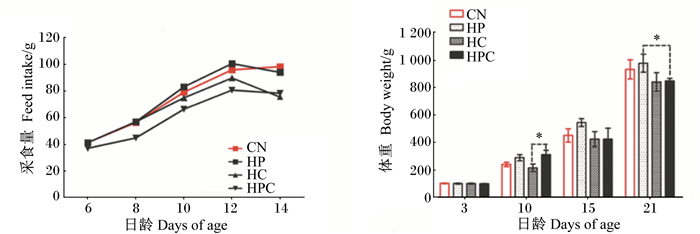
2 结果 2.1 高蛋白质高钙饲粮对雏鹅平均采食量和体重的影响由图 1可见,与对照组相比,高蛋白质组、高钙组和高蛋白质高钙组雏鹅平均采食量从12日龄起均有不同程度地下降。其中,高蛋白质高钙组鹅群平均采食量略低于其他各组(P>0.05)。3和15日龄时,各组体重差异不显著(P>0.05);10日龄时,高蛋白质高钙组体重显著高于高钙组(P<0.05);21日龄时,高蛋白质组体重显著高于高蛋白质高钙组(P<0.05)。
|
CN:对照组;HP:高蛋白质组;HC:高钙组;HPC:高蛋白质高钙组。*表示差异显著(P < 0.05),**表示差异极显著(P < 0.01)。下图同。 CN: control group; HP: high protein group; HC: high calcium group; HPC: high protein and calcium group. * mean significant difference (P < 0.05), and ** mean extremely significant difference (P < 0.01). The same as below. 图 1 高蛋白质高钙饲粮对雏鹅平均采食量和体重的影响 Fig. 1 Effects of high protein and calcium diets on average feed intake and body weight of goslings |
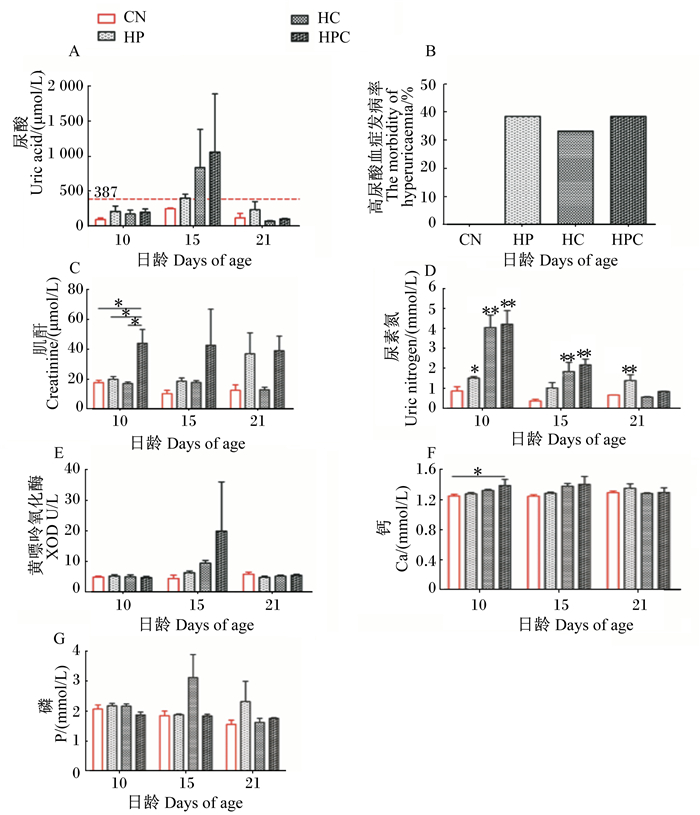
由图 2可见,高蛋白质高钙饲粮对雏鹅肾脏功能有一定的影响,并且这种影响在15日龄时最为明显。10日龄时,各组血清尿酸含量均在正常范围以内,且组间无显著差异(P>0.05);高蛋白质高钙组血清肌酐和钙含量显著高于对照组(P<0.05),血清尿素氮含量极显著高于对照组(P<0.01)。15日龄时,高蛋白质组、高钙组及高蛋白质高钙组血清尿酸含量均达到阈值,且以高蛋白质高钙组血清尿酸含量最高;高蛋白质组血清尿素氮含量显著高于对照组(P<0.05),高钙组和高蛋白质高钙组血清尿素氮含量极显著高于对照组(P<0.01)。21日龄时,大部分反映肾功能的指标均有所降低,只有高蛋白质组血清尿素氮含量极显著高于对照组(P<0.05)。整个试验期间,高蛋白质组、高钙组和高蛋白质高钙组高尿酸血症发病率接近40%。此外,试验中高尿酸血症雏鹅均出现了肾脏肿大、肾小管内充斥白色尿酸盐结晶症状,死亡2 h后,心脏外均出现白色物质覆盖,与痛风雏鹅的典型症状相符。
|
图 2 高蛋白质高钙饲粮对雏鹅肾脏功能的影响 Fig. 2 Effects of high protein and calcium diets on kidney function of goslings |
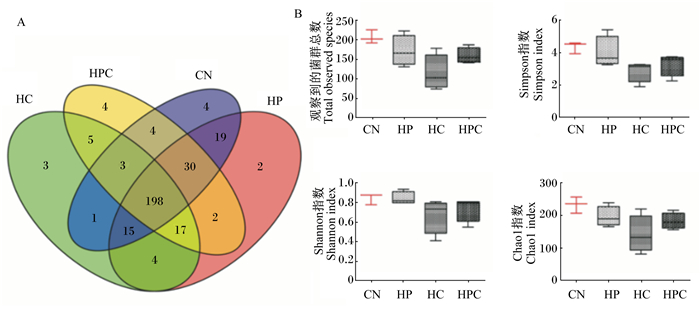
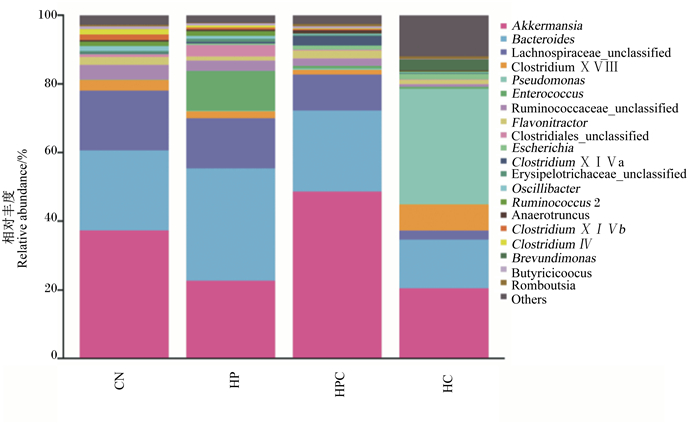
通过对盲肠食糜的16S rRNA测序,试验得到了640 414条原始序列,对数据进行整理后,得到554 431条高质量序列。按照97%的序列相似度将这些序列聚类成为OTU,最终得到2 155个OUT、5个门、11个纲、23个目、39个科、71个属和83个种。基于OTU的统计结果,我们计算了样品的alpha多样性指数。如图 3所示,各组间观测到的菌群总数及alpha多样性指数无显著差异(P>0.05)。此外,试验对属水平的菌群丰度进行了相对定量分析,如图 4所示,艾克曼菌属(Akkermansia)、拟杆菌属(Bacteroides)、毛螺菌科-未知属(Lachnospiraceae_unclassified)、梭菌ⅩⅤⅢ属(Clostridium ⅩⅤⅢ)、假单胞菌属(Pseudomonas)等为雏鹅盲肠食糜中的优势菌属,丰度较高。为了进一步分析高蛋白质高钙饲粮对雏鹅盲肠菌群结构的影响,我们将各组菌群丰度与对照组进行对比,通过LEfSe分析得到了主要的差异菌群,如图 5所示,高蛋白质组雏鹅盲肠中肠球菌属(Enterococcus)丰度显著高于对照组(P<0.05);高钙组与高蛋白质组情况类似,并发现盲肠中Enterococcus massiliensis丰度显著高于对照组(P<0.05);高蛋白质高钙组盲肠中变形杆菌属(Proteus)丰度显著高于对照组(P<0.05)。基于上述结果,我们进一步比较了肠球菌属和变形杆菌属在各组间的丰度变化,结果如图 5-D所示,这2种菌在对照组中丰度很低,但是在试验组中均大幅上升。
|
A:菌群数量韦恩图;B:观察到的总菌群数量和α-多样性指数(Shannon指数、Simpson指数、Chao1指数)。 A: Venn diagram of the observed species; B: total observed species and alpha diversity indexes (Shannon index, Simpson index and Chao1 index). 图 3 高蛋白质高钙饲粮对雏鹅盲肠中菌群和多样性的影响 Fig. 3 Effects of high protein and calcium diets on caecum bacterial community and diversity of goslings |
|
Akkermansia:艾克曼菌属;Bacteroides:拟杆菌属;Lachnospiraceae_unclassified:毛螺菌科未知菌属;Clostridium ⅩⅤⅢ:梭菌属ⅩⅤⅢ;Pseudomonas:假单胞菌属;Enterococcus:肠球菌属;Ruminococcaceae_unclassified:疣微菌科未知菌属;Clostridiales_unclassified:梭菌目未知菌属;Escherichia:埃希氏杆菌属;Clostridium ⅩⅠⅤa:梭菌属ⅩⅠⅤa型;Oscillibacter:颤螺旋菌属;Ruminococcus 2:瘤胃球菌属2;Clostridium ⅩⅠⅤb:梭菌属ⅩⅠⅤb型;Clostridium Ⅳ:梭菌属Ⅳ型;Brevundimonas:短波单胞菌属。 图 4 高蛋白质高钙饲粮对雏鹅盲肠菌群结构的影响 Fig. 4 Effects of high protein and calcium diets on caecum bacterial structure of goslings |

|
A:对照组vs.高蛋白质组;B:对照组vs.高钙组;C:对照组vs.高蛋白质高钙组;D:主要差异致病菌——肠球菌属(Enterococcus)和变形杆菌属(Proteus)在各组间的丰度比较。在图 5-A、图 5-B、图 5-C中,黄色圆形表示组间差异不显著的物种,红色圆形表示在对照组中丰度较高的物种,绿色圆形表示在试验组中丰度较高的物种。LDA SCORE为LDA评分,评分越高组间丰度差异越显著。 A: CN vs. HP; B: CN vs. HC; C: CN vs. HPC; D: comparisons among groups on the relative abundance of the most differential genera-Enterococcus and Proteus. In Fig. 5-A, Fig. 5-B and Fig. 5-C, the yellow circles represent the species with no significant difference between groups, the red circles represent the species with high abundances in the control group, and the green circles represent the species with high abundances in the experimental groups. The LDA score higher, the more significant difference of abundance between groups. Anaerostipes:厌氧棒状菌属;Bacillaceae:芽孢杆菌科;Bacillales:芽孢杆菌目;Bacillus:芽孢杆菌属;Clostridia:梭菌纲;Clostridiales:梭菌目;Clostridium:梭菌属;Coriobacteriaceae:红椿菌科;Coriobacteriales:红椿菌目;Eggerthella:埃格特菌;Enterococcaceae:肠球菌科;Enterococcus:肠球菌属;Enterococcus_cecorum:盲肠肠球菌;Enterococcus_massiliensis:马赛类肠球菌;Firmicutes:厚壁菌门;Gordonibacter:戈登氏杆菌属;Lachnospiraceae:毛螺菌科;Proteus:变形菌门;Ruminococcaceae:疣微菌科;Ruminococcus:瘤胃球菌属;Unclassified:未命名菌属。 图 5 LEfSe分析高蛋白质高钙饲粮影响下主要差异菌群 Fig. 5 LefSe identified the most differential under influences of high protein and calcium diets |
禽类痛风的易感性与其特殊的生理结构有关。由于缺乏尿素合成酶系,禽类不能利用氨合成尿素,此外,肾脏中缺乏谷氨酰胺合成酶,氨不能由谷氨酰胺携带,导致蛋白质代谢的氨产物只能通过嘌呤核苷酸合成及分解途径,最终以尿酸的形式排出[14]。研究表明,饲粮蛋白质水平的升高可导致尿酸合成的显著增加[15],进而导致高尿酸血症;而高钙饲粮则主要通过尿酸代谢障碍而诱发痛风[7]。本试验发现,高蛋白质高钙饲粮可造成雏鹅肾脏损伤,主要表现为血清尿酸、肌酐、尿素氮含量和XOD活性上升。同时,高钙饲粮造成的损伤较高蛋白质饲粮严重,而在高钙的基础上高蛋白质造成的肾脏损伤最为严重。与我们的结果相似,郭小权[7]研究发现,高蛋白质饲粮虽会导致鸡高尿酸血症的发生,但并不足以致死;而高钙饲粮能引起鸡肾脏肾小管上皮的广泛性变性坏死,导致肾功能不全或肾衰竭,进而引起肾小管上皮细胞对尿酸排泄的紊乱。肾小管肾病可经常导致痛风,而这与肾小管主要负责尿酸转运和分泌有关[14]。血清尿酸、肌酐和尿素氮含量的升高多数意味肾脏受损。血清尿酸含量的变化与痛风发生直接相关[16],血清尿酸含量过高导致其在内脏表面析出是雏鹅内脏型痛风的主要判定依据之一。血清肌酐和尿素氮分别为含氮的有机物和蛋白质代谢的终末产物,在肾脏功能正常的情况下,这些小分子物质从肾小球滤出,故可用作肾小球滤过功能的诊断和过筛指标。尿酸代谢限速酶——XOD活性上升则往往是尿酸代谢障碍造成的[17-18],其活性与血清尿酸含量呈正相关;钙离子含量对此酶活性影响很大,高钙往往会使黄嘌呤脱氢酶加速变为黄嘌呤氧化酶,产生更多的尿酸、一氧化氮(NO)及活性氧自由基,加剧肾脏损伤。而饲粮中的磷水平主要通过影响“钙-磷”平衡来影响肾脏功能[19]。换言之,由磷水平改变造成的肾脏损伤主要是因为改变了钙磷比,导致钙水平发生改变,进而影响肾脏功能。总之,高蛋白质饲粮可导致雏鹅肾脏受损,诱发痛风,而高钙的危害较高蛋白质更为严重。此外,我们还发现雏鹅的肾脏损伤在15日龄时最为严重,但在21日龄时,肾脏损伤得到一定缓解,这可能是由于肾脏有一定的自我修复能力,可在一定程度范围内调节肾小管的超滤负荷[14]。
肠道微生物对肾脏健康的影响近年来受到科研工作者的关注,研究人员测定了痛风患者和健康人群的肠道菌群丰度,发现利用痛风微生物指数模型预测痛风症的发生,其准确率高达88.9%[20]。雏鹅痛风主要发生在10~15日龄前后,此时雏鹅消化道菌群结构并不稳定[21-22],饲粮结构不合理极易造成肠道菌群紊乱[23]、肠道通透性改变和菌群易位,增加远隔器官,如肾脏的致病风险[8, 24]。研究发现,肝肾功能受损的小鼠,肠道菌群紊乱,细菌移位率大大增加;反之,使用乳酸菌等益生菌干预后,脂多糖(LPS)诱导肾小球系膜细胞的恶性增殖可被有效抑制[25]。本试验中,我们发现高蛋白质组雏鹅盲肠中肠球菌属丰度显著高于对照组;高钙组与高蛋白质组情况类似,并发现该盲肠中Enterococcus massiliensis丰度显著高于对照组;高蛋白质高钙组盲肠中变形杆菌属丰度显著高于对照组。肠球菌属是最常见的医院感染菌之一,不仅可引起尿路感染、皮肤软组织感染,还可引起危及生命的腹腔感染、败血症、心内膜炎和脑膜炎等[26]。变形杆菌属在自然界中存在极广,它们是条件致病菌,是引发食物细菌性中毒的主要病菌之一,在某些情况下也可导致如尿路感染、呼吸道感染或其他混合感染[27]。研究表明,变形杆菌具有一定的迁徙能力,病菌生长旺盛时可侵入肾脏诱发肾炎和膀胱炎,是造成尿路感染的主要病菌之一(仅次于大肠埃希氏菌)[28]。此外,变形杆菌属还产生尿素酶,水解尿素产氨,使尿液pH升高,引起钙和镁盐的沉积,生成结石[29]。这些证据表明,高蛋白质高钙饲粮可造成肠道有害菌群丰度增高,破坏微生态平衡,特别是某些致病菌的易位(如变形杆菌)可能对肾脏造成靶向性的伤害。
4 结论综上所述,高蛋白质饲粮可造成雏鹅肾脏受损,诱发痛风,而高钙饲粮的危害较高蛋白质饲粮更为严重;同时,这种饲粮因素造成的损伤与肠道肠球菌属、变形杆菌属等有害菌群丰度增高有关,特别是某些致病菌的易位(如变形杆菌)可直接导致肾脏损伤。
| [1] |
罗玲萍, 崔恒敏. 禽类痛风[J]. 中国家禽, 1995, 1(S1): 61-65. |
| [2] |
甘孟侯. 中国禽病学[M]. 北京: 中国农业出版社, 1999.
|
| [3] |
LOEB J N. The influence of temperature on the solubility of monosodium urate[J]. Arthritis & Rheumatism, 1972, 15(2): 189-192. |
| [4] |
刘宗平. 现代动物营养代谢病学[M]. 北京: 化学工业出版社, 2003.
|
| [5] |
朱书梁.高钙和高钙高蛋白质日粮对鸡临床病理学及相关基因表达的影响[D].硕士学位论文.南昌: 江西农业大学, 2014.
|
| [6] |
王宗元. 动物营养代谢病和中毒病学[M]. 北京: 中国农业出版社, 1997.
|
| [7] |
郭小权.高钙日粮致鸡痛风的机理研究[D].博士学位论文.南京: 南京农业大学, 2005.
|
| [8] |
LAN A, ANDRIAMIHAJA M, BLOUIN J M, et al. High-protein diet differently modifies intestinal goblet cell characteristics and mucosal cytokine expression in ileum and colon[J]. The Journal of Nutritional Biochemistry, 2015, 26(1): 91-98. |
| [9] |
KHOURY T, TZUKERT K, ABEL R, et al. The gut-kidney axis in chronic renal failure:a new potential target for therapy[J]. Hemodialysis International, 2017, 21(3): 323-334. DOI:10.1111/hdi.2017.21.issue-3 |
| [10] |
胡翔, 贺德. 肠黏膜生物屏障研究进展[J]. 中国医学工程, 2010, 18(2): 173-176. |
| [11] |
SHAO T J, SHAO L, LI H C, et al. Combined signature of the fecal microbiome and metabolome in patients with gout[J]. Frontiers in Microbiology, 2017, 8: 268. |
| [12] |
ANDERS H J, ANDERSEN K, STECHER B. The intestinal microbiota, a leaky gut, and abnormal immunity in kidney disease[J]. Kidney International, 2013, 83(6): 1010-1016. DOI:10.1038/ki.2012.440 |
| [13] |
施寿荣, 王志跃, 杨海明, 等. 生长鹅集约化饲养条件下的营养需要研究进展[J]. 家禽科学, 2007(1): 38-40. DOI:10.3969/j.issn.1673-1085.2007.01.018 |
| [14] |
GUO X, HUANG K, TANG J. Clinicopathology of gout in growing layers induced by high calcium and high protein diets[J]. British Poultry Science, 2005, 46(5): 641-646. DOI:10.1080/00071660500302661 |
| [15] |
REGINATO A M, MOUNT D B, YANG I, et al. The genetics of hyperuricaemia and gout[J]. Nature Reviews Rheumatology, 2012, 8(10): 610-621. DOI:10.1038/nrrheum.2012.144 |
| [16] |
梁晓萍, 梁琼麟, 胡坪, 等. 高尿酸血症与痛风研究进展[J]. 中国药理学通报, 2008, 24(10): 1265-1268. DOI:10.3321/j.issn:1001-1978.2008.10.002 |
| [17] |
LIN H Y, CHEN Y J, HUANG Q Q, et al. Prokaryotic expression of the chicken xanthine oxidase (XOD) subunit and its localization in liver and kidney[J]. International Journal of Biological Macromolecules, 2016, 87: 341-347. DOI:10.1016/j.ijbiomac.2016.03.001 |
| [18] |
朱明敏.复方土茯苓颗粒对高尿酸血症黄嘌呤氧化酶的抑制作用[D].博士学位论文.广州: 广州中医药大学, 2015.
|
| [19] |
CALVE J, POUPIN N, CHESNEAU C, et al. Protein intake, calcium balance and health consequences[J]. European Journal of Clinical Nutrition, 2012, 66(3): 281-295. DOI:10.1038/ejcn.2011.196 |
| [20] |
GUO Z, ZHANG J C, WANG Z L, et al. Intestinal microbiota distinguish gout patients from healthy humans[J]. Scientific Reports, 2016, 6: 20602. DOI:10.1038/srep20602 |
| [21] |
张名爱, 王宝维, 龙芳羽, 等. 日粮纤维水平对鹅肠道正常菌群的影响[J]. 福建农林大学学报(自然科学版), 2007, 36(2): 159-162. |
| [22] |
崔秀艳, 王长文, 刘墨, 等. 鹅消化道正常菌群定植规律的研究[J]. 中国家禽, 2008, 30(23): 17-21, 24. |
| [23] |
CHOCT M. Managing gut health through nutrition[J]. British Poultry Science, 2009, 50(1): 9-15. DOI:10.1080/00071660802538632 |
| [24] |
WINDEY K, DE PRETER V, VERBEKE K. Relevance of protein fermentation to gut health[J]. Molecular Nutrition & Food Research, 2012, 56(1): 184-196. |
| [25] |
HUANG W, GUO H L, DENG X, et al. Short-chain fatty acids inhibit oxidative stress and inflammation in mesangial cells induced by high glucose and lipopolysaccharide[J]. Experimental and Clinical Endocrinology & Diabetes, 2017, 125(2): 98-105. |
| [26] |
MAASJOST J, MUHLDORFER K, CORTEZ DE JÄCKEL S, et al. Antimicrobial susceptibility patterns of enterococcus faecalis and enterococcus faecium isolated from poultry flocks in germany[J]. Avian Diseases, 2015, 59(1): 143-148. DOI:10.1637/10928-090314-RegR |
| [27] |
毕水莲, 李琳, 唐书泽, 等. 变形杆菌属食物中毒的特点与防控措施[J]. 现代食品科技, 2009, 25(6): 690-695. |
| [28] |
ZUNINO P, SOSA V, ALLEN A G, et al. Proteus mirabilis fimbriae (PMF) are important for both bladder and kidney colonization in mice[J]. Microbiology, 2003, 149(11): 3231-3237. DOI:10.1099/mic.0.26534-0 |
| [29] |
HAWLEY L B.微生物学与感染性疾病[M].陈海伦译.北京: 中信出版社, 2004.
|




