2. 中国农业科学院北京畜牧兽医研究所, 北京 100193
2. Beijing Institute of Animal Science and Veterinary Medicine, Chinese Academy of Agricultural Sciences, Beijing 100193, China
奶牛乳腺健康是牛奶生产的关键问题。因此,对乳腺健康状况的有效监测是提高奶牛场经济效益的重要手段。尽管患有亚临床乳腺炎症的奶牛乳汁在外观上没有明显变化,但由于炎症的发生,乳成分及乳质量已经发生了改变。Forsbäck等[1]报道,在乳腺炎期间酪蛋白(CN)和乳清蛋白含量有所下降。患亚临床乳腺炎奶牛的乳汁中钠、氯化物、白蛋白、免疫球蛋白含量和乳酸脱氢酶活性升高,α-乳清蛋白(α-LA)、β-乳球蛋白(β-LG)、钙、磷和钾含量降低[2]。Yang等[3]在乳腺炎奶牛和健康奶牛的乳腺中检测到的蛋白质表达不同[如血红蛋白、β-酪蛋白(β-CN)、κ-酪蛋白(κ-CN)和色氨酰-tRNA合成酶],这些蛋白质在炎症乳腺乳汁中浓度均较低,而细胞色素C氧化酶和膜联蛋白Ⅴ在乳腺炎奶牛的乳中具有较高丰富度。Boggs等[4]研究发现,在注射大肠杆菌脂多糖后12 h,低浓度炎症标志物(如血清转铁蛋白、纤维蛋白原β链、S100钙结合蛋白A12和抗微生物导管素)在牛奶中的含量升高。
目前,关于早期乳腺炎症奶牛的乳蛋白质组研究较少。Minuti等[5]试验发现,与健康奶牛相比,亚临床乳腺炎奶牛的乳中急性期蛋白(触珠蛋白和血清淀粉样蛋白A)含量增加。Eckersall等[6]研究发现,用脂磷壁酸诱导乳腺感染12 h内观察到奶牛血细胞中细胞因子[肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)、白细胞介素-6(IL-6)和白细胞介素-8(IL-8)]的mRNA表达增加。此外,血液中触珠蛋白和白细胞含量增加。
蛋白质是生理功能的执行者,是生命现象的直接体现者,对蛋白质结构和功能的研究将有助于阐明生命在生理或病理状态下的变化机制。己有研究表明,98%的疾病与蛋白质表达密切相关,病理状态下的细胞蛋白质组与正常生理条件下的存在较大差异,这都需要通过差异蛋白质组学来进行研究和分析。差异蛋白质组学的概念就是针对不同空间、不同时间上动态变化着的蛋白质组的整体进行比较,分析不同蛋白质组之间蛋白质在表达数量、表达水平和修饰状态上的差异,并研究差异蛋白质及其功能[7]。蛋白质组学研究在探索病因、致病机制以及治疗方法中具有重要性。因此,本试验旨在利用蛋白质组学方法,通过对比奶牛不同乳腺健康状态下乳清蛋白表达水平的差异性,从蛋白质功能角度探究炎症发生及病原菌致病机制,同时也为诊断乳腺健康程度以及早期炎症的发生提供潜在生物标记物。
1 材料与方法 1.1 试验设计本试验牛奶样本采集自北京地区3家奶牛养殖场,共102头荷斯坦奶牛[胎次2~3胎、泌乳天数(152±27) d、产奶量(27±3) kg/d]。收集时间为2017年7月5日,共挤奶2次,分别为08:00和19:00。将约50 mL来自每头奶牛3个乳区的混合奶样收集在无菌管中,随后将牛奶样本分装成3个子样本,分别用于牛奶乳体细胞数(SCC)检测、细菌学鉴定及蛋白质组学检测,最后将所有样本储存于-80 ℃冰箱中。根据SCC检测及细菌学鉴定结果将乳样本分为6组,分别为细菌培养阳性组(传染型、环境型和机会型)和细菌培养阴性组[培养阴性-低SCC组(培养阴性-L组,SCC < 100 000个/mL)、培养阴性-中等SCC组(培养阴性-M组,SCC为100 000~400 000个/mL)和培养阴性-高SCC组(培养阴性-H组,SCC>400 000个/mL)],并对6组乳清样本中的蛋白质功能及表达水平进行鉴定。
1.2 检测指标及检测方法 1.2.1 牛奶SCC检测使用Fossomatic 5000(Foss Electric公司,丹麦)获得SCC,并进行分组,分别为低SCC组(SCC < 100 000个/mL)、中等SCC组(SCC为100 000~400 000个/mL)、高SCC组(SCC>400 000个/mL)。
1.2.2 牛奶细菌学鉴定分别将每个牛奶样本10 μL涂布到含有5%脱纤维蛋白绵羊血液的血琼脂平板(YA1190,北京索莱宝科技有限公司)和麦康凯琼脂平板(ICP-03N-1,北京索莱宝科技有限公司)。将平板在(37±1) ℃下有氧培养并在24和48 h后检查。革兰氏阳性菌通过过氧化氢酶反应分化为葡萄球菌和链球菌。使用绵羊血浆中的凝固酶试管用于区分金黄色葡萄球菌(Staphylococcus aureus)与凝固酶阴性葡萄球菌(CNS)。通过氧化酶测试以及麦康凯琼脂和曙红亚甲基蓝琼脂上的生长特征鉴定革兰氏阴性细菌[8]。
PCR反应简易模板的制备:直接挑取单菌体溶于100 μL高纯水中,在沸水中煮1 min裂解菌体,使DNA释放出来,直接作为PCR反应的模板。
PCR反应与结果分析:在25 μL的PCR反应体系中,DNA模板用量约为30 ng。PCR反应条件:95 ℃预变性7 min,94 ℃变性1 min,52 ℃退火1 min,65 ℃延伸8 min,30个循环,65 ℃最后延伸16 min,4 ℃停止反应。用1.5%琼脂糖凝胶电泳(北京六一仪器厂)检测PCR产物,用全自动数码凝胶图像分析系统(Tanon-3500R,上海天能科技有限公司)照相。用Bray-Curtis法进行聚类分析[9]。
1.2.3 蛋白质浓度测定蛋白质浓度测定参考碧云天二喹啉甲酸(BCA)蛋白浓度测定试剂盒,如表 1所示,取1.2 mL蛋白质标准配制液加入到1管蛋白质标准[30 mg牛血清蛋白(BSA)]中,充分溶解后配制成25 mg/mL的蛋白质标准溶液。取适量25 mg/mL蛋白质标准,稀释至终浓度为0.5 mg/mL。根据样本数量,按50体积BCA试剂A加1体积BCA试剂B,配制适量BCA工作液,充分混匀。将标准品按0、1、2、4、8、12、16、20 μL加到96孔板孔中,加稀释液补足到20 μL。加适当体积样本到96孔板的样本孔中,加标准品稀释液到20 μL。各孔加入200 μL BCA工作液,37 ℃放置20~30 min, 测定540~595 nm之间的波长。根据标准曲线计算出样本的蛋白质浓度。
|
|
表 1 蛋白质浓度测定所需试剂 Table 1 Reagents for protein concentration determination |
取10 mL牛奶样本,4 ℃、3 000×g离心20 min(Beckman Coulter AvantiJ-26XX离心机,美国)。取1 mL脱脂乳加入30 μL 33%的乙酸(分析纯,天津市大茂化学试剂厂),振荡混匀。室温放置10 min,在上述混合液中加入30 μL 3.3 mol/L的乙酸钠,混匀后,使用台式快速离心机(LNG-T88,太仓市华美生化仪器厂)20 ℃、14 000×g离心30 min。超速离心后,将样本分离成3相,分离中间层的乳清液,-20 ℃保存,用于蛋白质组学样本制备[10]。
1.2.4.2 十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)使用SDS-PAGE进一步分离纯化乳清蛋白。配制12%的分离胶,将分离胶注入玻璃板夹层中,上部用MilliQ水封面,保持胶面平整,待分离胶聚合后,配制5%浓缩胶。配制好浓缩胶后,倒去分离胶表面的少量水分,然后灌入浓缩胶,插入点样梳。将待分析鉴定的蛋白质样本中加入1/4样本体积的5×SDS-PAGE上样缓冲液(2148398AX,北京艾德莱生物科技有限公司),100 ℃水浴3~5 min。在电泳槽加入电泳缓冲液后,拔去上样梳,关闭电源。牛奶样本的上样蛋白质含量为18 μg,加样量为每孔30 μL。加样完毕后,接通电源,起始时用的低电流或低电压(80 V较为适宜),待样本在浓缩胶部分浓缩成一条线后,再加大电流(或电压)(120 V较为适宜),待溴酚蓝指示剂达到底部边缘时即可停止电泳。将电泳结束后的凝胶,用考马斯亮蓝G-250(C8420,北京索莱宝科技有限公司)染色,室温染色4~6 h。再将胶块取出,放入脱色液中,多次脱色至蛋白质条带清晰[11]。
1.2.4.3 还原烷基化及酶解本试验中使用的所有碳酸氢铵(NH4HCO3,0.05 mol/L)缓冲液pH均为8。将样本超声处理1 min,然后离心。使用解剖刀将每个样本的凝胶泳道切成8片,每个切片切成1~3 mm,并转移到低结合微量离心管(0030 108.094,德国)。在0.05 mol/L二硫苏糖醇中60 ℃条件下温育1 h将蛋白质还原,然后在室温下在黑暗中在0.1 mol/L碘乙酰胺中孵育1 h。甲酰胺甲基化后,将凝胶片用0.05 mol/L ABC缓冲液洗涤3次。然后将凝胶片冷冻并解冻3次以增加胰蛋白酶的可接近性。将样本在20 μL新鲜制备的胰蛋白酶溶液(10 ng/μL)中再水合。加入额外的0.05 mol/L ABC缓冲液以在室温下孵育过夜后将消化液的上清液转移到干净的低结合的离心管中。将每次超声处理后的上清液加入到相同的低结合微量离心管中[12]。使用pH纸检查肽混合物的最终pH。
1.2.4.4 液相色谱-串联质谱(LC-MS/MS)分析将总共18 μL的胰蛋白酶消化的牛奶级分在最大压力为27 000 kPa的0.10 mm×30.00 mm Magic C18AQ 200A5 μm微珠(Michrom Bioresources Inc.,美国)预浓缩柱(室内制备)中注射。将肽从预浓缩柱洗脱到0.10 mm×200.00 mm Prontosil 300-3-C18H分析柱(Prontosil Bischoff,德国)上,乙腈梯度以0.5 μL/min的流速洗脱,在3 min内,将乙腈增加至80%(在乙腈和水中用20%水和0.5%乙酸)洗涤该柱。在预浓缩和分析柱之间,通过固定在P777 Upchurch微胶(IDEX,美国)固体0.5 mm平板上的电极将3.5 kV的电喷雾电压直接施加到洗脱液上。在LTQOrbitrap XL(Thermo Electron,美国)上,测量全扫描正模式傅立叶变换质谱(FTMS)光谱。在线性阱(MS/MS阈值=5 000)中,以数据依赖模式记录FTMS扫描中4个最丰富的双重和三重电峰的碰撞诱导解离(collision-induced dissociation,CID)碎片[13]。
1.3 数据分析本试验使用Student’s t检验评估样本之间的统计学差异,P < 0.05为差异显著。质谱数据通过R version 3.2.1(https://cran.r-project.org/src/base/R-3/)软件进行分析,生物信息学分析使用UniProt知识库[14]。蛋白质功能分析数据库如下:GO功能分类注释blast2go(http://www.blast2go.com/b2ghome),KEGG注释通路分析KEGG:Kyoto Encyclopedia of Genes and Genomes(http://www.genome.jp/tools/kaas/),火山图R version 3.2.1(https://cran.r-project.org/src/base/R-3/),差异蛋白质GO分类blast2go(http://www.blast2go.com/b2ghome),差异蛋白质表达模式聚类分析R gplots package (https://cran.r-project.org/web/packages/gplots/),差异蛋白质互作网络分析(http://string-db.org/)。
2 结果与分析 2.1 牛奶中的SCC由表 2可知,102份牛奶样本中,有44份奶样SCC < 100 000个/mL,为低SCC组;有28份奶样SCC在100 000 ~ 400 000个/mL之间,为中等SCC组;有30份奶样SCC>400 000个/mL,为高SCC组。
|
|
表 2 牛奶样本中的SCC Table 2 SCC in milk samples (n=102) |
试验检测的102份牛奶样本中,有13.72%的样本细菌培养结果呈阴性,83.34%样本细菌培养结果呈阳性,有3个样本受到污染(培养皿中生长杂菌)。根据引起奶牛乳腺炎病原菌的种类、对乳腺的亲和力、在牛群中的传播特方式等特点,将分离鉴定的病原菌分类为传染型、环境型和机会型[15]。由表 3可知,在培养阳性的样本中,机会型病原体为CNS(占总样本的34.32%,占培养样本的39.77%),而感染CNS的奶样中平均SCC为71 850个/mL;传染型病原体(占总样本的27.45%,占培养样本的31.81%)中金黄色葡萄球菌和无乳链球菌(Streptococcus agalactiae)是最主要的病原体,感染传染型病原体的奶样中平均SCC为824 280个/mL;环境型病原体(占总样本的21.57%,占培养样本的25.00%)包括变形菌属(Proteus spp.)、绿脓杆菌(Pseudomonas)、肺炎克雷伯杆菌(Klebsiella)、芽孢杆菌(Bacillus)、大肠杆菌(Escherichia coli)、乳酸乳球菌(Lactococcus lactis)等,感染环境型病原体的奶样中平均SCC为338 670个/mL。
|
|
表 3 牛奶样本中的细菌鉴定及分类 Table 3 Identification and classification of bacteria in milk samples (n=102) |
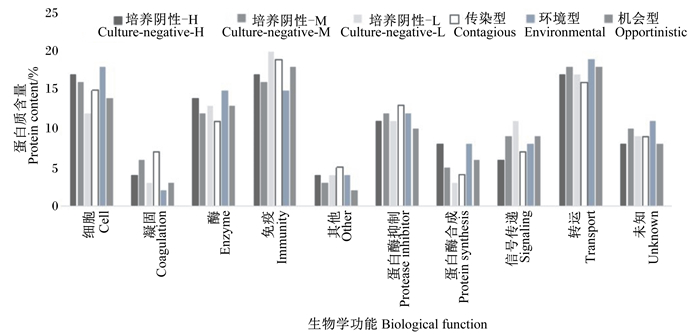
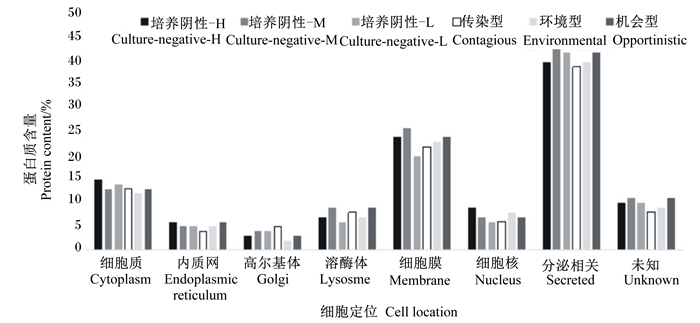
在102份乳清样本中总共鉴定出272种蛋白质。使用超视频数据(DAVID)鉴定奶样中蛋白质的生物学功能及其细胞定位。如图 1所示,所鉴定的蛋白质功能多数与免疫、转运、细胞功能(包括细胞黏附、细胞迁移、细胞生长和细胞凋亡)或酶有关。如图 2所示,蛋白质所在细胞定位,其中3个主要组织,即分泌组织、细胞膜和细胞质中蛋白质比例之和占总蛋白质的80%以上。分泌组织是主要的蛋白质所在地,蛋白质含量约45%。由图 1和图 2可知,基于其生物学功能和细胞定位鉴定的蛋白质数量与乳腺健康状态没有呈现明显相关性。
|
图 1 不同乳腺健康状态下牛奶样本中蛋白质功能分类 Fig. 1 Functional classification of proteins in milk samples under different mammary health conditions |
|
图 2 不同乳腺健康状态选的牛奶样本中蛋白质的细胞定位 Fig. 2 Cellular localization of proteins in milk samples selected under different mammary health conditions |
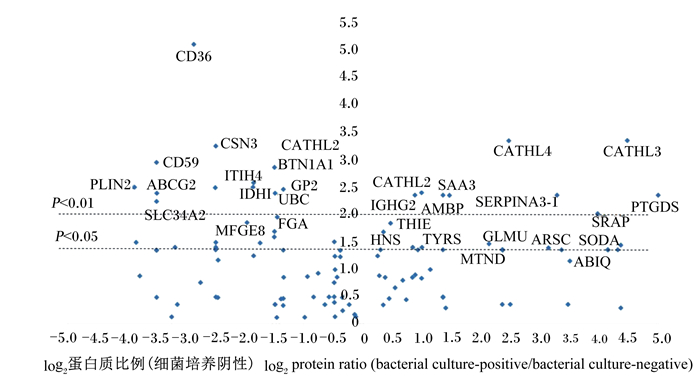
尽管在蛋白质鉴定前已将所有牛奶样本的总蛋白浓度调整一致,但鉴定结果发现,与培养阴性样本相比,培养阳性样本组间中有58种蛋白质的表达水平呈现出显著差异(P < 0.05),如表 4和图 3所示,其中38种蛋白质的表达下调,其中血小板糖蛋白4(CD36)、补体蛋白CD59(CD59)、κ酪蛋白(CSN3)、嗜乳脂蛋白亚家族1成员A1(BTN1A1)、ATP结合盒转运蛋白G2(ABCG2)、围脂滴蛋白2(PLIN2)、包膜糖蛋白2(GP2)、聚泛素-C(UBC)和异柠檬酸脱氢酶1(IDH1)的表达呈现极显著下调(P < 0.01)。其余20种蛋白质表达显著上调(P < 0.05),其中导管素-4(CATHL4)、导管素-3(CATHL3)、导管素-2(CATHL2)、α-球蛋白抑制因子H4(ITIH4)、丝氨酸蛋白酶抑制剂A3-1(SERPINA3-1)、前列腺素H-2 D异构酶(PTGDS)、血清淀粉样蛋白A3(SAA3)和免疫球蛋白κv3-20(IGKV3-20)在培养阳性样本中的表达量超过培养阴性样本的约8倍。由表 3可知,在这些上调的蛋白质中,大多数与免疫系统有关,如CATHL2、CATHL3、CATHL4、IGKV3-20、PTGDS和乳铁蛋白(LTF)。在显著下调的蛋白质中,BTN1A1与脂质合成和分泌有关,PLIN2和GP2与转运有关,ABCG2具有酶活性,乳凝集素(MFGE8)参与细胞凋亡,CD59与免疫系统有关。
|
|
表 4 细菌培养样阳性样本中差异显著表达蛋白质列表 Table 4 List of significant differentially expressed proteins in bacterial culture-positive versus bacterial culture-negative milk samples |
|
图 3 细菌培养样阳性与细菌培养阴性奶样之间差异显著表达蛋白 Fig. 3 Differentially expressed protein between bacterial culture-positive and bacterial culture-negative milk samples |
由表 5可知,在细菌培养阳性奶样中检测到21种菌体蛋白。其中显著上调的菌体蛋白包括砷酸还原酶(ARSC)、DNA结合蛋白H-NS(HNS)、基转移酶Cfr(cfr)、超氧化物歧化酶[Mn/Fe](SODA)、Ⅲ型输出蛋白质pscF(pscF)(P < 0.05),上调极显著的菌体蛋白包括血小板富含丝氨酸的黏附素(SRAP)、胸苷酸合成酶(THIE)、双功能AAC/APH(aacA-aphD)(P < 0.01)。此外,在所有鉴定到的菌体蛋白中,所属CNS的菌体蛋白占比最多,达到36.84%,其次是金黄色葡萄球菌菌体蛋白(19.14%)。这些菌体蛋白的主要功能包括吸附、物质转运、免疫保护、细菌合成以及免疫原性。其中,多数菌体蛋白发挥了细胞吸附(30.8%)、免疫原性(22.5%)和细菌合成(21.1%)的分子功能。
|
|
表 5 细菌培养阳性奶样中差异表达显著的菌体蛋白 Table 5 Differentially expressed bacterial proteins in bacterial culture-positive milk samples |
在细菌培养阴性奶样中,根据不同SCC将样本分为3组,即细菌培养阴性-H组(SCC>400 000个细胞/mL)、细菌培养阴性-M组(100 000 < SCC < 400 000个/mL)和细菌培养阴性-L组(SCC < 100 000个细胞/mL),对3组样本中的差异表达蛋白质进行鉴定。由表 6可知,在高SCC的奶样中,显著上调表达的蛋白质多数为特异性免疫相关蛋白质(如LTF、CATHL2、CATHL3、PTGDS和IGKV3-20)以及蛋白酶抑制剂[如SERPINA3-1、肌动蛋白细胞质1(ACTB)和丝氨酸蛋白酶抑制剂1(SERPINA1)]。在7种显著下调表达的蛋白质中,多数发挥非免疫应答相关功能。其中BTN1A1、载脂蛋白A-Ⅳ(APOA4)和PLIN2与脂质代谢功能有关,IDH1与具有催化活性,MFGE8可介导吞噬细胞凋亡,α-乳清蛋白(LALBA)和CSN3与乳蛋白合成有关。
|
|
表 6 细菌培养阴性奶样中不同SCC水平奶样中显著调节差异表达蛋白质 Table 6 Significant regulation of differentially expressed proteins in different SCC levels in bacterial culture-negative milk samples |
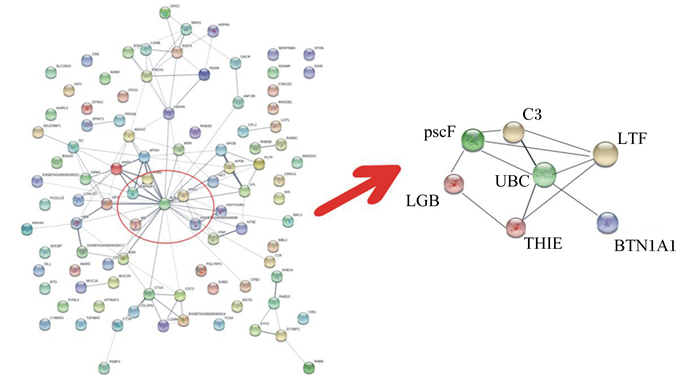
由图 4可知,在复杂的蛋白质互作网络图中β-乳球蛋白(LGB)、LTF、THIE、BTN1A1、C3、pscF和UBC这7蛋白质之间紧密连接。通过GO功能注释分析发现这些互作关系紧密的蛋白质大多与免疫应答相关。
|
图 4 细菌培养阳性组和培养阴性组之间差异表达的蛋白质的相互作用 Fig. 4 Interaction of differentially expressed proteins between bacterial culture-positive group and bacterial culture-negative group |
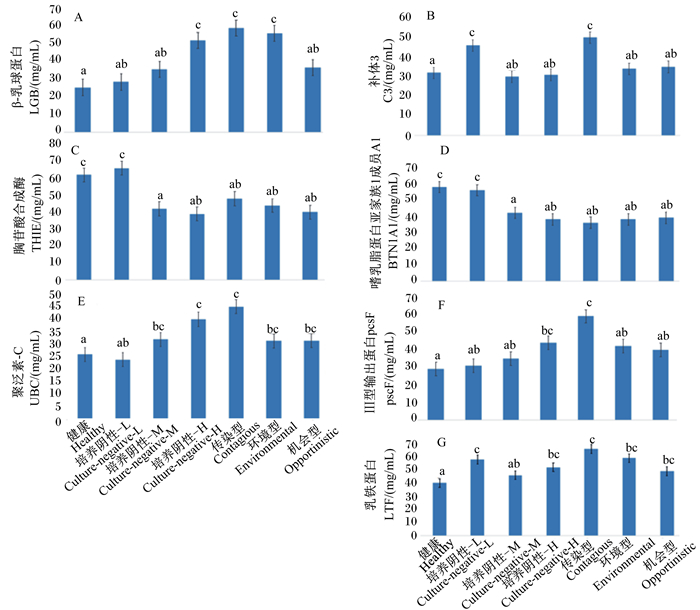
由图 5可见,与健康组相比,传染型病原体感染的奶样中UBC、LGB、C3、LTF和pscF这5种蛋白质表达量显著增加(P < 0.05),而环境型病原体感染的奶样中只有LBG和LTF这2种蛋白质表达量显著增加(P < 0.05);机会型病原体感染的奶样中只有UBC和LTF这2种蛋白质表达显著增加(P < 0.05);C3和LTF在培养阴性-L组中表达量显著增加(P < 0.05)。
|
数据柱标相同小写字母表示差异不显著(P>0.05),不同小写字母表示差异显著(P<0.05)。 Value columns with the same small letter mean no significant difference (P > 0.05), while with different small letters mean significant difference (P < 0.05). 图 5 紧密互作蛋白在不同乳腺状态组中的差异表达 Fig. 5 Differential expression of tightly interacting proteins in different breast state groups |
本试验在细菌培养阳性样本中鉴定到21种菌体蛋白。Typas等[16]报道指出,菌体蛋白在细菌代谢物质的运输、维持细菌形态以及调节细菌有关物质的合成方面起到重要作用。姚远等[17]研究发现,大肠杆菌BtuB基因编码的蛋白质与菌体的代谢相关。大肠杆菌ompA蛋白具有维持菌体结构和新陈代谢方面的作用。本试验中,显著上调表达的克雷伯菌(mtnD)和乳酸链球菌(ABIQ)菌体蛋白具有细菌DNA合成以及信号转导的功能。
研究表明,菌体蛋白具有免疫原性,不仅可以刺激体液免疫,而且对细胞免疫也有刺激作用[18]。本试验中,显著上调表达的ARSC和HNS均属于金黄色葡萄球菌菌体蛋白,ARSC与感染有关,通过T细胞介导途径促进免疫应答。HNS对淋巴细胞具有较高的多克隆激活作用,同时具有较强的细胞免疫能力。李雷等[19]研究指出,菌体蛋白的致病作用是通过3方面实现的,即细胞吸附、穿越防御屏障和免疫防御的逃逸。大多数的感染中,病原微生物只有吸附在机体组织上才能致病。Battesti等[20]研究发现,大肠杆菌是通过菌毛吸附气管上皮细胞从而实现入侵的第一步。本试验中,显著上调表达的pscF是绿脓杆菌菌体蛋白,对巨噬细胞有强大的吸附作用,并随之对巨噬细胞产生细胞毒性,破坏其吞噬作用;显著上调表达的cfr和极显著上调表达的aacA-aphD均属于CNS菌体蛋白。cfr具有较强的细胞黏附力,进而引发宿主血管内毒力感染。aacA-aphD通过菌毛吸附在乳腺上皮细胞,进而在正常细胞内产生对生物系统有毒的超氧阴离子自由基,与细胞内羟基(-OH)结合后的产物会导致细胞DNA损坏,破坏奶牛乳腺上皮细胞功能[21]。
Dilucca等[22]研究表明,菌体蛋白有助于细菌通过防御屏障。本试验中,SODA属于CNS菌体蛋白,它参与细菌染色体组织的形成,并能够诱导侵入细菌蛋白的传播。本研究中,极显著上调表达的SRAP(金黄色葡萄球菌菌体蛋白)对血清的杀菌作用具有抵抗力;THIE(CNS菌体蛋白)对庆大霉素、妥布霉素和卡那霉素等具有抗性;ABIQ(乳酸链球菌菌体蛋白)除了参与细菌合成,还是Ⅲ型毒素-抗毒素(TA)的有毒成分,在抑制剂存在的条件下,仍能保护菌株生长,进而引起流产感染[23]。
3.2 乳清样本中的上调表达蛋白本试验研究表明,在58种显著调节的蛋白中,除菌体蛋白外,有11种蛋白表达显示出4倍以上的上调变化。与培养阴性-L组相比,培养阴性-H组的乳清样本中显著上调的蛋白质中,3种蛋白质是导管素(CATHL2、CATHL3、CATHL4),其表达量在乳清样本中显著增加,这一结果在大肠杆菌诱导乳房炎奶牛乳样本中被发现。这可能与导管胶原蛋白以及它们的抗微生物活性在调节先天和适应性免疫应答中的作用有关[24]。免疫球蛋白(IGHG2和IGKV3-20)和急性期蛋白(SAA3和ITIH4)在细菌培养阳性乳清样本和培养阴性-H乳清样本中显著增加,与前人研究结果[25]一致。Chiaradia等[26]在研究高SCC对牛奶蛋白质变化影响时指出,与低SCC组奶样相比,高SCC奶样中,结合珠蛋白(HP)和LTF显著上调。HP是急性期反应蛋白,当机体处在应激状态(如肿瘤、炎症、创伤、感染等病理状态)时,血液中的HP含量明显增多,因此HP可作为乳腺炎症的诊断指标。LTF是主要的铁结合蛋白质,参与乳汁分泌,具有抗菌活性,对大肠杆菌和铜绿假单胞菌可见最有效的活性抑制力[27]。
本试验研究发现,蛋白酶抑制剂[SERPINA3-1和色氨酸-tRNA连接酶细胞质(WARS)]在调节嗜中性粒细胞的蛋白酶活性中起重要作用。Bobbo等[28]研究证明,SERPINA3-1可以保护组织免受可能由感染期间嗜中性粒细胞分泌的蛋白酶引起的损伤。因此,高SCC乳清样本中SERPINA3-1表达量的增加可能与乳腺细胞的保护有关。而C3作为慢性炎症中性粒细胞的化学引诱物,其在细菌培养阳性和培养阴性-H乳清样本中显著上调表达,标志着炎症程度的加剧,因此C3同样可作为乳腺内感染(IMI)的诊断标志物[29]。
3.3 乳清样本中的下调表达蛋白本试验结果显示,在细菌培养阴性乳清样本中有10种表达蛋白下调超过2倍,其中有7种表达蛋白在培养阴性-H乳清样本中显著下调。大多数下调的蛋白质与非免疫保护的其他生物学功能相关,例如CD36、BTN1A1和PLIN2参与脂质代谢。Petersen等[30]研究表明,APOA4能够调节乳糜微粒和极低密度脂蛋白的分泌与分解代谢。Piccinini等[31]报道,BTN1A1除了能够调节乳脂分泌,还能激活CD4和CD8 T淋巴细胞的增殖。PLIN2可参与脂肪组织发育和维持。在具有乳腺炎症的奶牛的乳汁中这些蛋白质的下调,表明乳脂率受损。
在本试验结果中,LALBA和CSN3在细菌培养阳性和培养阴性-H乳清样本中显著下调。Järvinen等[32]研究指出,α-乳白蛋白是唯一能结合钙的乳清蛋白,是必需氨基酸和支链氨基酸的极好来源,其中必需氨基酸占63.2%。α-乳白蛋白具有与乳糖合成有关的乳糖产生和乳分泌的基本功能。乳腺内炎症的发生,特别是一些菌体蛋白的活性增强,破坏了泌乳时乳糖合成酶系(β-半乳糖苷基转移酶-1和α-乳白蛋白),导致乳糖合成受损。补体调节蛋白CD59可以保护乳腺免受过度活化的补体介导的细胞裂解和组织损伤[33],高SCC的牛奶中CD59含量的降低表明其在炎症期间对乳腺的保护作用减弱。MFGE8介导凋亡上皮细胞的吞噬作用。
3.4 几种紧密互作蛋白质在不同乳腺健康状态组中的差异表达与健康组相比,传染型病原体感染的奶样中UBC、LGB、C3、LTF和pscF这5种蛋白质表达量显著增加,而环境型病原体感染的奶样中只有LBG和LTF这2种蛋白质表达量显著增加。其中C3、LGB和LTF与中性粒细胞(PMN)的合成与吞噬功能相关,这些蛋白质浓度的增多代表抗菌活性和免疫反应的活跃程度[34];UBC参与核因子-κB(NF-κB)通路激活与信号转导,说明其所在机体内强烈的炎症反应过程。机会型病原体感染的奶样中只有THIE和LTF这2种蛋白质表达显著增加,THIE所属CNS菌体蛋白,其强大的免疫保护功能能够帮助CNS逃逸免疫防御,抑制吞噬作用[35]。感染机会型病原体的奶样中未观察到LGB等免疫球蛋白的显著变化,可能的原因为CNS通常在乳房皮肤上发现,一些培养阳性结果可能是由于在收集复合奶样时的乳头皮肤污染而不是真正的乳腺内感染[36]。BTN1A1蛋白主要激活CD4和CD8 T淋巴细胞增殖,BTN1A1蛋白只在健康组和培养阴性-L组中表达较高,而在高SCC组和培养阳性奶样中表达较低。
C3和LTF蛋白在培养阴性-L组中表达显著增加,说明即使在低SCC的乳区内,血液和乳腺中的PMN逐渐募集到感染或创伤乳腺部位,此时慢性炎症很可能已经开始发生[37]。此外THIE蛋白在培养阴性-L组乳样中被检测到,这一结果证明,即使通过细菌培养鉴定技术并没有鉴定到病原微生物的存在,但蛋白质鉴定结果表明CNS菌体蛋白(THIE)已经存在于乳区内,只是CNS存在量低于细菌鉴定检测最低限度,或是由于试验所分析的牛奶样本是4个乳区的复合乳,因而存在健康乳区的稀释效应[38]。
4 结论本试验结果表明,通过对奶牛不同乳腺炎症状态下乳清蛋白差异表达的研究,分析诱发乳腺炎症病原菌的种类,将炎症分为不同类型,进而根据不同炎症类型奶样中乳清蛋白及菌体蛋白的表达变化及功能揭示了不同乳腺炎症状态下乳腺内的生物学现象,为诊断乳腺健康特别是早期乳腺炎症的发生提供潜在生物标记物。
| [1] |
FORSBÄCK L, LINDMARK-MÅNSSON H, ANDRÉN A, et al. Evaluation of quality changes in udder quarter milk from cows with low-to-moderate somatic cell counts[J]. Animal, 2010, 4(4): 617-626. |
| [2] |
BATAVANI R A, ASRI S, NAEBZADEH H. The effect of subclinical mastitis on milk composition in dairy cows[J]. Iranian Journal of Veterinary Research, 2007, 8(3): 205-211. |
| [3] |
YANG Y X, ZHAO X X, ZHANG Y. Proteomic analysis of mammary tissues from healthy cows and clinical mastitic cows for identification of disease-related proteins[J]. Veterinary Research Communications, 2009, 33(4): 295-303. DOI:10.1007/s11259-008-9177-0 |
| [4] |
BOGGS I, HINE B, SMOLENSKI G, et al. Changes in the repertoire of bovine milk proteins during mammary involution[J]. EuPA Open Proteomics, 2015, 9: 65-75. DOI:10.1016/j.euprot.2015.09.001 |
| [5] |
MINUTI A, ZHOU Z, GRAUGNARD D E, et al. Acute mammary and liver transcriptome responses after an intramammary Escherichia coli lipopolysaccharide challenge in postpartal dairy cows[J]. Physiological Reports, 2015, 3(4): e12388. DOI:10.14814/phy2.12388 |
| [6] |
ECKERSALL P D, YOUNG F J, NOLAN A M, et al. Acute phase proteins in bovine milk in an experimental model of Staphylococcus aureus, subclinical mastitis[J]. Journal of Dairy Science, 2006, 89(5): 1488-1501. DOI:10.3168/jds.S0022-0302(06)72216-0 |
| [7] |
BOEHMER J L, BANNERMAN D D, SHEFCHECK K, et al. Proteomic analysis of differentially expressed proteins in bovine milk during experimentally induced Escherichia coli mastitis[J]. Journal of Dairy Science, 2008, 91(11): 4206-4218. DOI:10.3168/jds.2008-1297 |
| [8] |
SHOME B R, DAS MITRA S, BHUVANA M, et al. Multiplex PCR assay for species identification of bovine mastitis pathogens[J]. Journal of Applied Microbiology, 2011, 111(6): 1349-1356. DOI:10.1111/j.1365-2672.2011.05169.x |
| [9] |
田梅, 沈静. 实时荧光定量PCR法与常规细菌鉴定法检测肠道致病菌的比较[J]. 中国微生态学杂志, 2015, 27(10): 1221-1223, 1237. |
| [10] |
TURK R, PIRAS C, KOVAČIĆ M, et al. Proteomics of inflammatory and oxidative stress response in cows with subclinical and clinical mastitis[J]. Journal of Proteomics, 2012, 75(14): 4412-4428. DOI:10.1016/j.jprot.2012.05.021 |
| [11] |
VOHR H W. Encyclopedic reference of immunotoxicology[M]. Heidelberg: Springer, 2005.
|
| [12] |
JIAO F, ZHANG D, JIANG M, et al. Label-free proteomic analysis of placental proteins during Toxoplasma gondii infection[J]. Journal of Proteomics, 2017, 150: 31-39. DOI:10.1016/j.jprot.2016.08.013 |
| [13] |
COX J, HEIN M Y, LUBER C A, et al. Accurate proteome-wide label-free quantification by delayed normalization and maximal peptide ratio extraction, termed MaxLFQ[J]. Molecular & Cellular Proteomics, 2014, 13(9): 2513-2526. |
| [14] |
JIAN F W, XING X Z, YONG Z, et al. Proteomic analysis of nuclei of mammary tissue from healthy cows and clinical mastitic cows[J]. Journal of Animal and Veterinary Sciences, 2010. DOI:10.1088/1674-4527/10/12/011 |
| [15] |
SAFI S, KHOSHVAGHTI A, JAFARZADEH S R, et al. Acute phase proteins in the diagnosis of bovine subclinical mastitis[J]. Veterinary Clinical Pathology, 2009, 38(4): 471-476. DOI:10.1111/vcp.2009.38.issue-4 |
| [16] |
TYPAS A, SOURJIK V. Bacterial protein networks:properties and functions[J]. Nature Reviews Microbiology, 2015, 13(9): 559-572. DOI:10.1038/nrmicro3508 |
| [17] |
姚远, 李攀, 韩冰, 等. 大肠杆菌TorR蛋白对基因entA、sufA、speA和yhiD的表达调控作用[J]. 基因组学与应用生物学, 2017, 36(2): 661-669. |
| [18] |
朱杰.致病基因和细菌蛋白质亚细胞分布的预测方法研究[D].博士学位论文.上海: 上海师范大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10270-1016126142.htm
|
| [19] |
李雷, 卫科科, 姜卫红, 等. 细菌双组分系统应答调控蛋白调控策略的多样性[J]. 中国科学(生命科学), 2017, 47(5): 462-469. |
| [20] |
BATTESTI A, BOUVERET E. The bacterial two-hybrid system based on adenylate cyclase reconstitution in Escherichia coli[J]. Methods, 2012, 58(4): 325-334. DOI:10.1016/j.ymeth.2012.07.018 |
| [21] |
CAUFIELD J H, WIMBLE C, SHARY S, et al. Bacterial protein meta-interactomes predict cross-species interactions and protein function[J]. BMC Bioinformatics, 2017, 18: 171. DOI:10.1186/s12859-017-1585-0 |
| [22] |
DILUCCA M, CIMINI G, GIANSANTI A.Topological transition in bacterial protein-protein interaction networks ruled by gene conservation, essentiality and function[J/OL].[2018-07-01].http://arxiv.org/pdf/1708.02299
|
| [23] |
GÓMEZ M I, LEE A, REDDY B, et al. Staphylococcus aureus protein A induces airway epithelial inflammatory responses by activating TNFR1[J]. Nature Medicine, 2004, 10(8): 842-848. DOI:10.1038/nm1079 |
| [24] |
KOVÁCS K, HURST L D, PAPP B. Stochasticity in protein levels drives colinearity of gene order in metabolic operons of Escherichia coli[J]. PLoS Biology, 2009, 7(5): e1000115. DOI:10.1371/journal.pbio.1000115 |
| [25] |
LU J, FERNANDES E A, CANO A E P, et al. Changes in milk proteome and metabolome associated with dry period length, energy balance, and lactation stage in postparturient dairy cows[J]. Journal of Proteome Research, 2013, 12(7): 3288-3296. DOI:10.1021/pr4001306 |
| [26] |
CHIARADIA E, VALIANI A, TARTAGLIA M, et al. Ovine subclinical mastitis:proteomic analysis of whey and milk fat globules unveils putative diagnostic biomarkers in milk[J]. Journal of Proteomics, 2013, 83: 144-159. DOI:10.1016/j.jprot.2013.03.017 |
| [27] |
SCHRICK F N, HOCKETT M E, SAXTON A M, et al. Influence of subclinical mastitis during early lactation on reproductive parameters[J]. Journal of Dairy Science, 2001, 84(6): 1407-1412. DOI:10.3168/jds.S0022-0302(01)70172-5 |
| [28] |
BOBBO T, RUEGG P L, STOCCO G, et al. Associations between pathogen-specific cases of subclinical mastitis and milk yield, quality, protein composition, and cheese-making traits in dairy cows[J]. Journal of Dairy Science, 2017, 100(6): 4868-4883. DOI:10.3168/jds.2016-12353 |
| [29] |
BAEKER R, HAEBEL S, SCHLATTERER K, et al. Lipocalin-type prostaglandin D synthase in milk:a new biomarker for bovine mastitis[J]. Prostaglandins & Other Lipid Mediators, 2002, 67(1): 75-88. |
| [30] |
PETERSEN H H, NIELSEN J P, HEEGAARD P M H. Application of acute phase protein measurements in veterinary clinical chemistry[J]. Veterinary Research, 2004, 35(2): 163-187. DOI:10.1051/vetres:2004002 |
| [31] |
PICCININI R, BINDA E, BELOTTI M, et al. The evaluation of non-specific immune status of heifers in field conditions during the periparturient period[J]. Veterinary Research, 2004, 35(5): 539-550. DOI:10.1051/vetres:2004030 |
| [32] |
JÄRVINEN K M, CHATCHATEE P, BARDINA L, et al. IgE and IgG binding epitopes on α-lactalbumin and β-lactoglobulin in cow's milk allergy[J]. International Archives of Allergy and Immunology, 2001, 126(2): 111-118. DOI:10.1159/000049501 |
| [33] |
KAWAI T, AKIRA S. Toll-like receptors and their crosstalk with other innate receptors in infection and immunity[J]. Immunity, 2011, 34(5): 637-650. DOI:10.1016/j.immuni.2011.05.006 |
| [34] |
BRUMINI D, CRISCIONE A, BORDONARO S, et al. Whey proteins and their antimicrobial properties in donkey milk:a brief review[J]. Dairy Science & Technology, 2016, 96(1): 1-14. |
| [35] |
WELLNITZ O, BRUCKMAIER R M. The innate immune response of the bovine mammary gland to bacterial infection[J]. The Veterinary Journal, 2012, 192(2): 148-152. DOI:10.1016/j.tvjl.2011.09.013 |
| [36] |
BARBOSA B F, SILVA D A O, COSTA I N, et al. Bewo trophoblast cell susceptibility to Toxoplasma gondii is increased by interferon-γ, interleukin-10 and transforming growth factor-β[J]. Clinical & Experimental Immunology, 2008, 151(3): 536-545. |
| [37] |
YONG X Y, YONG Z, LEI Z, et al. Comparative proteomic analysis of membrane proteins of mammary gland between clinical healthy and mastitic cows[J]. Scientia Agricultura Sinica, 2010. DOI:10.1097/MOP.0B013E3283423F35 |
| [38] |
KULAK N A, PICHLER G, PARON I, et al. Minimal, encapsulated proteomic-sample processing applied to copy-number estimation in eukaryotic cells[J]. Nature Methods, 2014, 11(3): 319-324. DOI:10.1038/nmeth.2834 |




