2. 湖南畜禽安全生产协调创新中心, 长沙 410128;
3. 中国科学院亚热带农业生态研究所, 长沙 410125;
4. 华南农业大学动物科学学院, 广州 510640
2. Hunan Co-Innovation Center of Animal Production Safety, Changsha 410128, China;
3. Institute of Subtropical Agriculture, Chinese Academy of Sciences, Changsha 410125, China;
4. College of Animal Science, South China Agriculture University, Guangzhou 510640, China
近年来,我国的小麦和水稻播种面积分别超过2亿和3亿hm2[1]。小麦和水稻秸秆可为反刍家畜提供粗饲料,但小麦和水稻秸秆细胞壁的主要成分为纤维素、半纤维素和木质素[2],而木质素不能被瘤胃微生物降解,并且木质素与纤维素和半纤维素偶联,阻碍瘤胃微生物对纤维素和半纤维的降解[3-4]。只有破坏木质素结构,降低木质素纤维化程度,才有利于提高秸秆的瘤胃降解和饲用价值[5]。
甲烷是瘤胃内碳水化合物无氧酵解的代谢终产物,也是反刍家畜消化饲粮过程中的能量损失,占饲粮总能的2%~12%[6]。另外,甲烷还是重要的温室气体,对全球温室效应的贡献率为15%~20%[7]。因此,降低瘤胃甲烷生成,有助于提高饲粮能量利用效率和缓解全球温室效应。
白腐真菌能够降解秸秆木质素,破坏木质素-纤维素-半纤维素间的偶联结构[8]。不同秸秆细胞壁组成及结构存在差异,白腐真处理对不同秸秆纤维的破坏程度可能不同[9]。Van Kuijk等[10]用白腐真菌中的平菇(Pleurotus ostreatus, P. ostreatus)处理小麦秸秆后降低了木质素含量,而Yang等[11]用平菇处理玉米秸秆没有改变木质素含量。另外,白腐真菌在降解纤维的过程中伴随着次级代谢产物的产生,可能会抑制瘤胃微生物的活性[12],影响秸秆在瘤胃中的降解及甲烷生成。本试验选用平菇接种小麦和水稻秸秆,获取平菇处理小麦和水稻秸秆发酵底物,利用全自动体外模拟瘤胃发酵设备进行72 h发酵试验,研究平菇处理2种秸秆对瘤胃纤维降解、甲烷生成和挥发性脂肪酸含量的影响。
1 材料与方法 1.1 试验材料 1.1.1 体外模拟瘤胃发酵底物试验所用小麦和水稻秸秆分别来自甘肃省和湖南省,所用平菇菌种由湖南农业大学食品科学技术学院提供。试验中对照组的秸秆不作处理,平菇组的秸秆接种平菇42 d。接种过程:将风干秸秆用铡草机切至1.5~2.5 cm长短,在1%(质量体积比)石灰水中浸泡48 h后沥干、装入菌包(1 kg/包),于高压灭菌锅内灭菌(120~125 ℃、0.15~0.20 MPa、4 h)。在超净工作台中接种,每个菌包(灭菌后)接种1 cm×1 cm×1 cm的平菇块,在(25±2) ℃下避光培养。当菌包内长满菌丝体时即停止发菌(第42天)。分别取对照组和平菇组的秸秆,65 ℃烘干并粉碎过筛,作为体外模拟瘤胃发酵底物。
1.1.2 体外模拟瘤胃发酵设备试验采用全自动体外模拟瘤胃发酵设备,包括恒温培养箱、发酵瓶、三通电磁阀、压力传感器、计算机和气相色谱仪(安捷伦7890A,美国)。仪器的参数设定及使用操作参照Wang等[13]提供的方法。恒温培养箱中的发酵瓶通过导管与三通电磁阀和压力传感器连接。压力传感器与计算机连接,每分钟测定并记录发酵瓶中的压力,根据压力与气体体积间的关系计算气体生成量。三通电磁阀受计算机控制,当发酵瓶中压力到达设定排气压力(9 kPa)时[14],电磁阀打开,发酵瓶中的气体通过导管进入气相色谱仪,触发气相色谱仪工作,测定气体中的甲烷和氢气含量。甲烷和氢气产量根据发酵瓶顶部空间大小、压力与气体体积间转化系数、甲烷和氢气含量进行计算[15]。
1.1.3 人工瘤胃培养液选择3只体况良好、体重相近且安装有永久性瘤胃瘘管的去势成年湘东黑山羊作为瘤胃液供体羊。饲粮配制参照NRC(2012)标准,精粗比为40 : 60。精饲料组成:玉米47.00%、豆粕24.00%、麦麸22.00%、食盐0.77%、石粉2.23%、预混料4.00%。每千克预混料含800 mg铜、1 530 mg铁、5 000 mg锌、3 000 mg锰、460 mg硒、3 060 mg碘、740 mg钴、840 000 IU维生素A、168 000 IU维生素D、3 360 IU维生素E,其他为载体。粗饲料为水稻秸秆。试验期内每头瘘管羊每天饲喂精饲料200 g、粗饲料300 g,每天饲喂2次(08:30和18:00),单笼饲养,自由饮水。
人工瘤胃缓冲液:参照Menke等[16]提供的方法配制2 400 mL的人工瘤胃缓冲液。用恒温磁力搅拌器加热人工瘤胃缓冲液,温度为39.5 ℃,通入纯二氧化碳(CO2)保持溶液厌氧环境(刃天青变成无色)。
人工瘤胃培养液:晨饲前1 h,通过瘤胃瘘管采集3只湘东黑山羊的新鲜瘤胃液装入保温瓶中,迅速将瘤胃液用6层脱脂纱布过滤,量取600 mL过滤液迅速加入到准备好的2 400 mL人工瘤胃缓冲液中(瘤胃液与人工瘤胃缓冲液体积比为1 : 4),制成人工瘤胃培养液。
1.2 试验方法 1.2.1 体外模拟瘤胃发酵称取0.6 g底物放入150 mL发酵瓶中,在振荡频率为50 r/min和温度为39.5 ℃的恒温培养箱中预热。取出发酵瓶,通入CO2,以保证发酵瓶中为厌氧环境。用瓶口分液器(Eppendorf)依次向每个发酵瓶中加入60 mL人工瘤胃培养液,并将发酵瓶放入恒温培养箱中进行体外模拟瘤胃发酵,72 h后终止发酵。
1.2.2 样品的采集和测定体外模拟瘤胃发酵72 h后终止发酵,取2 mL发酵液,4 ℃、15 000 r/min条件下离心10 min。取1 mL上清液于2 mL离心管中,加入0.1 mL 25%偏磷酸固定15 min,-20 ℃保存。参照Wang等[17]的方法测定挥发性脂肪酸(volatile fatty acid, VFA)浓度。
将发酵内容物用纱布抽干置于铝盒中,105 ℃烘箱中烘8 h,用于测定干物质降解率(dry matter degradation, DMD)和中性洗涤纤维降解率(neutral detergent fiber disappearance, NDFD),DMD与NDFD的计算参照Zhang等[5]提供的方法。
参照杨胜[18]提供的方法测定干物质(dry matter,DM)、粗蛋白质(crude protein,CP)和粗灰分(Ash)含量。按照Van Soest等[19]提供的方法,用Fibretherm FT12全自动纤维仪(Gerhardt Analytical Systems, 德国)测定中性洗涤纤维(neutral detergent fiber, NDF)、酸性洗涤纤维(acid detergent fiber, ADF)和酸性洗涤木质素(acid detergent lignin, ADL)含量。参照Zhang等[5]提供的方法计算中性洗涤可溶物(neutral detergent soluble, NDS)含量。参照Tuyen等[20]提供的方法计算半纤维素(hemicellucose)和纤维素(cellulose)含量。
1.3 数据分析 1.3.1 产气曲线拟合应用非线性回归程序,按照Wang等[21]的模型对体外瘤胃发酵产气曲线进行拟合,模型及相关参数的计算公式如下:
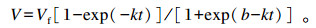
|
式中:V为t时间点底物的累积产气量(gas production, mL/g);Vf为理论最大产气量(finalasymptotic gas production, mL/g);k为产气速率(fractional rate of gas production,h-1);b为曲线的形状指标(shape parameter)。
起始底物降解速率(fractional rate of degradation, FRD0, h-1),即t=0时的底物降解速率,计算公式参考Wang等[22]的模型,数学表达方程为:
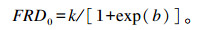
|
本试验数据分析使用SPSS 21.0软件。首先,采用双因素方差分析,分析模型中秸秆类型和平菇处理2个因子。分析结果显示,秸秆类型与平菇处理间存在强交互作用,这说明平菇处理对稻草和小麦秸秆的响应结果不一样。在此基础上,采用单因素方差分析分别分析平菇处理对小麦和水稻秸秆的显著情况。P < 0.05表示差异显著。
2 结果 2.1 平菇处理对发酵底物常规营养成分含量的影响由表 1可知,平菇处理小麦秸秆显著提高NDS含量(+31.1%)(P < 0.05),显著降低NDF(-12.5%)和ADL(-52.1%)含量(P < 0.05)。平菇处理水稻秸秆显著提高NDS(+68.8%)、ADL(+39.1%)和CP(+7.3%)含量(P < 0.05),显著降低NDF(-22.6%)和半纤维素(-57.1%)含量(P < 0.05)。
|
|
表 1 平菇处理对小麦和水稻秸秆营养成分的影响(干物质基础) Table 1 Effects of P. ostreatus treatment on nutrient composition of wheat and rice straw (DM basis) |
平菇处理小麦和水稻秸秆影响体外模拟瘤胃发酵72 h产气曲线(图 1)。由表 2可知,平菇处理小麦秸秆显著提高72 h总产气量(+23.0%)和潜在最大产气量(+15.5%)(P < 0.05)。平菇处理水稻秸秆显著降低72 h总产气量(-6.7%)(P < 0.05)。
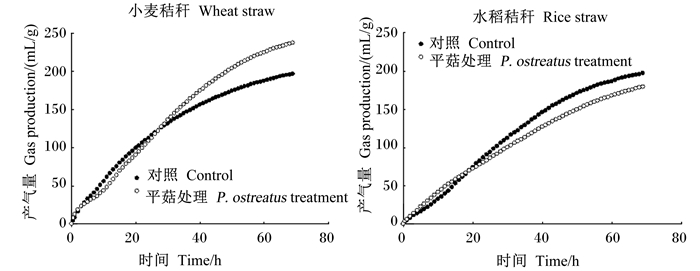
|
图 1 平菇处理小麦和水稻秸秆对体外模拟瘤胃发酵72 h产气曲线的影响(干物质基础) Fig. 1 Effects of P. ostreatus treatment of wheat straw and rice straw on gas production curves of in vitro rumen fermentation for 72 h (DM basis) |
|
|
表 2 平菇处理小麦和水稻秸秆对体外模拟瘤胃发酵72 h气体生成的影响(干物质基础) Table 2 Effects of P. ostreatus treatment of wheat straw and rice straw on gas production in vitro rumen fermentation for 72 h (DM basis) |
平菇处理影响小麦和水稻秸秆体外模拟瘤胃发酵72 h甲烷生成曲线(图 2)。由表 2可知,平菇处理小麦秸秆显著提高甲烷(+26.1%)和氢气产量(+187.0%)(P < 0.05)。平菇处理水稻秸秆显著降低甲烷含量(-10.1%)和产量(-15.6%)(P < 0.05),显著提高氢气含量(+122.0%)和产量(+69.9%)(P < 0.05)。
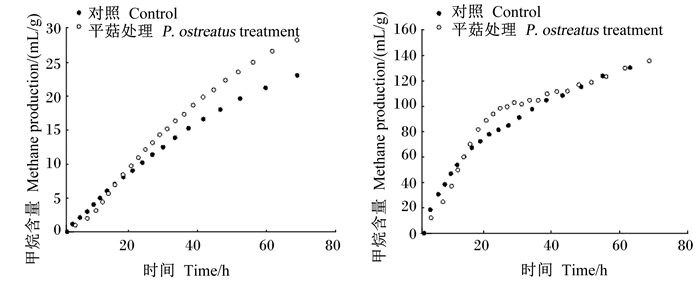
|
图 2 平菇处理小麦和水稻秸秆对体外模拟瘤胃发酵72 h甲烷含量和产量曲线的影响(干物质基础) Fig. 2 Effects of P. ostreatus treatment of wheat straw and rice straw on methane production and content curves of in vitro rumen fermentation for 72 h (DM basis) |
由表 3可知,平菇处理小麦秸秆显著提高DMD(+18.7%)、NDFD(+20.3%)和丙酸比例(+26.9%)(P < 0.05),显著降低乙酸(-8.0%)、丁酸(-10.1%)比例和乙丙比(P < 0.05)。平菇处理水稻秸秆显著降低NDFD(-27.8%)、挥发性脂肪酸浓度(-11.0%)、乙酸比例(-3.9%)和乙丙比(P < 0.05),显著增加丙酸比例(+12.7%)(P < 0.05)。
|
|
表 3 平菇处理小麦和水稻秸秆对体外模拟瘤胃发酵72 h底物降解和挥发性脂肪酸生成的影响 Table 3 Effects of P. ostreatus treatment of wheat straw and rice straw on substrate degradation and VFA production in vitro rumen fermentation for 72 h |
白腐真菌能够分泌纤维降解酶,降解秸秆细胞壁中的纤维素和半纤维素,转变成可溶性碳水化合物[21, 23]。本试验结果显示,平菇处理小麦和水稻秸秆显著降低NDF含量,显著提高NDS含量。这说明平菇处理能够降解小麦和水稻秸秆细胞壁纤维生成小分子碳水化合物。这和Tuyen等[20, 24]的试验结果一致。白腐真菌还能够分泌木质素降解酶分解秸秆细胞壁中的木质素[23]。另外,白腐真菌还会利用秸秆营养物质来维持自身的生长与繁殖[25],可能会影响白腐真菌对秸秆木质素的降解效果。本试验结果显示平菇处理降低小麦秸秆ADL含量,说明平菇对小麦秸秆营养物质的消耗小于对木质素的破坏。但是,平菇处理显著提高水稻秸秆ADL含量,说明平菇对水稻秸秆营养物质的消耗超过对木质素的破坏。水稻秸秆中半纤维素含量偏高,增加了木质素降解酶到达作用部位的难度[24],导致平菇在降解水稻秸秆时消耗的营养物质增多。
平菇处理改变了小麦和水稻秸秆的碳水化合物组成,进而影响瘤胃微生物对纤维的降解。本试验结果发现,平菇处理小麦秸秆显著提高72 h产气量、DMD和NDFD。这说明平菇处理促进瘤胃微生物对小麦秸秆的降解。平菇处理后小麦秸的ADL含量降低,有利于瘤胃微生物降解并生成更多气体[24]。Tuyen等[20]报道平菇处理显著降低小麦秸秆木质素含量,提高瘤胃发酵产气量。然而,平菇处理水稻秸秆降低72 h总产气量和NDFD,说明平菇处理抑制瘤胃微生物对水稻秸秆的降解。平菇处理增加了水稻秸秆中ADL的比重,不利于瘤胃微生物对水稻秸秆利用,导致产气量下降。
Tuyen等[24]报道,虫拟蜡菌处理能够减少棕榈叶的甲烷排放。AKinfemi等[26]发现,平菇处理豇豆和高粱秸秆能够降低甲烷产量和含量。本试验结果表明,平菇处理能够降低水稻秸秆的甲烷产量和甲烷生成效率。这说明平菇处理水稻秸秆能够抑制甲烷生成。Da Silva等[12]和Gezer等[27]曾报道,蘑菇能够抑制革兰氏阳性菌的活性。在本试验中,平菇处理水稻秸秆可能通过抑制瘤胃甲烷菌活性,减少甲烷生成。相反,平菇处理小麦秸秆提高了甲烷产量,这可能是平菇处理小麦秸秆增加瘤胃微生物对底物的降解所致。
氢气是瘤胃甲烷菌生长的重要底物,能够被甲烷菌利用并代谢生成甲烷。当甲烷菌的生长与繁殖受到抑制时,甲烷菌对氢气的利用减少,导致氢气累积[28]。汪悦等[29]发现茶皂素能够改变瘤胃甲烷菌结构,减少某些甲烷菌的数量。本试验结果显示,平菇处理提高小麦秸秆的氢气产量和水稻秸秆的氢气产量及含量。这说明平菇处理水稻秸秆能够抑制甲烷菌活性,不利于甲烷菌利用氢气,限制氢气的消耗使得氢气累积。
平菇处理底物还可能影响体外模拟瘤胃发酵的挥发性脂肪酸生成。Shrivastava等[30]报道,平菇处理可提高小麦秸秆瘤胃发酵的挥发性脂肪酸浓度。本试验中,虽然平菇处理没有提高小麦和水稻秸秆瘤胃发酵的挥发性脂肪酸浓度,但减少了乙丙比。植物细胞壁中的纤维素和半纤维素被瘤胃中的纤维分解菌降解主要生成乙酸,而可溶性碳水化合物被瘤胃淀粉降解菌利用主要生成丙酸[31-32]。平菇处理增加小麦和水稻秸秆的NDS含量,这有助于瘤胃丙酸生成[33]。平菇处理小麦和水稻秸秆造成氢气产量增加,氢气累积改变挥发性脂肪酸的组成,有助于瘤胃丙酸的生成。
4 结论① 平菇处理小麦秸秆可降低ADL含量和增加NDS含量,促进小麦秸秆的瘤胃纤维降解和丙酸生成。
② 平菇处理水稻秸秆会提高ADL含量,抑制水稻秸秆的瘤胃纤维降解、挥发性脂肪酸和甲烷生成,造成氢气累积,有助于丙酸生成。
| [1] |
中华人民共和国国家统计局. 中国统计年鉴2017[M]. 北京: 中国统计出版社, 2017.
|
| [2] |
冯仰廉. 反刍动物营养学[M]. 北京: 科学出版社, 2004: 314.
|
| [3] |
ZENG Y N, ZHAO S, YANG S H, et al. Lignin plays a negative role in the biochemical process for producing lignocellulosic biofuels[J]. Current Opinion in Biotechnology, 2014, 27: 38-45. DOI:10.1016/j.copbio.2013.09.008 |
| [4] |
RAFFRENATO E, FIEVISOHN R, COTANCH K W, et al. Effect of lignin linkages with other plant cell wall components on in vitro and in vivo neutral detergent fiber digestibility and rate of digestion of grass forages[J]. Journal of Dairy Science, 2017, 100(10): 8119-8131. DOI:10.3168/jds.2016-12364 |
| [5] |
ZHANG X M, WANG M, WANG R, et al. Urea plus nitrate pretreatment of rice and wheat straws enhances degradation and reduces methane production in in vitro ruminal culture[J]. Journal of the Science of Food and Agriculture, 2018. DOI:10.1002/jsfa.9056 |
| [6] |
JOHNSON K A, JOHNSON D E. Methane emissions from cattle[J]. Journal of Animal Science, 1995, 73(8): 2483-2492. DOI:10.2527/1995.7382483x |
| [7] |
VISSCHER A D, CLEEMPUT O V. Simulation model for gas diffusion and methane oxidation in landfill cover soils[J]. Waste Management, 2003, 23(7): 581-591. DOI:10.1016/S0956-053X(03)00096-5 |
| [8] |
VAN KUIJK S J A, SONNENBERG A S M, BAARS J J P, et al. Fungal treated lignocellulosic biomass as ruminant feed ingredient:a review[J]. Biotechnology Advances, 2015, 33(1): 191-202. |
| [9] |
VAN KUIJK S J A, DEL RÍO J C, RENCORET J, et al. Selective ligninolysis of wheat straw and wood chips by the white-rot fungus Lentinula edodes and its influence on in vitro rumen degradability[J]. Journal of Animal Science and Biotechnology, 2016, 7: 55. DOI:10.1186/s40104-016-0110-z |
| [10] |
VAN KUIJK S J A, SONNENBERG A S M, BAARS J J P, et al. Fungal treatment of lignocellulosic biomass:importance of fungal species, colonization and time on chemical composition and in vitro rumen degradability[J]. Animal Feed Science and Technology, 2015, 209: 40-50. DOI:10.1016/j.anifeedsci.2015.07.026 |
| [11] |
YANG X W, ZENG Y L, MA F Y, et al. Effect of biopretreatment on thermogravimetric and chemical characteristics of corn stover by different white-rot fungi[J]. Bioresource Technology, 2010, 101(14): 5475-5479. DOI:10.1016/j.biortech.2010.01.129 |
| [12] |
DA SILVA R F, DE ALMEIDA BARROS A C, PLETSCH M, et al. Study on the scavenging and anti-Staphylococcus aureus activities of the extracts, fractions and subfractions of two Volvariella volvacea strains[J]. World Journal of Microbiology and Biotechnology, 2010, 26(10): 1761-1767. DOI:10.1007/s11274-010-0355-1 |
| [13] |
WANG M, WANG R, TANG S X, et al. Comparisons of manual and automated incubation systems:effects of venting procedures on in vitro ruminal fermentation[J]. Livestock Science, 2016, 184: 41-45. DOI:10.1016/j.livsci.2015.12.002 |
| [14] |
龙栋磊, 文江南, 王敏, 等. 全自动体外模拟瘤胃发酵系统:19 kPa以下排气压力不影响发酵特征[J]. 动物营养学报, 2017, 29(11): 4171-4179. DOI:10.3969/j.issn.1006-267x.2017.11.041 |
| [15] |
WANG M, JANSSEN P H, SUN X Z, et al. A mathematical model to describe in vitro kinetics of H2 gas accumulation[J]. Animal Feed Science and Technology, 2013, 184(1/2/3/4): 1-16. |
| [16] |
MENKE K H, RAAB L, SALEWISK A, et al. The estimation of the digestibility and metabolizable energy content of ruminant feeding stuffs from the gas production when they are incubated with rumen liquor in vitro[J]. The Journal of Agricultural Science, 1979, 93(1): 217-222. DOI:10.1017/S0021859600086305 |
| [17] |
WANG M, SUN X Z, JANSSEN P H, et al. Responses of methane production and fermentation pathways to the increased dissolved hydrogen concentration generated by eight substrates in in vitro ruminal cultures[J]. Animal Feed Science and Technology, 2014, 194: 1-11. DOI:10.1016/j.anifeedsci.2014.04.012 |
| [18] |
杨胜. 饲料分析及饲料质量检测技术[M]. 北京: 北京农业大学出版社, 1993: 58-64.
|
| [19] |
VAN SOEST P J, ROBERTSON J B, LEWIS B A. Methods for dietary fiber, neutral detergent fiber, and nonstarch polysaccharides in relation to animal nutrition[J]. Journal of Dairy Science, 1991, 74(10): 3583-3597. DOI:10.3168/jds.S0022-0302(91)78551-2 |
| [20] |
TUYEN V D, CONE J W, BAARS J J P, et al. Fungal strain and incubation period affect chemical composition and nutrient availability of wheat straw for rumen fermentation[J]. Bioresource Technology, 2012, 111: 336-342. DOI:10.1016/j.biortech.2012.02.001 |
| [21] |
WANG M, TANG S X, TAN Z L. Modeling in vitro gas production kinetics:derivation of Logistic-Exponential(LE) equations and comparison of models[J]. Animal Feed Science and Technology, 2011, 165(3/4): 137-150. |
| [22] |
WANG M, SUN X Z, TANG S X, et al. Deriving fractional rate of degradation of Logistic-Exponential (LE) model to evaluate early in vitro fermentation[J]. Animal, 2013, 7(6): 920-929. |
| [23] |
WAN C X, LI Y B. Microbial delignification of corn stover by Ceriporiopsis subvermispora for improving cellulose digestibility[J]. Enzyme and Microbial Technology, 2010, 47(1/2): 31-36. |
| [24] |
TUYEN D V, PHUONG H N, CONE J W, et al. Effect of fungal treatments of fibrous agricultural by-products on chemical composition and in vitro rumen fermentation and methane production[J]. Bioresource Technology, 2013, 129: 256-263. |
| [25] |
ZHAO X L, LUO K, ZHANG Y, et al. Improving the methane yield of maize straw:focus on the effects of pretreatment with fungi and their secreted enzymes combined with sodium hydroxide[J]. Bioresource Technology, 2017, 250: 204-213. |
| [26] |
AKINFEMI A, ADU O A, DOHERTY F. Conversion of sorghum stover into animal feed with white-rot fungi:Pleurotus ostreatus and Pleurotus pulmonarius[J]. African Journal of Biotechnology, 2010, 9(11): 1706-1712. DOI:10.5897/AJB |
| [27] |
GEZER K, DURU M E, KIVRAK I, et al. Free-radical scavenging capacity and antimicrobial activity of wild edible mushroom from Turkey[J]. African Journal of Biotechnology, 2006, 5(20): 1924-1928. |
| [28] |
GARCÍA-GONZÁLEZ R, LOPÉZL S, FERNÁNDEZ M, et al. Dose-response effects of Rheum officinale root and Frangula alnus bark on ruminal methane production in vitro[J]. Animal Feed Science and Technology, 2008, 145(1/2/3/4): 319-334. |
| [29] |
汪悦, 张议夫, 蒋林树. 茶皂素对奶牛瘤胃甲烷菌及甲烷排放的影响[J]. 中国农学通报, 2018, 34(29): 104-111. |
| [30] |
SHRIVASTAVA B, THAKUR S, KHASA Y P, et al. White-rot fungal conversion of wheat straw to energy rich cattle feed[J]. Biodegradation, 2011, 22(4): 823-831. DOI:10.1007/s10532-010-9408-2 |
| [31] |
DEMEYER D I. Rumen microbes and digestion of plant cell walls[J]. Agriculture and Environment, 1981, 6(2/3): 295-337. |
| [32] |
NOCEK J E, TAMMINGA S. Site of digestion of starch in the gastrointestinal tract of dairy cows and its effect on milk yield and composition[J]. Journal of Dairy Science, 1991, 74(10): 3598-629. DOI:10.3168/jds.S0022-0302(91)78552-4 |
| [33] |
DEPETERS E J, GETACHEW G, FADEL J G, et al. In vitro gas production as a method to compare fermentation characteristics of steam-flaked corn[J]. Animal Feed Science and Technology, 2003, 105(1/2/3/4): 109-122. |




