2. 南京皮格曼农牧有限公司, 南京 211300
2. Nanjing Pigman Agriculture and Animal Husbandry Co., Ltd., Nanjing 211300, China
在当今畜牧业生产中抗生素的使用已经受到严格限制甚至禁用,欧盟于2003年通过1831号法案,从2006年起禁止在欧洲养猪生产中使用抗生素作为促生长剂[1]。因此,寻求无公害的抗生素替代品,发展绿色畜牧业、生产绿色畜产品成为了国内外营养领域研究的热点问题之一。益生菌可通过产生有机酸、过氧化氢或抗菌物质、竞争营养素或结合位点,发挥抗毒素作用,刺激免疫系统。屎肠球菌作为一种非致病性的乳酸菌受到人们的广泛关注,它可通过增加肠道中乳酸菌的数量和有机酸的含量,来减少大肠杆菌等有害菌的定植,改善肠道内环境,提高机体的免疫力。并且,屎肠球菌还能促进消化酶的分泌[2],改善蛋白质、脂肪和能量代谢,提高饲料转化率等[3]。本课题组已通过饲养试验已经证实饲粮中添加屎肠球菌有提高平均日增重、平均日采食量,降低料重比的作用[4]。目前屎肠球菌对断奶仔猪肠道组织形态的研究还较少,且并无关于混合添加屎肠球菌和抗生素应用效果的报道。鉴于此,本试验拟通过在饲粮中添加屎肠球菌SF68,研究其对断奶仔猪腹泻率、肠道发育及组织形态的影响,旨在从肠道组织形态学方面探讨屎肠球菌SF68对减少断奶仔猪腹泻的可能作用机制,同时探究是否可混合使用屎肠球菌和抗生素,为屎肠球菌SF68在饲料行业的进一步应用提供科学依据。
1 材料与方法 1.1 试验材料屎肠球菌SF68(NCMIB10415)由滨海普润生物科技有限公司提供,有效菌数量为1.0×1010 CFU/g。
1.2 试验设计试验在苏州市太仓金诸种猪场进行。选用90头21日龄体重[(6.58±0.07) kg]相近的“杜洛克×长白×大约克”三元杂交断奶仔猪,试验前全部去势,随机分配至5组,每组3个重复,每个重复6头猪(公母各占1/2),各组初始体重无显著差异(P>0.05)。对照组(CON组)仔猪饲喂基础饲粮,抗生素组(ANT组)仔猪饲喂基础饲粮+0.02%硫酸抗敌素+0.007 5%金霉素,抗生素+低剂量屎肠球菌组(ALEF组)仔猪饲喂基础饲粮+0.01%屎肠球菌SF68+0.02%的硫酸抗敌素+0.007 5%的金霉素,低剂量屎肠球菌组(LEF组)仔猪饲喂基础饲粮+0.01%屎肠球菌SF68,高剂量屎肠球菌组(HEF组)仔猪饲喂基础饲粮+0.05%屎肠球菌SF68,试验期21 d。抗生素和屎肠球菌SF68通过逐级混匀添加到基础饲粮中。试验期21 d。
1.3 基础饲粮与饲养管理基础饲粮为参照NRC(2012)营养需要配制的粉状配合饲料,其组成及营养水平见表 1。试验期间猪自由采食、饮水,防疫消毒程序按猪场管理规定执行。
|
|
表 1 基础饲粮组成及营养水平(风干基础) Table 1 Composition and nutrient levels of the basal diet (air-dry basis) |
每天14:00逐只观察仔猪腹泻情况,按照表 2的标准对粪便情况进行打分,以评分≥2为开始出现腹泻症状,同时结合精神状态、圈内粪便情况、肛门情况(肛门处有无粪便污染或红肿)判断,记录腹泻仔猪头数和持续时间,按照如下公式计算腹泻率:

|
|
|
表 2 粪便评分标准 Table 2 Scoring standard of faeces |
试验结束后试验猪空腹12 h,然后从每组的每个重复中随机选择2头(共30头)仔猪称重后屠宰,分离肠道,除去肠系膜,分离十二指肠、空肠、回肠,测量各肠段长度并称重。

|
仔猪屠宰后,采集肠道,迅速剪取小肠中段1 cm的肠段,磷酸盐缓冲液(PBS)小心冲洗后,用手术剪剪开肠段,然后用2.5%戊二醛固定液固定保存。分别从十二指肠、空肠和回肠中段剪取1 cm的肠段,PBS小心冲洗后,用4%多聚甲醛固定液固定保存。
将用4%多聚甲醛固定液固定的仔猪十二指肠、空肠和回肠肠段取出,经过修整、脱水、透明、透蜡后进行石蜡包埋,蜡块制作完成后切片(厚度5 μm),再经过苏木精-伊红(HE)染色,中性树脂封片后制成永久切片。使用Image-Pro Plus 6.0显微镜图像处理软件测量其绒毛高度(VH)及与之相连的隐窝深度(CD),并计算绒毛高度与隐窝深度的比值(VH/CD),每个切片测定10个数据,取平均值[5]。
将用2.5%戊二醛固定液固定的小肠中段肠段取出,先切除样品2端1 mm左右片段,以消除边缘效应,然后截取2个1 mm的片段,放入2.5%的戊二醛溶液前固定4 h,用0.1 mol/L PBS冲洗3次,1%的锇酸固定2 h(直至样品变黑为止),用0.1 mol/L PBS冲洗3次,不同梯度(30%、50%、70%、80%、90%、95%和100%)的乙醇脱水,每次15 min,100%丙酮置换,环氧812树脂浸透与包埋,最后放入37 ℃的烘箱中聚合24 h,再在60 ℃聚合48 h。将包埋好的树脂块修好后,用钻石刀在Leica EM UC6超薄切片机下切成厚100 nm的薄片,用200目的铜网捞片后,用2%醋酸双氧铀和1%柠檬酸铅双重染色,在Philips CM100透射电镜下观察并拍照。
1.5 数据整理与统计分析试验数据用Excel 2013进行整理,以平均值±标准误(mean±SE)表示。采用SPSS 19.0软件的单因素方差分析(one way-ANOVA)程序进行方差分析,并使用LSD法进行多重比较,以P < 0.01作为差异极显著标准,以P < 0.05作为差异显著标准,以0.05≤P < 0.10作为有差异显著趋势标准。
2 结果与分析 2.1 屎肠球菌SF68对断奶仔猪腹泻率的影响由表 3可知,与CON组相比,ALEF组仔猪腹泻率显著降低(P<0.05),降幅达到82%;LEF组腹泻率有降低的趋势(P=0.059),降幅达到67%。
|
|
表 3 屎肠球菌SF68对断奶仔猪腹泻率的影响 Table 3 Effects of Enterococcus faecium SF68 on diarrhea rate of weaned piglets |
由表 4可知,与CON组相比,LEF组和HEF组十二指肠相对重显著增加(P < 0.05),同时LEF组回肠相对重也显著增加(P < 0.05)。各组各肠段单位长度重无显著差异(P>0.05)。
|
|
表 4 屎肠球菌SF68对断奶仔猪肠道相对重和单位长度重的影响 Table 4 Effects of Enterococcus faecium SF68 on intestinal relative weight and weight per unit length of weaned piglets |
由表 5可知,与CON组相比,LEF组十二指肠绒毛高度显著增加(P < 0.05);与ANT组相比,LEF组十二指肠绒毛高度极显著增加(P < 0.01)。与ANT组相比,LEF组十二指肠隐窝深度极显著增加(P < 0.01)。与CON组相比,ALEF组绒毛高度与隐窝深度的比值显著增加(P < 0.05)。
|
|
表 5 屎肠球菌SF68对断奶仔猪十二指肠组织形态的影响 Table 5 Effects of Enterrococcus feacium SF68 on duodenum morphology of weaned piglets |
由表 6可知,与CON组相比,ALEF组和HEF组空肠绒毛高度显著增加(P < 0.05);且相比于CON组,LEF组空肠绒毛高度有增加的趋势(P=0.086)。与CON组和ANT组相比,ALEF组和HEF组空肠绒毛高度与隐窝深度的比值显著增加(P < 0.05);与CON相比组,LEF组空肠绒毛高度与隐窝深度的比值有增加的趋势(P=0.087)。各组空肠隐窝深度无显著差异(P>0.05)。
|
|
表 6 屎肠球菌SF68对断奶仔猪空肠组织形态学的影响 Table 6 Effects of Enterrococcus feacium SF68 on jejunum morphology of weaned piglets |
由表 7可知,与CON组相比,ANT组回肠绒毛高度显著减少(P < 0.05);与CON组相比,ALEF组回肠隐窝深度有降低的趋势(P=0.086)。与CON组相比,ANT组和HEF组绒毛高度与隐窝深度的比值显著升高(P < 0.05),ALEF组绒毛高度与隐窝深度的比值极显著升高(P < 0.01);与CON组相比,LEF组绒毛高度与隐窝深度的比值有升高的趋势(P=0.056)。
|
|
表 7 屎肠球菌SF68对断奶仔猪回肠组织形态学的影响 Table 7 Effects of Enterrococcus feacium SF68 on ileum morphology of weaned piglets |
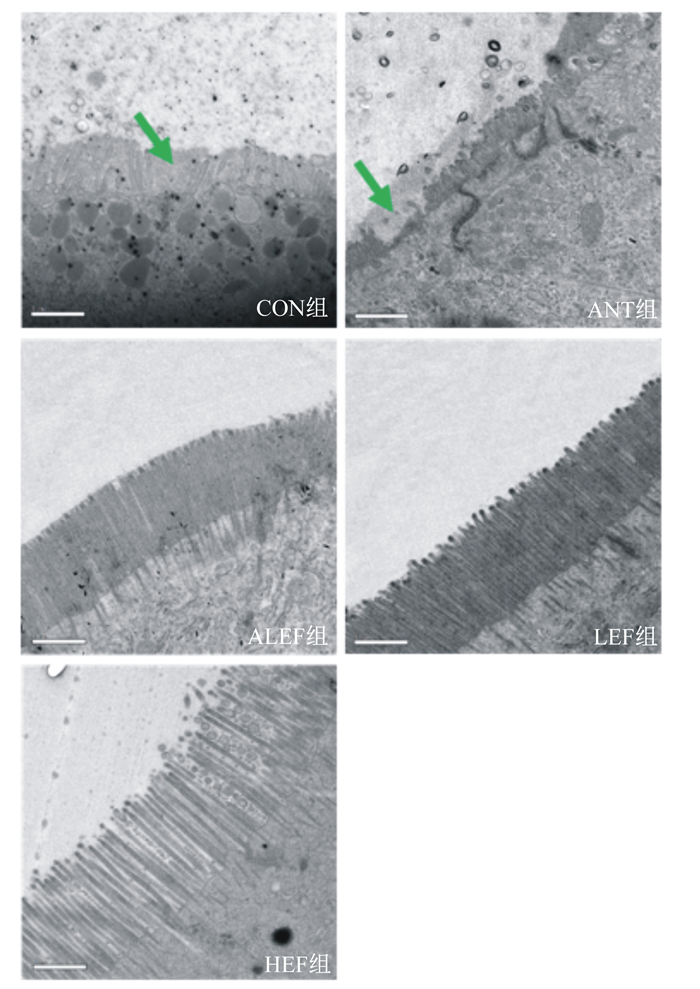
从图 1可以看出,CON组和ANT组小肠微绒毛都出现了不同程度的脱落,而CON组微绒毛脱落较ANT组严重,呈倒伏状。CON组和ANT组纹状缘厚度均明显低于其他各组。相比于ALEF组、LEF组、HEF组,CON组、ANT组微绒毛高度较短。相比于CON组、ANT组、HEF组,ALEF组、LEF组纹状缘更为整齐,微绒毛间隙更为致密。
|
图中箭头所指为小肠微绒毛脱落处。 The microvilli sloughy position indicated by arrows in the figure. 图 1 透射电镜下小肠微绒毛超微结构(放大倍数:3 900×,比例尺:1 μm) Fig. 1 Ultrastructure of small intestine under transmission electron microscope (magnification: 3 900×, scale bar: 1 μm) |
断奶是仔猪生产环节中一个关键的过渡时期。集约化养猪场仔猪的断奶日龄一般控制在3~5周龄,这常常会导致仔猪断奶应激,并引发仔猪腹泻。屎肠球菌在畜禽生产中主要用来调节肠道菌群平衡,以减少腹泻和促进生长[6]。Zeyner等[7]研究发现,口服屎肠球菌SF68能够显著减少哺乳期仔猪的腹泻率。Underdahl[8]的研究也发现,屎链球菌能够显著减少大肠杆菌引起的定菌猪的腹泻率,同时减少仔猪肠道内大肠杆菌数量。Huang等[9]的研究发现,复合乳酸杆菌能够降低仔猪腹泻率和腹泻指数。Mallo等[10]研究发现,屎肠球菌CECT 4515可有效增加断奶仔猪回肠、盲肠中乳酸杆菌的数量,减少大肠杆菌的数量,从而降低腹泻率。本研究也得到相似的结果,即屎肠球菌SF68能够降低断奶仔猪的腹泻率。然而,随着屎肠球菌添加剂量的增加,对应腹泻率随之升高,这可能是由于屎肠球菌添加剂量太大,在一定程度上扰乱了肠道菌群的平衡。研究发现,益生菌可以用来预防抗生素相关性腹泻,而乳酸菌有在这种情况下使用的潜力[11]。混合添加抗生素和屎肠球菌组(ALEF组)相比于CON组能够显著降低断奶仔猪腹泻率,且降低断奶仔猪腹泻率的效果优于单纯添加抗生素组(ANT组),这可能是由于添加屎肠球菌能够减轻抗生素对断奶仔猪带来的不利影响。Giang等[12]的研究表明,饲粮中添加含有屎肠球菌的复合乳酸菌制剂能够显著增加断奶仔猪断奶后1~14 d的平均日增重、平均日采食量,降低料重比。但对断奶后15~35 d的平均日增重、平均日采食量和料重比无显著影响,Broom等[13]也报道称在饲粮中添加屎肠球菌对断奶仔猪的平均日增重、平均日采食量和料重比无显著影响。本课题组的相关研究也发现屎肠球菌对断奶仔猪的促生长作用效果并不显著,可能是由于屎肠球菌对断奶仔猪的这种作用效果主要体现在断奶后前2周,从断奶后第3周开始这种作用效果开始减弱。本研究发现,添加屎肠球菌SF68的2组(LEF组和HEF组)断奶仔猪的肠道相对重和单位长度重均处在较高水平,说明屎肠球菌SF68对断奶仔猪肠道发育有促进作用,从而可能通过增强肠道功能来减少腹泻的发生。
3.2 屎肠球菌SF68对断奶仔猪十二指肠、空肠和回肠组织形态及小肠微绒毛形态的影响小肠黏膜形态结构的完整性是保证动物维持肠道正常生理活动的基础[14]。小肠绒毛的作用主要是增加小肠的吸收面积并起到过滤物质的作用[15]。当仔猪发生腹泻时,机体脱水往往会导致肠绒毛防御性缩短,进而导致绒毛高度降低,小肠吸收面积减少[16]。研究表明,益生菌能够促进动物肠道绒毛的发育。邓军等[17]研究发现,用枯草芽孢杆菌RJGP16和猪源乳酸杆菌B1混合饲喂仔猪后,显著提高了小肠绒毛高度和绒腺比,增加了十二指肠和空肠绒毛数量,促进了肠道绒毛发育,并能拮抗大肠埃希菌K88。肠隐窝又名小肠腺,其深度主要反映肠上皮细胞的成熟率,隐窝变浅表明上皮细胞成熟率增加,分泌功能增强。隐窝深度反应的是小肠上皮细胞的更新生成率,未分化的细胞在隐窝不断生成,并向绒毛的顶端移动并逐渐成熟,以此补充绒毛顶端不断脱落的细胞[18],如果上皮细胞的脱落多于再生,在形态上就会表现为肠黏膜萎缩[8]。绒毛高度与隐窝深度的比值则综合反映小肠的功能状态,绒毛长度变短,隐窝深度变深即绒腺比下降,意味着绒毛吸收细胞减少,分泌细胞增多,肠内膜面积减少,小肠消化吸收功能下降,常伴随腹泻的发生。纹状缘是单层柱状上皮细胞顶部胞质突起形成,由大量微绒毛构成。而微绒毛的高度和密度与吸收细胞代谢活动的强度密切相关;同时,微绒毛的高度和密度也体现了纹状缘的形态结构,平整的纹状缘有利于抵御病原微生物入侵,发挥机体物理屏障功能,提高机体健康水平[19]。
本试验结果表明,饲粮中添加屎肠球菌SF68能够在一定程度上提高断奶仔猪肠道绒毛高度,降低隐窝深度,增加绒毛高度与隐窝深度的比值,而这种作用效果与肠道各段的发育基本对应,说明屎肠球菌SF68在促进肠道发育的同时增强了肠道功能,而肠道功能的增强导致仔猪腹泻率的减少。屎肠球菌SF68可能是通过改善肠道组织形态结构、促进微绒毛的更新来加快上皮细胞成熟,促进肠黏膜形态结构稳定,从而减少断奶仔猪腹泻的发生。同时,本试验还发现在十二指肠和空肠中,屎肠球菌SF68这种对肠道功能的增强作用甚至优于抗生素,并且以混合添加抗生素和屎肠球菌SF68时效果为最佳。Vieira等[20]的研究发现,生长性能与小肠绒毛高度、隐窝深度之间并无显著的相关性,本试验与此结果相似。另外,本试验中ALEF组和LEF组小肠绒毛高度较长,且排列致密,没有出现肠绒毛脱落等情况,此结果与腹泻率结果相对应。在养殖业中,益生菌和抗生素的配伍兼容性一直深受关注,在本试验中,屎肠球菌SF68与硫酸抗敌素和金霉素混合使用,其效果优于单独添加屎肠球菌SF68或抗生素,这可能是因为抗生素和屎肠球菌发生互作,使菌群在肠道定植中达到一种平衡,建立起了更好的微生物屏障来发挥作用。
4 结论① 饲粮中混合添加屎肠球菌SF68和抗生素(硫酸抗敌素、金霉素)能够显著或极显著增加断奶仔猪小肠各段绒毛高度与隐窝深度的比值。
② 饲粮中添加屎肠球菌SF68能够增加断奶仔猪小肠相对重和单位长度重,同时增加微绒毛高度,使纹状缘更为整齐、致密。
③ 综合试验结果得出,屎肠球菌SF68可通过改善肠道发育、增强肠道功能来减少断奶仔猪腹泻,建议断奶仔猪饲粮中屎肠球菌SF68的添加量为0.01%,并且可与硫酸抗敌素和金霉素混合使用。
| [1] |
刘正旭.竹酢粉对断奶仔猪生产性能、免疫机能及肠道微生物区系的影响[D].硕士学位论文.扬州: 扬州大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-11117-1016284407.htm
|
| [2] |
葛龙, 李波. 屎肠球菌在饲用微生态制剂中的研究与应用[J]. 饲料与畜牧, 2013(6): 57-59. |
| [3] |
SAMLI H E, SENKOYLU N, KOC F, et al. Effects of Enterococcus faecium and dried whey on broiler performance, gut histomorphology and intestinal microbiota[J]. Archives of Animal Nutrition, 2007, 61(1): 42-49. DOI:10.1080/17450390601106655 |
| [4] |
冯宝宝, 方伟, 封飞飞, 等. 屎肠球菌SF68对断奶仔猪生长性能、血常规和血清生化指标及抗氧化性能的影响[J]. 动物营养学报, 2018, 30(3): 1125-1135. DOI:10.3969/j.issn.1006-267x.2018.03.038 |
| [5] |
MITCHAOTHAI J, YUANGKLANG C, VASUPEN K, et al. Effect of dietary calcium and lecithin on growth performance and small intestinal morphology of young wild pigs[J]. Livestock Science, 2010, 134(1/2/3): 106-108. |
| [6] |
VONDRUSKOVA H, SLAMOVA R, TRCKOVA M, et al. Alternatives to antibiotic growth promoters in prevention of diarrhoea in weaned piglets:a review[J]. Veterinární Medicína, 2010, 55(5): 199-224. DOI:10.17221/VETMED |
| [7] |
ZEYNER A, BOLDT E. Effects of a probiotic Enterococcus faecium strain supplemented from birth to weaning on diarrhoea patterns and performance of piglets[J]. Journal of Animal Physiology and Animal Nutrition, 2006, 90(1/2): 25-31. |
| [8] |
UNDERDAHL N R. The effect of feeding Streptococcus faecium upon Escherichia coli induced diarrhea in gnotobiotic pigs[J]. Progress in Food & Nutrition Science, 1983, 7(3/4): 5-12. |
| [9] |
HUANG C H, QIAO S Y, LI D F, et al. Effects of Lactobacilli on the performance, diarrhea incidence, VFA concentration and gastrointestinal microbial flora of weaning pigs[J]. Asian-Australasian Journal of Animal Sciences, 2004, 17(3): 401-409. DOI:10.5713/ajas.2004.401 |
| [10] |
MALLO J J, RIOPEREZ J, HONRUBIA P. The addition of Enterococcus faecium to diet improves piglet's intestinal microbiota and performance[J]. Livestock Science, 2010, 133(1/2/3): 176-178. |
| [11] |
D'SOUZA A L, RAJKUMAR C, COOKE J, et al. Probiotics in prevention of antibiotic associated diarrhoea:meta-analysis[J]. Bmj Chinese Edition, 2003, 324(7350): 1361. |
| [12] |
GIANG H H, VIET T Q, OGLE B, et al. Growth performance, digestibility, gut environment and health status in weaned piglets fed a diet supplemented with potentially probiotic complexes of lactic acid bacteria[J]. Livestock Science, 2010, 129(1/2/3): 95-103. |
| [13] |
BROOM L J, MILLER H M, KERR K G, et al. Effects of zinc oxide and Enterococcus faecium SF68 dietary supplementation on the performance, intestinal microbiota and immune status of weaned piglets[J]. Research in Veterinary Science, 2006, 80(1): 45-54. DOI:10.1016/j.rvsc.2005.04.004 |
| [14] |
HOUSHMAND M, AZHAR K, ZULKIFLI I, et al. Effects of non-antibiotic feed additives on performance, immunity and intestinal morphology of broilers fed different levels of protein[J]. South African Journal of Animal Science, 2012, 42(1): 22-32. |
| [15] |
王永超.肠膜蛋白粉和发酵豆粕替代鱼粉对断奶仔猪作用效果的研究[D].硕士学位论文.郑州: 河南科技大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10464-1015902653.htm
|
| [16] |
PLUSKE J R, WILLIAMS I H, AHERNE F X. Maintenance of villous height and crypt depth in piglets by providing continuous nutrition after weaning[J]. Animal Science, 1996, 62(1): 131-144. DOI:10.1017/S1357729800014417 |
| [17] |
邓军, 李云锋, 杨倩. 枯草芽孢杆菌和猪源乳酸杆菌混合饲喂对仔猪肠绒毛发育的影响[J]. 畜牧兽医学报, 2013, 44(02): 295-301. |
| [18] |
YANG H, XIONG X, WANG X, et al. Effects of weaning on intestinal upper villus epithelial cells of piglets[J]. PLoS One, 2016, 11(3): e0150216. DOI:10.1371/journal.pone.0150216 |
| [19] |
SEGAWA S, FUJIYA M, KONISHI H, et al. Probiotic-derived polyphosphate enhances the epithelial barrier function and maintains intestinal homeostasis through integrin-p38 MAPK pathway[J]. PLoS One, 2011, 6(8): e23278. DOI:10.1371/journal.pone.0023278 |
| [20] |
VIEIRA S L, OYARZABAL O A, FREITAS D M, et al. Performance of broilers fed diets supplemented with sanguinarine-like alkaloids and organic acids[J]. The Journal of Applied Poultry Research, 2008, 17(1): 128-133. DOI:10.3382/japr.2007-00054 |




