2. 水产高效健康生产湖南省协同创新中心, 常德 415000
2. Collaborative Innovation Center for Efficient and Health Production of Fisheries in Hunan Province, Changde 415000, China
近年来,水产行业对鱼粉的巨大需求导致寻找鱼粉替代蛋白质源成为当前水产营养与饲料的研究热点。豆粕是水产饲料中最常用的植物蛋白质源,与鱼粉相比,豆粕存在氨基酸不平衡、含有较多抗营养因子以及适口性不佳等缺点,导致其过高比例替代鱼粉后会影响鱼类的蛋白质利用率、摄食量、免疫能力和消化能力等,进而降低鱼类的生长性能[1-4]。本实验室前期研究结果表明,当膨化豆粕替代鱼粉的量超过18.6%后,会显著降低黄鳝的生长性能[5]。
为了提高豆粕替代鱼粉的效果,改善饲料中氨基酸平衡是当前水产饲料研究中常用方法之一,其中最普遍的方法是添加人工合成的氨基酸。在畜禽动物研究中,添加晶体氨基酸对养殖对象生长性能的改善效果明显[6-7],但在水产动物中却存在争议。研究发现,晶体氨基酸可以有效提高不同蛋白质源在卵形鲳鲹(Trachinotus ovatus)[8]和花鲈(Lateolabrax japonicus)[9]中对鱼粉的替代效果,然而在异育银鲫(Carassius auratus gibelio)[10]和草鱼(Ctenopharyngodon idellus)[11]上的效果却有限。其原因可能是晶体氨基酸与饲料中蛋白质态氨基酸的吸收速率无法同步[12]。为了提高水产动物对添加的氨基酸的利用率,微胶囊技术被应用于水产饲料中,在牙鲆(Paralichthys olivaceus)[13]、建鲤(Cyprinus carpio var. Jian)[14]、罗非鱼(Oreochromis niloticus×O. aureus)[15]上的研究发现,添加微囊氨基酸能显著提高大豆产品对鱼粉的替代效果。消除抗营养因子是另一种改善豆粕对鱼粉替代效果的方法。豆粕中抗营养因子主要以胰蛋白酶抑制因子(trypsin inhibitor, TI)、大豆凝集素(soybean agglutinin, SBA)、低聚糖(oligosaccharide, OS)和抗原蛋白为主。大豆浓缩蛋白(soy protein concentrate, SPC)和大豆分离蛋白(soy protein isolate, SPI)是对豆粕进行不同加工处理后得到的大豆蛋白。在加工过程中,大豆分离蛋白有效地消除了皂素等抗营养因子[16-17]。在大黄鱼(Larimichthys crocea)幼鱼[18-19]和石斑鱼(♀ Epinephelus fuscoguttatus× ♂ Epinephelus lanceolatus)[20-21]的研究中发现,大豆浓缩蛋白相比豆粕具有更好的替代鱼粉效果。而消除了大豆凝集素和低聚糖的大豆分离蛋白[22-23],也能有效替代幼建鲤[24]和虹鳟(Oncorhynchus mykiss)[25-26]饲料中的鱼粉。
本试验以黄鳝为研究对象,通过比较膨化豆粕(extruded soybean meal,ESM)、膨化豆粕中添加晶体和微囊赖氨酸(lysine, Lys)与蛋氨酸(methionine, Met)以及去除了大部分抗营养因子的大豆浓缩蛋白和大豆分离蛋白替代部分鱼粉后对黄鳝生长、肠道消化酶活性和血清生化指标等方面的影响,探讨影响黄鳝饲料中植物蛋白质利用的限制因子,为提高大豆蛋白在黄鳝饲料中对鱼粉的替代效果提供理论依据。
1 材料与方法 1.1 试验饲料以含55%鱼粉的黄鳝商品饲料为对照饲料(CON组),然后分别用膨化豆粕(ESM组)、膨化豆粕+晶体赖氨酸与蛋氨酸(ESMC组)、膨化豆粕+微囊赖氨酸与蛋氨酸(ESMM组)、大豆浓缩蛋白(SPC组)和大豆分离蛋白(SPI组)代替对照饲料中48%的鱼粉,共配制6种等氮等能的试验饲料。试验饲料组成及营养水平如表 1所示,试验饲料氨基酸组成如表 2所示。试验饲料所用大豆蛋白质源均由山东万得福公司提供,晶体和微囊赖氨酸与蛋氨酸由杭州康德权公司提供,赖氨酸以赖氨酸盐酸盐形式添加,其中晶体赖氨酸有效含量为78.0%,微囊赖氨酸有效含量为39.0%;晶体蛋氨酸有效含量为99.0%,微囊蛋氨酸有效含量为49.5%。氨基酸添加量以本实验室所做膨化豆粕替代鱼粉试验结果[5]作为参考。饲料原料粉碎后,用80目筛网筛分,按配方要求称量各饲料原料,均匀混合后风干,直至水分含量低于10%。饲料成品保存在-20 ℃冰柜中。投喂时需提前加20%水,将饲料揉成面团后投喂。
|
|
表 1 试验饲料组成及营养水平(风干基础) Table 1 Composition and nutrient levels of experimental diets (air-dry basis) |
|
|
表 2 试验饲料氨基酸组成 Table 2 Amino acid composition of experimental diets |
养殖试验在本团队位于湖南省常德市西湖镇的试验基地开展。挑选规格齐整的野生黄鳝,通过池塘网箱养殖方式进行试验,黄鳝放入网箱后停食2 d。前期驯化投喂蚯蚓和鱼浆混合物(比例为1 : 1),根据黄鳝摄食状况相应地提高投喂量以及鱼浆含量,直至黄鳝摄食全鱼浆。后期驯化投喂饲料与鱼浆混合物(比例为1 : 4),根据摄食情况提高饲料的比例,直至黄鳝完全摄食饲料。经过约20 d驯化后,饥饿24 h,挑选初始体重为(11.95±0.11) g的黄鳝1 800条,随机分成6组,每组3个重复,共18个网箱(1.5 m×2.0 m×1.0 m),每个网箱饲养黄鳝100条。投喂量以黄鳝初始体重的3%~5%为标准,每日投喂1次(17:00—18:00),投喂量每周调整1次,试验期间记录每个网箱采食量。养殖试验持续10周,试验期间水温保持在(27.0±2.5) ℃,溶氧浓度为(5.8±0.8) mg/L,氨氮浓度低于0.7 mg/L。
1.3 样品收集与指标测定 1.3.1 生长性能指标试验开始时和结束后测量所有网箱中黄鳝数量和重量,用以计算黄鳝的成活率(SR)、增重率(WGR)、饲料系数(FCR)、特定生长率(SGR)和蛋白质效率(PER)。
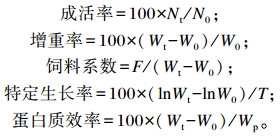
|
式中:Nt为终末条数;N0为初始条数;Wt为末均重(g);W0为初均重(g);F为平均饲料摄入量(g);T为饲喂天数(d);Wp为平均每条摄入蛋白质总量(g)。
试验结束后,从每个网箱中随机选取3条黄鳝,测定体长和体重以及内脏和肝脏重量,用以计算肥满度(CF)、肝体比(HSI)和脏体比(VSI)。
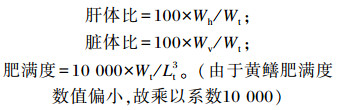
|
式中:Wh为肝脏重(g);Wt为体重(g);Wv为内脏重(g);Lt为体长(cm)。
1.3.2 饲料氨基酸组成分析饲料氨基酸组成参照《食品中氨基酸的测定》(GB/T 5009.124—2003)方法测定并适当修改,具体如下:饲料烘干粉碎后,称量100 mg放进水解管中,同时吸取5 mL盐酸(浓度为6 mol/L),密封管口,于110 ℃温度下水解22 h,完全冷却后过滤,定容至100 mL,取1 mL稀释10倍后上机(氨基酸自动分析仪,A300,德国)分析。
1.3.3 肠道消化酶活性测定养殖试验结束时,从每个网箱中随机选取5条黄鳝,经过MS-222麻醉后,解剖肠道,将肠道内的粪便及附着物清理后,用冰双蒸水洗净,吸去水分并准确称量重量。将肠道剪碎后冰水浴条件下匀浆,4 ℃下3 000 r/min离心15 min,取上清液用以测定胰蛋白酶(trypsin)、淀粉酶(amylase)和脂肪酶(lipase)活性,其中胰蛋白酶活性单位定义为:pH 8.0、37 ℃条件下,每毫克蛋白质中含有的胰蛋白酶每分钟使吸光度变化0.003为1个酶活性单位;淀粉酶活性单位定义为:每毫克蛋白质在37 ℃与底物作用30 min,水解10 mg淀粉定义为1个酶活性单位;脂肪酶活性单位定义为:每毫克蛋白质在37 ℃下,每分钟水解甘油三酯(TG)生成1 μmol脂肪酸定义为1个酶活性单位。上述消化酶在肠道中的活性均按照从南京建成生物工程研究所订购的试剂盒的操作要求进行测定。
1.3.4 血清生化指标的测定养殖试验结束后,将黄鳝停食24 h,从每个网箱中随机选取5条黄鳝,经过MS-222麻醉后,采取尾静脉抽血,血液在4 ℃下静置过夜后,3 500 r/min离心15 min,取上层血清置于-80 ℃冰箱备用。
血清中葡萄糖(GLU)、甘油三酯、总胆固醇(T-CHO)含量及谷草转氨酶(GOT)、谷丙转氨酶(GPT)和溶菌酶(LYZ)活性按照从南京建成生物工程研究所订购的试剂盒的操作要求进行检测。其中GOT和GPT活性单位定义为:1 mL血清,反应液总容量3 mL,在340 nm波长下,使用内径为1 cm的比色皿,在25 ℃下1 min内所生成的丙酮酸,使还原态烟酰胺腺嘌呤二核苷酸(NADH)氧化成氧化态烟酰胺腺嘌呤二核苷酸(NAD+)而引起吸光度每下降0.001为1个卡门氏单位(1卡门氏单位=0.482 U/L);溶菌酶活性单位定义为:25 ℃、pH 6.0、450 nm波长条件下,每分钟引起溶酶小球菌体溶液吸光度下降0.001所需酶量为1个酶活性单位(1 μg/mL=80 U/mL)。血清中补体3(C3)、补体4(C4)含量按照从浙江伊利康生物技术有限公司订购的试剂盒的操作要求进行检测。
1.4 数据统计与分析数据用“平均值±标准误”表示,使用SPSS 19.0统计软件进行单因素方差分析(one-way ANOVA),如果组间差异显著(P < 0.05),则作Duncan氏多重比较分析。
2 结果 2.1 3种大豆产品替代鱼粉对黄鳝生长性能的影响由表 3可知,各组间黄鳝的SR和VSI没有显著差异(P>0.05)。膨化豆粕替代48%鱼粉后增重率、特定生长率和蛋白质效率均显著下降(P < 0.05)。相比ESM组,膨化豆粕中添加微囊或晶体赖氨酸与蛋氨酸均能使增重率、特定生长率和蛋白质效率升高,且微囊组效果比晶体组要好,但3组之间差异不显著(P>0.05);膨化豆粕中添加微囊或晶体赖氨酸与蛋氨酸还能使饲料系数降低,其中ESMM组与ESM组的差异达到显著水平(P < 0.05)。相比ESM组,SPC和SPI组的增重率、特定生长率和蛋白质效率显著升高,饲料系数显著降低(P < 0.05),且SPI组上述指标与CON组无显著差异(P>0.05)。ESM组的肝体比和肥满度显著低于CON组(P < 0.05);与ESM组相比,SPC组的肝体比和肥满度以及SPI组的肥满度有升高的趋势,但差异没有达到显著水平(P>0.05)。
|
|
表 3 3种大豆产品替代鱼粉对黄鳝生长性能的影响 Table 3 Effects of fish meal replacement by three kinds of soybean products on growth performance of ricefield eel |
由表 4可知,不同大豆产品以及添加晶体或微囊氨基酸后替代48%的鱼粉均未对黄鳝的肠道淀粉酶活性产生显著影响(P>0.05)。膨化豆粕替代48%的鱼粉后显著降低了黄鳝肠道脂肪酶活性(P < 0.05);相比膨化豆粕,膨化豆粕中添加微囊赖氨酸与蛋氨酸,以及大豆浓缩蛋白和大豆分离蛋白都会显著升高黄鳝肠道脂肪酶活性(P < 0.05)SPI组黄鳝肠道胰蛋白酶活性显著低于ESM、ESMC、ESME和SPI组(P < 0.05),而与CON组没有显著差异(P>0.05)。
|
|
表 4 3种大豆产品替代鱼粉对黄鳝肠道消化酶活性的影响 Table 4 Effects of fish meal replacement by three kinds of soybean products on intestinal digestive enzymes activities of ricefield eel |
由表 5可知,不同大豆产品以及添加晶体或微囊氨基酸后替代48%的鱼粉均未对黄鳝的血清葡萄糖含量造成显著影响(P>0.05)。膨化豆粕替代48%的鱼粉后血清谷丙转氨酶活性显著降低(P < 0.05);与膨化豆粕相比,膨化豆粕中添加微囊或晶体赖氨酸与蛋氨酸,以及大豆浓缩蛋白和大豆分离蛋白均使黄鳝血清谷丙转氨酶活性显著升高(P < 0.05)。SPC组血清补体4含量以及SPI组血清补体3、补体4和甘油三酯含量均显著高于ESM组(P < 0.05)。SPC和SPI组血清总胆固醇含量显著低于ESM组(P < 0.05),但各替代组与CON组均没有显著差异(P>0.05)。
|
|
表 5 3种大豆产品替代鱼粉对黄鳝血清生化指标的影响 Table 5 Effects of fish meal replacement by three kinds of soybean products on serum biochemical indexes of ricefiled eel |
本试验结果表明,膨化豆粕替代48%的鱼粉后显著降低了黄鳝的生长性能,与本实验室前期研究结果[5]一致。与膨化豆粕相比,在膨化豆粕中添加晶体或微囊赖氨酸与蛋氨酸后,黄鳝的生长性能得到了一定程度的改善,其中微囊组增重率提高了约18%,而晶体组增重率提高了约15%。对于草鱼[27]、鲤鱼[11]和奥尼罗非鱼的研究也得出类似结果。其主要原因在于,鱼体能够直接利用饲料中补充的晶体氨基酸,而饲料中蛋白质则需要经过消化分解成氨基酸后才能参与鱼体的蛋白质合成,2种形态的氨基酸吸收不同步,使得添加的晶体氨基酸被机体代谢掉而无法有效利用[28];而对氨基酸进行微囊化后,可以有效延缓鱼体对氨基酸的吸收速率,对同步2种形态氨基酸的吸收速率, 起到促进作用,从而提高氨基酸的利用效果。但在本试验中,相对大豆浓缩蛋白和大豆分离蛋白,在膨化豆粕中添加晶体或微囊赖氨酸与蛋氨酸并不能显著改善黄鳝的生长性能,这表明在膨化豆粕替代48%的鱼粉后,赖氨酸与蛋氨酸不是限制膨化豆粕利用的主要因素。
大豆浓缩蛋白和大豆分离蛋白对黄鳝饲料中鱼粉的替代效果要明显优于膨化豆粕。相比ESM组,SPC和SPI组黄鳝的增重率分别提高了33%和43%。这与大豆浓缩蛋白在大黄鱼[19, 29]和大西洋鲷(Sparus aurata L.)[30-31]以及大豆分离蛋白在幼建鲤[32]上的研究结果一致。不同大豆产品替代鱼粉对黄鳝生长性能造成不同影响的原因可能是:1)膨化豆粕经过的高温高压处理只对大豆蛋白中存在的部分热敏性抗营养因子的去除有效,而对于其他非热敏性抗营养因子的去除效果甚微。大豆浓缩蛋白是豆粕除去水溶性和醇溶性非蛋白部分后的产物,有效地消除了大豆凝集素、皂素等抗营养因子[16-17]。大豆分离蛋白是对低温变性大豆粕进行浸提和沉淀后的蛋白产物,含有极低水平的大豆凝集素和低聚糖[22-23]。通过对上述3种大豆产品中抗营养因子的比较发现,相比豆粕,大豆浓缩蛋白和大豆分离蛋白中大豆球蛋白和β-伴大豆球蛋白含量均出现了显著下降[33]。大豆球蛋白和β-伴大豆球蛋白是大豆蛋白中最主要的抗原蛋白,会引起动物的过敏反应[34-35],同时其还会影响鱼类肠道的消化吸收能力[36]。2)黄鳝作为依靠嗅觉觅食的动物,饲料气味对其摄食有重要的影响,大豆浓缩蛋白和大豆分离蛋白相比膨化豆粕能够有效消除饲料中的豆腥味,进而提高黄鳝的摄食量。在养殖期间,我们观察发现SPC和SPI组黄鳝相对ESM组摄食时间更短。另外,杨代勤等[37]的研究结果显示,饲料中添加甘氨酸和丙氨酸这类呈味氨基酸能够有效提高黄鳝的摄食量。而本试验关于饲料氨基酸组成的检测发现,大豆浓缩蛋白和大豆分离蛋白饲料中甘氨酸和丙氨酸含量较膨化豆粕饲料均有不同程度的升高。另外,饲料氨基酸组成检测结果还发现,相对于膨化豆粕饲料,大豆浓缩蛋白和大豆分离蛋白饲料中赖氨酸和蛋氨酸含量没有出现显著升高的现象,这也从侧面证明,赖氨酸和蛋氨酸不是制约膨化豆粕在黄鳝饲料中替代鱼粉的主要因素。
3.2 3种大豆产品替代鱼粉对黄鳝肠道消化酶活性的影响本试验中,黄鳝肠道脂肪酶和胰蛋白酶活性较高,而淀粉酶活性偏低,这符合黄鳝的摄食习性,即以肉食性为主。相比ESM组,SPC组黄鳝的肠道胰蛋白酶活性出现显著降低。这可能与不同大豆产品中胰蛋白酶抑制因子含量有关。胰蛋白酶抑制因子是大豆蛋白对胰蛋白酶活性造成影响的最主要抗营养因子,Alarcón等[38]以及Sveier等[39]在大西洋鲑鱼(Salmo salar L.)的研究中显示,胰蛋白酶抑制因子主要通过影响肝胰脏的发育或者与肠道中的蛋白酶结合而降低肠道中蛋白酶的活性。但在虹鳟的研究中同时发现,胰蛋白酶抑制因子会激活机体的反馈机制,即通过增加胰蛋白酶的分泌缓解胰蛋白酶抑制因子的影响[40]。本试验中,与ESM组相比,SPI组黄鳝的肠道胰蛋白酶活性出现了显著的降低,但与CON组相比没有显著差异,这可能是由于大豆分离蛋白中胰蛋白酶抑制因子含量相比膨化豆粕要少很多,不会影响黄鳝肝胰脏的发育,黄鳝不需要通过提高胰蛋白酶的分泌来缓解大豆蛋白中胰蛋白酶抑制因子的影响。通过生长性能相关数据发现,SPI组黄鳝的生长性能与CON组没有显著差异,这也从侧面表明SPI组中胰蛋白酶活性较低没有对黄鳝的正常生理功能造成不良影响。ESM组黄鳝肠道脂肪酶活性较CON组显著降低,相比膨化豆粕,大豆浓缩蛋白和大豆分离蛋白替代48%的鱼粉后能显著提高肠道脂肪酶活性,这可能与这2种大豆蛋白中的大豆寡糖含量较膨化豆粕低有关。同时,在本试验发现,黄鳝肠道脂肪酶活性的变化趋势与黄鳝生长性能的变化趋势具有很大的相似性。
3.3 3种大豆产品替代鱼粉对黄鳝血清生化指标的影响血清中溶菌酶活性和补体含量能反映鱼类的非特异性免疫状态。本试验中,与CON组相比,ESM组血清溶菌酶活性有所降低,但没有显著差异,而SPC组则显著下降。这与段培昌等[41]和刘勇等[42]的研究结果相吻合。作为一类具有酶活性的蛋白质,补体主要存在于体液中,补体3是其中的关键因子,其参与了经典途径、旁路途径和凝集素途径这3条激活途径[43]。相比补体3,补体4主要参与经典途径和凝集素途径[44]。在本试验中,大豆浓缩蛋白和大豆分离蛋白替代48%的鱼粉后,黄鳝血清中补体4含量相比CON组均出现升高的趋势;同时,大豆分离蛋白还会显著升高黄鳝血清中补体3的含量。上述结果表明大豆分离蛋白能够提高黄鳝的免疫力。血清中谷草转氨酶和谷丙转氨酶活性能够有效反映肝脏的受损状态。在本试验中,各替代组黄鳝血清中谷草转氨酶没有出现升高,这说明试验所用的膨化豆粕、大豆浓缩蛋白和大豆分离蛋白对黄鳝的肝脏不会造成严重的损伤。有关大黄鱼[45]和暗纹东方鲀(Takifugu fasciatus)[46]研究结果也印证了这一点。另外,血清中谷草转氨酶和谷丙转氨酶活性也能够反映机体氨基酸代谢的强度[47]。ESM组黄鳝血清中谷丙转氨酶活性显著低于CON组,可能与膨化豆粕替代鱼粉后降低了氨基酸代谢强度,减少蛋白质的沉积有关。相对膨化豆粕,在膨化豆粕中添加晶体或微囊赖氨酸与蛋氨酸,以及大豆浓缩蛋白和大豆分离蛋白均显著升高了黄鳝血清中谷草转氨酶活性,这表示黄鳝的氨基酸代谢强度得到了提高,本试验中黄鳝的生长性能结果也印证了这一效应。
4 结论在本试验条件下,大豆浓缩蛋白和大豆分离蛋白相比膨化豆粕具有更好的替代鱼粉效果,而且在膨化豆粕中添加不同形式的赖氨酸与蛋氨酸并不能进一步提高膨化豆粕对鱼粉的替代效果。由此可知,限制大豆蛋白在黄鳝饲料中替代鱼粉的首要因素是其中的部分抗营养因子以及大豆蛋白对饲料适口性的影响,而不是赖氨酸与蛋氨酸的缺乏。
| [1] |
CHOU R L, HER B Y, SU M S, et al. Substituting fish meal with soybean meal in diets of juvenile cobia Rachycentron canadum[J]. Aquaculture, 2004, 229(1/2/3/4): 325-333. |
| [2] |
YAGHOUBI M, MOZANZADEH M T, MARAMMAZI J G, et al. Dietary replacement of fish meal by soy products (soybean meal and isolated soy protein) in silvery-black porgy juveniles (Sparidentex hasta)[J]. Aquaculture, 2016, 464: 50-59. DOI:10.1016/j.aquaculture.2016.06.002 |
| [3] |
KOKOU F, SARROPOULOU E, COTOU E, et al. Effects of fish meal replacement by a soybean protein on growth, histology, selected immune and oxidative status markers of gilthead sea bream, Sparus aurata[J]. Journal of the World Aquaculture Society, 2015, 46(2): 115-128. DOI:10.1111/jwas.2015.46.issue-2 |
| [4] |
吕云云, 常青, 陈四清, 等. 发酵豆粕对圆斑星鲽生长及消化能力的影响[J]. 水生生物学报, 2016, 40(1): 10-18. |
| [5] |
张俊智, 吕富, 郇志利, 等. 膨化豆粕替代不同比例鱼粉对黄鳝生长性能、体成分、肠道消化酶活力及血清生化指标的影响[J]. 动物营养学报, 2015, 27(11): 3567-3576. DOI:10.3969/j.issn.1006-267x.2015.11.030 |
| [6] |
宋巧燕, 夏先林, 熊光源, 等. 日粮中添加氨基酸对黔东南小香鸡生长和屠宰性能的影响[J]. 贵州农业科学, 2011, 39(8): 143-145. DOI:10.3969/j.issn.1001-3601.2011.08.041 |
| [7] |
董志岩, 刘景, 叶鼎承, 等. 不同低蛋白日粮添加氨基酸对生长猪生长性能及血液生化指标的影响[J]. 福建农业学报, 2009, 24(4): 341-344. DOI:10.3969/j.issn.1008-0384.2009.04.013 |
| [8] |
NIU J, FIGUEIREDO-SILVA C, DONG Y, et al. Effect of replacing fish meal with soybean meal and of DL-methionine or lysine supplementation in pelleted diets on growth and nutrient utilization of juvenile golden pompano (Trachinotus ovatus)[J]. Aquaculture Nutrition, 2016, 22(3): 606-614. |
| [9] |
胡亮, 薛敏, 王彬, 等. 晶体氨基酸提高混合动物蛋白替代花鲈饲料中鱼粉的潜力[J]. 水产学报, 2011, 35(2): 268-275. |
| [10] |
冷向军, 王冠, 李小勤, 等. 饲料中添加晶体或包膜氨基酸对异育银鲫生长和血清游离氨基酸水平的影响[J]. 水产学报, 2007, 31(6): 743-748. |
| [11] |
罗运仙, 谢骏, 吕利群, 等. 饲料中补充晶体或微囊赖氨酸对草鱼生长和血浆总游离氨基酸的影响[J]. 水产学报, 2010, 34(3): 466-473. |
| [12] |
冷向军, 李小勤, 陈丙爱, 等. 鱼类对晶体氨基酸利用的研究进展[J]. 水生生物学报, 2009, 33(1): 119-123. |
| [13] |
DENG J M, MAI K S, AI Q H, et al. Effects of replacing fish meal with soy protein concentrate on feed intake and growth of juvenile Japanese flounder, Paralichthys olivaceus[J]. Aquaculture, 2006, 258(1/2/3/4): 503-513. |
| [14] |
单玲玲, 李小勤, 郑小淼, 等. 不同形式蛋氨酸对建鲤生长性能及血清游离氨基酸含量的影响[J]. 水生生物学报, 2015, 39(2): 259-266. |
| [15] |
冷向军, 田娟, 陈丙爱, 等. 罗非鱼对晶体蛋氨酸、包膜蛋氨酸利用的比较研究[J]. 水生生物学报, 2013, 37(2): 235-242. |
| [16] |
李二超, 陈立侨, 彭士明, 等. 大豆浓缩蛋白作为水产饲料蛋白源的评价[J]. 水产养殖, 2005, 26(1): 18-20. DOI:10.3969/j.issn.1004-2091.2005.01.005 |
| [17] |
BUREAU D P, HARRIS A M, CHO C Y. The effects of purified alcohol extracts from soy products on feed intake and growth of chinook salmon (Oncorhynchus tshawytscha) and rainbow trout (Oncorhynchus mykiss)[J]. Aquaculture, 1998, 161(1/2/3/4): 27-43. |
| [18] |
冯建, 王萍, 何娇娇, 等. 大豆浓缩蛋白替代鱼粉对大黄鱼幼鱼生长、体成分、血清生化指标及肝组织学的影响[J]. 中国水产科学, 2017, 24(2): 268-277. |
| [19] |
张帆, 张文兵, 麦康森, 等. 饲料中豆粕替代鱼粉对大黄鱼生长、消化酶活性和消化道组织学的影响[J]. 中国海洋大学学报(自然科学版), 2012(增刊1): 75-82. |
| [20] |
FAUDZI N M, YONG A S K, SHAPAWI R, et al. Soy protein concentrate as an alternative in replacement of fish meal in the feeds of hybrid grouper, brown-marbled grouper (Epinephelus fuscoguttatus)×giant grouper (E. lanceolatus) juvenile[J]. Aquaculture Research, 2018, 48: 431-441. |
| [21] |
李学丽, 王际英, 宋志东, 等. 两种豆粕部分替代鱼粉在珍珠龙胆石斑鱼幼鱼饲料中的研究[J]. 上海海洋大学学报, 2017, 26(5): 716-725. |
| [22] |
王丽, 张英华. 大豆分离蛋白的凝胶性及其应用的研究进展[J]. 中国粮油学报, 2010, 25(4): 96-99. |
| [23] |
LUSAS E W, RIAZ M N. Soy protein products:processing and use[J]. The Journal of Nutrition, 1995, 125(Suppl.3): 573S-580S. |
| [24] |
姜光丽, 周小秋. 不同大豆蛋白对幼建鲤体蛋白质沉积的影响[J]. 大连海洋大学学报, 2005, 20(2): 81-86. DOI:10.3969/j.issn.1000-9957.2005.02.001 |
| [25] |
WANG Y Y, YANG Y H, WANG F, et al. Effects of replacing fish meal with soybean protein isolate on growth performance and nitrogen and phosphorus excretion of rainbow trout (Oncorhynchus mykiss)[J]. Acta Hydrobiologica Sinica, 2011, 35(1): 105-114. DOI:10.3724/SP.J.1035.2011.00105 |
| [26] |
REFSTIE S, KORSOEN O J, STOREBAKKEN T, et al. Differing nutritional responses to dietary soybean meal in rainbow trout (Oncorhynchus mykiss) and Atlantic salmon (Salmo salar)[J]. Aquaculture, 2000, 190(1): 49-63. |
| [27] |
罗运仙, 谢骏, 吕利群, 等. 饲料中补充晶体或微囊赖氨酸对草鱼生长和血浆总游离氨基酸的影响[J]. 水产学报, 2010, 34(3): 466-473. |
| [28] |
LIOU C H, LIN S C, CHENG J H. Urinary amino acid excretion by marine shrimp, Penaeus monodon, in response to orally administrated intact protein and crystalline amino acids[J]. Aquaculture, 2005, 248(1/2/3/4): 35-40. |
| [29] |
WANG P, ZHU J Q, FENG J, et al. Effects of dietary soy protein concentrate meal on growth, immunity, enzyme activity and protein metabolism in relation to gene expression in large yellow croaker Larimichthys crocea[J]. Aquaculture, 2017, 477: 15-22. DOI:10.1016/j.aquaculture.2017.04.030 |
| [30] |
KOKOU F, SARROPOULOU E, COTOU E, et al. Effects of graded dietary levels of soy protein concentrate supplemented with methionine and phosphate on the immune and anti-oxidant responses of gilthead sea bream (Sparus aurata L.)[J]. Fish & Shellfish Immunology, 2017, 64: 111-121. |
| [31] |
MARTÍNEZ-LLORENS S, MOÑINO A V, VIDAL A T, et al. Soybean meal as a protein source in gilthead sea bream (Sparus aurata L.) diets:effects on growth and nutrient utilization[J]. Aquaculture Research, 2007, 38(1): 82-90. |
| [32] |
姜光丽.SPI和DSBM对幼建鲤体蛋白沉积及消化道蛋白酶活力的影响[D].硕士学位论文.雅安: 四川农业大学, 2003. http://cdmd.cnki.com.cn/Article/CDMD-10626-2004123517.htm
|
| [33] |
赵元, 秦贵信, 王涛, 等. 不同大豆加工制品中主要抗营养因子免疫及抑制活性的比较[J]. 大豆科学, 2007, 26(6): 930-934. DOI:10.3969/j.issn.1000-9841.2007.06.024 |
| [34] |
PENG S, LI D, BING D, et al. Vitamin C:an immunomodulator that attenuates anaphylactic reactions to soybean glycinin hypersensitivity in a swine model[J]. Food Chemistry, 2009, 113(4): 914-918. DOI:10.1016/j.foodchem.2008.08.018 |
| [35] |
GUO P, PIAO X, CAO Y, et al. Recombinant soybean protein beta-conglycinin alpha'-subunit expression and induced hypersensitivity reaction in rats[J]. International Archives of Allergy & Immunology, 2008, 145(2): 102-10. |
| [36] |
孙玲.大豆抗原蛋白对不同食性鱼类消化酶活性及血液指标的影响[D].硕士学位论文.长春: 吉林农业大学, 2008. http://cdmd.cnki.com.cn/Article/CDMD-10193-2009162738.htm
|
| [37] |
杨代勤, 严安生, 陈芳. 几种氨基酸及香味物质对黄鳝诱食活性的初步研究[J]. 水生生物学报, 2002, 26(2): 205-208. DOI:10.3321/j.issn:1000-3207.2002.02.018 |
| [38] |
ALARCÓN F J, GARCÍA-CARREÑO F L, DEL TORO M A N. Effect of plant protease inhibitors on digestive proteases in two fish species, Lutjanus argentiventris and L.novemfasciatus[J]. Fish Physiology and Biochemistry, 2001, 24(3): 179-189. DOI:10.1023/A:1014079919461 |
| [39] |
SVEIER H, KVAMME B O, RAAE A J. Growth and protein utilization in Atlantic salmon (Salmo salar L.) given a protease inhibitor in the diet[J]. Aquaculture Nutrition, 2015, 7(4): 255-264. |
| [40] |
KROGDAHL Å, LEA T B, OLLI J J. Soybean proteinase inhibitors affect intestinal trypsin activities and amino acid digestibilities in rainbow trout (Oncorhynchus mykiss)[J]. Comparative Biochemistry and Physiology Part A:Physiology, 1994, 107(1): 215-219. DOI:10.1016/0300-9629(94)90296-8 |
| [41] |
段培昌, 张利民, 王际英, 等. 新型蛋白源替代鱼粉对星斑川鲽幼鱼生长、体成分和血液学指标的影响[J]. 水产学报, 2009, 33(5): 797-804. |
| [42] |
刘勇, 冷向军, 李小勤. 发酵蛋白在水产饲料中的研究应用[J]. 上海海洋大学学报, 2009, 18(1): 101-106. |
| [43] |
王光锋, 张士璀. 补体和溶菌酶在清除文昌鱼体内细菌中的作用[J]. 水产科学, 2013(9): 497-502. DOI:10.3969/j.issn.1003-1111.2013.09.001 |
| [44] |
BOSHRA H, GELMAN A E, SUNYER J O. Structural and functional characterization of complement C4 and C1s-like molecules in teleost fish:insights into the evolution of classical and alternative pathways[J]. Journal of Immunology, 2004, 173(1): 349-359. |
| [45] |
吴钊, 陈乃松, 华雪铭, 等. 4种豆粕替代鱼粉对大黄鱼生长、抗氧化及抗菌能力的影响[J]. 海洋渔业, 2016, 38(5): 495-506. DOI:10.3969/j.issn.1004-2490.2016.05.006 |
| [46] |
孔纯, 华雪铭, 杨璐, 等. 暗纹东方鲀饲料中豆粕替代鱼粉的营养生理效应及其与大豆抗原蛋白的相关性[J]. 水产学报, 2017, 41(5): 734-745. |
| [47] |
YAN Q, XIE S, ZHU X, et al. Dietary methionine requirement for juvenile rockfish, Sebastes schlegeli[J]. Aquaculture Nutrition, 2007, 13(3): 163-169. |




