2. 塔里木大学动物科学学院, 阿拉尔 843300;
3. 巴彦淖尔市农牧业科学研究院, 巴彦淖尔 015000;
4. 内蒙古富川饲料科技股份有限公司, 巴彦淖尔 015000
2. College of Animal Science, Tarim University, Alar 843300, China;
3. Scientific Research Institute of Agricultural and Animal Husbandry in Bayanur, Bayanur 015000, China;
4. Inner Mongolia Fuchuan Feed Science and Technology Ltd., Co., Bayanur 015000, China
维生素是维持动物健康生长所必需的一类有机化合物,主要作为饲料原料中天然存在的维生素的补充,包括以维生素A、维生素D、维生素E为代表的脂溶性维生素和以B族维生素为代表的水溶性维生素,具有提高动物抗病或抗应激能力、促进生长、改善畜产品品质等作用[1]。维生素A的活性形式包括视黄醇、视黄醛和视黄酸,其不仅能够维持动物的免疫机能和正常视觉功能,还对脂类代谢的调控具有重要作用。维生素D能够调节钙磷平衡,在代谢、细胞增殖与分化、自身免疫、心血管生理功能、神经与肌肉功能及防癌等方面具有重要作用。维生素E具有缓解应激、改善生长性能和提高繁殖性能等作用[2]。由于反刍动物瘤胃微生物不能合成脂溶性维生素[1],因此需要在饲粮中添加维生素A、维生素D和维生素E,以满足反刍动物不同生理阶段对上述维生素的需要。
关于肉羊脂溶性维生素需要量的研究主要集中在20世纪80年代,如育肥期肉羊对维生素A的需要量为330 IU/kg BW[3-4],妊娠期或哺乳期肉羊对维生素A的需要量会相应增加1.8~2.1倍[5];肉羊对于维生素D的维持需要量为30 IU/kg BW,其育肥阶段每增重50 g需要额外添加54 IU/d的维生素D;在饲粮砷不缺乏的前提下,育肥期肉羊对维生素E的需要量为15 IU/kg DM[2]。然而,上述报道中的试验动物均基于国外肉羊品种,其养殖方式均以放牧采食新鲜青绿饲料为主要特点[6-7]。我国受放牧条件的限制,目前肉羊养殖方式以舍饲为主,且受成本的影响,饲喂优质青绿饲料较少,以传统农副产品为主要饲料原料。国外研究的维生素适宜添加量是否适用于我国肉羊还有待进一步验证。因此,本试验旨在通过研究饲粮中部分扣除或过量添加脂溶性维生素(维生素A、维生素D、维生素E)对育肥期杜寒杂交肉羊生长性能、营养物质表观消化率、氮和能量代谢的影响,以明确育肥期肉羊适宜的脂溶性维生素添加量,为我国肉羊脂溶性维生素需要量参数的制订提供依据。
1 材料与方法 1.1 试验条件本试验于2017年7月20日至2017年10月26日在内蒙古富川养殖科技股份有限公司进行,试验期间最低温度为0 ℃,最高温度为29 ℃,平均温度为16.5 ℃。试验中所用维生素A、维生素D、维生素E均购自北京精准动物营养研究中心。饲粮营养成分分析在中国农业科学院饲料研究所和巴彦淖尔市农牧业科学研究院进行。
1.2 试验设计与饲粮试验选用120只90日龄断奶后体重(BW)为(26.0±0.1) kg的杜寒杂交肉羊,公母各占1/2。试验羊于70~75日龄接受免疫,于76~90日龄进行过渡,于90日龄开始正式试验。采用单因素试验设计,试验羊按照BW相近原则随机分到5个组中:对照组(PC组)、对照组基础上扣除30%维生素A组(PC-VA组)、对照组基础上扣除30%维生素D组(PC-VD组)、对照组基础上扣除30%维生素E组(PC-VE组)以及过量添加组(维生素A、维生素D、维生素E添加量为对照组的7.5倍,PC-7.5组),每组24只羊,每个圈饲养2只相同性别的羔羊,即每个组12个重复。PC组维生素A、维生素D和维生素E添加量分别为330 IU/kg BW[3-4]、30 IU/kg BW+350 IU[2]和15 IU/kg BW[2]。预试期10 d,试验期90 d。
|
|
表 1 基础饲粮组成及营养水平(干物质基础) Table 1 Composition and nutrient levels of the basal diet (DM basis) |
每天06:00和18:00饲喂,所有羊只自由采食,每日剩料量不超过前日饲喂量的10%。试验前用强力消毒灵溶液对羊舍的顶部、地面、四壁等喷洒消毒,每个栏位每隔半月消毒1次,并按羊场规定进行四联苗(羊快疫、羊碎死、羊肠毒血症和羔羊痢疾)防疫和饲喂驱虫药。
1.4 样品采集与指标测定及方法 1.4.1 生长性能每天记录每个圈肉羊的饲喂量和剩料量,于正试期第1、30、60和90天晨饲前空腹测定每只试验羊BW,计算各组平均日增重(ADG)、干物质采食量(DMI)和饲料转化率(FCR)。
1.4.2 消化代谢各组选取4只接近平均BW的健康试验羊,公母各2只,分别于试验第40~50天和第80~90天开展消化代谢试验,试验期10 d,前5天为预试期,后5天为正试期。正试期每日晨饲前对每只羊剩料进行称重并采集样品,随后称量排粪量,并按总重的10%采样,将每天采集的粪样混合,然后按照每100 g鲜粪加入10%的稀盐酸10 mL进行固氮。饲料样和粪样置于-20 ℃保存,待测。每天向集尿盆中加入10%稀盐酸100 mL,测量每只羊每天的尿液总量,取总尿量的1%,然后倒入专用尿样瓶中,-20 ℃保存。参照实验室常规成分分析方法《饲料分析及饲料质量检测技术》(第2版)[8]测定饲粮、剩料样和粪样的干物质(DM)、粗蛋白质(CP)、粗脂肪(EE)、中性洗涤纤维(NDF)、酸性洗涤纤维(ADF)、钙(Ca)、磷(P)含量和总能(GE),测定尿样的氮含量和GE,计算各营养物质表观消化率和氮沉积,计算公式为:

|
所有数据经过Excel 2010处理,应用SPSS 17.0统计软件进行单因素方差分析(one-way ANOVA),并采用Duncan氏法进行多重比较,以P < 0.05作为判断差异显著性的标准,0.05≤P < 0.10代表有升高或降低的趋势。
2 结果 2.1 部分扣除或过量添加脂溶性维生素对杜寒杂交肉羊生长性能的影响由表 2和表 3可见,各组公羊和母羊在整个试验期虽然BW差异不显著(P>0.05),但PC-VE组公羊和PC-7.5组母羊的第90天BW为各组最低。各组公羊和母羊在整个试验期(第1~90天)的ADG均差异不显著(P>0.05);在第60~90天,PC-VE组公羊和PC-7.5组母羊ADG显著低于其他各组(P < 0.05),且PC-VE组母羊ADG显著低于PC-VA组(P < 0.05)。各组公羊和母羊在整个试验期的DMI均差异不显著(P>0.05)。
|
|
表 2 部分扣除或过量添加脂溶性维生素对杜寒杂交公羊生长性能的影响 Table 2 Effects of partial deduction or excess amount of fat-soluble vitamins on growth performance of Dorper×thin-tailed Han crossbred rams |
|
|
表 3 部分扣除或过量添加脂溶性维生素对杜寒杂交母羊生长性能的影响 Table 3 Effects of partial deduction or excess amount of fat-soluble vitamins on growth performance of Dorper×thin-tailed Han crossbred ewes |
第60~90天,PC-VE组公羊DMI显著低于其他各组(P < 0.05),PC-7.5组母羊DMI则有低于其他各组的趋势(P=0.06),部分扣除维生素E和试验周期对公羊DMI和ADG存在交互作用(P < 0.05)(图 1)。第60~90天,PC-VE组公羊的FCR有高于其他各组的趋势(P=0.08),PC-7.5组母羊的FCR显著高于其他各组(P < 0.05),摄入高倍剂量脂溶性维生素和试验周期对母羊ADG和FCR存在交互作用(P < 0.05)(图 2)。
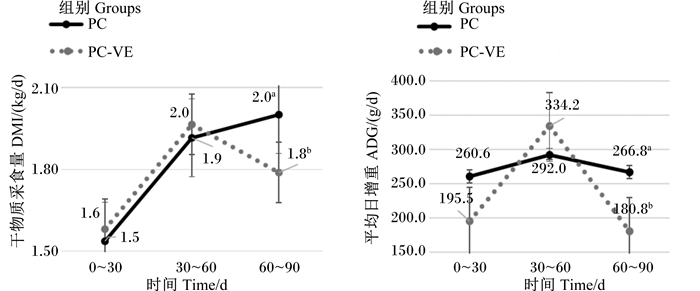
|
图 1 部分扣除维生素E和试验周期对杜寒杂交公羊DMI和ADG的交互作用 Fig. 1 Interaction effects of partial deduction of vitamin E and experimental period on DMI and ADG of Dorper×thin-tailed Han crossbred rams |
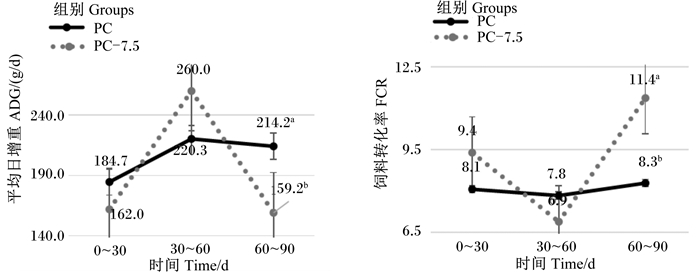
|
图 2 过量添加脂溶性维生素和试验周期对杜寒杂交母羊ADG和FCR的交互作用 Fig. 2 Interaction effects of excess amount of fat-soluble vitamins and experimental period on ADG and FCR of Dorper×thin-tailed Han crossbred ewes |
由表 4可见,在2期消化代谢的结果中,各组肉羊在整个试验期摄入氮、总排出氮、氮利用率和氮表观消化率等指标均差异不显著(P>0.05)。
|
|
表 4 部分扣除或过量添加脂溶性维生素对杜寒杂交肉羊氮代谢的影响 Table 4 Effects of partial deduction or excess amount of fat-soluble vitamins on nitrogen metabolism of Dorper×thin-tailed Han crossbred lambs |
由表 5可见,在2期消化代谢的结果中,各组肉羊在整个试验期摄入总能、总能代谢率、总能表观消化率和消化能代谢率等指标均差异不显著(P>0.05)。
|
|
表 5 部分扣除或过量添加脂溶性维生素对杜寒杂交肉羊能量代谢的影响 Table 5 Effects of partial deduction or excess amount of fat-soluble vitamins on energy metabolism of Dorper×thin-tailed Han crossbred lambs |
由表 6可见,第40~50天,各组各营养物质表观消化率均无显著差异(P>0.05);第80~90天,PC-7.5组粗脂肪表观消化率显著低于PC组和PC-VA组(P < 0.05),各组其他营养物质表观消化率均无显著差异(P>0.05)。摄入高倍剂量脂溶性维生素和试验周期对DM、有机物(OM)、CP和ADF的表观消化率均存在交互作用(P < 0.05),PC-7.5组在第80~90天消化代谢试验中上述指标均显著低于PC组(P < 0.05)(图 3)。
|
|
表 6 部分扣除或过量添加脂溶性维生素对肉羊营养物质表观消化率的影响 Table 6 Effects of partial deduction or excess amount of fat-soluble vitamins on apparent nutrient digestibility of Dorper×thin-tailed Han crossbred lambs |
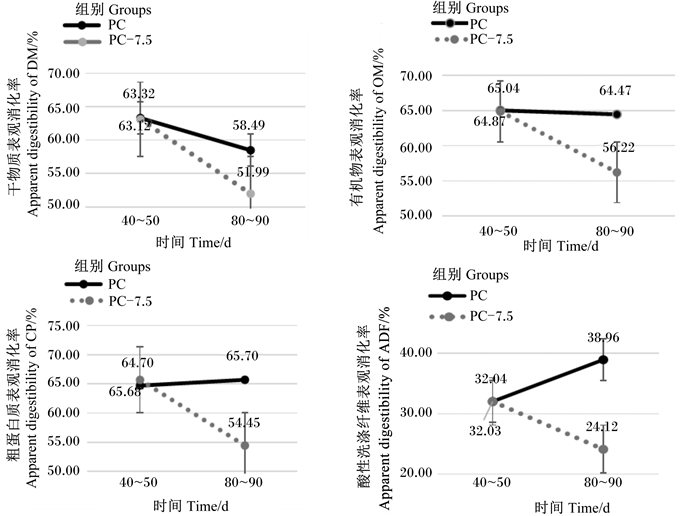
|
图 3 过量添加脂溶性维生素和试验周期对杜寒杂交肉羊营养物质消化率的交互作用 Fig. 3 Interaction effects of excess amount of fat-soluble vitamins and experimental period on apparent nutrient digestibility of Dorper×thin-tailed Han crossbred lambs |
本试验在前人研究结果[2]得出的肉羊育肥阶段脂溶性维生素适宜添加量基础上,分别对维生素A、维生素D、维生素E进行部分扣除,试验结果表明,维生素A、维生素D部分扣除对肉羊生长性能没有负面影响。本试验中PC组的维生素A添加量是参考NRC(2007)[2]推荐量,其提出的育肥羊维生素A适宜添加量是基于Donoghue等[3]试验得出(330 IU/kg BW),但该试验并未以肉羊生长性能为评价指标,而是以血清、尿液以及粪便中的视黄醇含量为评定指标,认为在该添加水平下,肉羊能够保持机体视黄醇代谢稳定,从而维持正常生理功能。本试验并未测定肉羊血清视黄醇含量,但限制30%的维生素A没有对肉羊生长性能和消化代谢产生负面的影响,因此Donoghue等[3]的结果可能高估了杜寒杂交肉羊育肥期对于维生素A的需要量。就维生素D而言,肉羊对于维生素D的维持需要量为30 IU/kg BW,其育肥阶段每增重50 g需要额外添加54 IU/d的维生素D。对于早期断奶的不超过4月龄的小反刍动物,维生素D的需要量要高出育肥阶段肉羊的20%[5]。本试验通过对肉羊生长性能和消化代谢指标的评定,发现NRC(2007)提出的维生素A和维生素D推荐量可能高估了杜寒杂交肉用绵羊发挥正常生长性能的需要,从而可能造成资源的浪费。
本试验中,PC-VE组公羊整个试验期ADG与PC组相比没有显著差异,Dufrasne等[9]在肉牛上研究得出的结论也支持本研究结果,即不同水平的维生素E添加量对肉牛的ADG等生长性能没有显著影响。然而在第60~90天,PC-VE组公羊ADG显著低于PC组,进一步通过交互作用分析发现,长期累积缺乏维生素E能够降低杜寒杂交羊ADG和DMI。此结果与Zhao等[10]在4月龄绵羊的饲粮中补充不同水平的维生素E后对生长性能影响的研究结果一致,即长期缺乏维生素E会导致ADG显著降低。NRC(2007)[2]提出育肥期肉用绵羊饲粮中添加维生素E的最低需要量是10.0 mg/kg DM,然而关于维生素E缺乏对育肥期肉羊生理功能的影响研究较少。Fry等[11]在4月龄美利奴绵羊饲粮中补充α-生育酚(15 mg/d)后,只饲喂大麦和谷壳,不再补充维生素E,进而测定维生素E的消耗情况,结果发现绵羊在此过程中肝脏生育酚含量迅速下降,试验期第2周时2只试验羊出现轻度亚临床营养性肌病,提示缺乏维生素E可能会对肉羊健康状态产生影响,但该试验并未涉及具体肉羊生长性能的变化。从本试验研究结果来看,限制饲粮中30%的维生素E在试验的前2个月能够满足杜寒杂交肉用绵羊发挥正常生长性能,但在育肥期的第3个月(第60~90天)可能会降低其生长性能,表明NRC(2007)[2]提出的肉用羊维生素E推荐量符合本试验条件下杜寒杂交肉羊正常生长的最低需要,但如果延长育肥周期,其推荐量可能无法满足肉羊育肥的需要量,会对生长性能造成负面影响。本试验结果表明,扣除30%的脂溶性维生素对羊只的生长性能没有显著影响,可能NRC标准中的维生素需要量高估了我国的舍饲肉羊的脂溶性维生素需要量。
3.2 过量添加脂溶性维生素对杜寒杂交羊生长性能和消化代谢的影响本试验中过量添加组的设立是考虑NRC提出的中毒剂量(10倍添加量)[2],但考虑到实际生产安全,将最终过量添加量设立为对照组的7.5倍。从结果来看,PC-7.5组母羊ADG在第60~90天显著低于PC组,进一步通过交互作用分析发现,长期摄入高倍剂量脂溶性维生素能够降低杜寒杂交羊ADG,提高FCR。NRC(2007)[2]建议肉羊通过视黄醇或视黄酯的形式摄入维生素A含量不应超过6 000 μg/kg BW(即20 000 IU/kg BW)。已有不同研究发现过量添加维生素A会影响肉羊的生长性能。研究发现,肉用山羊连续7周摄入17 640 μg/kg BW的维生素A后,DMI降低,BW在第8周后降低[12];Donoghue等[13]研究发现,母羊按6 000~18 000 mg/kg BW饲喂维生素A超过6周,每周DMI降低29.8%~52.4%。关于高剂量的维生素D对于肉羊生长性能的影响尚未见报道,Smith等[14]向肉羊肌肉注射维生素D3后,在4种组织中发现过量的维生素D3,可能引起动脉硬化,但是只要将摄入量控制在100 IU/kg BW以下,维生素D3可以维持稳态,因此一般在饲粮中补充过量维生素D不会造成动物中毒。维生素E在机体内的吸收主要发生在小肠,通过淋巴系统和脂蛋白复合物发生转运[15]。Zhao[9]给4月龄绵羊饲粮中补充高倍剂量的维生素E,发现其BW、ADG、DMI等指标均没有受到显著影响。虽然其试验周期与本试验相似,但该研究并未报道试验周期和添加量的交互作用,无法明确长期添加对生长性能的影响;其次上述试验只选用了35只母滩羊作为试验动物,试验动物样本数量相对较少,得出的结果可能具有一定的局限性。上述结果表明,按照NRC提出的中毒剂量的75%添加脂溶性维生素虽然在整个试验期没有显著降低动物的生长性能,但长期摄入可能造成动物ADG和FCR降低,影响肉羊的生长性能。
反刍动物采食饲粮后,含氮物质在机体中消化吸收,一部分氮通过粪便和尿排出体外,另一部分氮吸收后被用于合成机体所需的蛋白质,氮在动物体内的这一过程即为氮代谢[16]。机体摄入营养物质之后,经过吸收和消化代谢产生的能量,以ATP的形式释放得以提供动物自身的营养需要的这一过程即为能量代谢[17]。本试验分别从氮沉积和代谢、能量代谢和表观消化率3个方面研究了杜寒杂交肉羊对营养物质的消化代谢能力。结果表明,长期摄入高倍剂量的脂溶性维生素会降低肉羊DM、OM、EE的表观消化率。杨奇慧[18]研究发现,长期摄入过量维生素A降低动物营养物质消化率的原因可能是降低了小肠绒毛高度,后者是评定肠道消化能力的重要指标,小肠绒毛高度的降低在一定程度上反映了营养物质消化能力的下降。此外,虽然适量摄入维生素D能够有效调节机体对钙、磷吸收,维持血钙和血磷的正常水平,但过量摄入维生素D则会导致机体中有过量的钙,从而在肠道中与脂肪酸形成不溶性的皂化物,使饱和脂肪消化率降低。综合上述研究结果,长期摄入过量的脂溶性维生素A、维生素D、维生素E能够降低杜寒杂交肉羊的营养物质表观消化率,从而影响其生长性能。
4 小结虽然扣除30%或过量添加脂溶性维生素对整个试验期内杜寒杂交肉羊的生长性能和营养物质表观消化代谢没有显著影响,但是通过交互作用分析表明,长期缺乏维生素E会降低杜寒杂交肉羊生长性能和营养物质表观消化率;长期摄入高倍剂量的维生素A、维生素D、维生素E也会降低其生长性能和营养物质表观消化率,影响动物健康生长。
| [1] |
冯仰廉. 反刍动物营养学[M]. 北京: 科学出版社, 2004.
|
| [2] |
NRC. Nutrient requirements of small ruminants:sheep, goats, cervids, and new world camelids[M]. Washington, D.C.: National Academies Press, 2007.
|
| [3] |
DONOGHUE S, KRONFELD D S, SKLAN D. Retinol homeostasis in lambs given low and high intakes of vitamin a[J]. British Journal of Nutrition, 1983, 50(2): 235-248. DOI:10.1079/BJN19830093 |
| [4] |
DONOGHUE S, DONAWICK W J, KRONFELD D S. Transfer of vitamin a from intestine to plasma in lambs fed low and high intakes of vitamin a[J]. The Journal of Nutrition, 1983, 113(11): 2197-2204. DOI:10.1093/jn/113.11.2197 |
| [5] |
NRC. Nutrient requirements of sheep[M]. 6th ed. Washington, D.C.: National Academy Press, 1985.
|
| [6] |
DE RANCOURT M, FOIS N, LAVIN M P, et al. Mediterranean sheep and goats production:an uncertain future[J]. Small Ruminant Research, 2006, 62(3): 167-179. DOI:10.1016/j.smallrumres.2005.08.012 |
| [7] |
WRIGHT A D G, WILLIAMS A J, WINDER B, et al. Molecular diversity of rumen methanogens from sheep in western Australia[J]. Applied and Environmental Microbiology, 2004, 70(3): 1263-1270. DOI:10.1128/AEM.70.3.1263-1270.2004 |
| [8] |
张丽英. 饲料分析及饲料质量检测技术[M]. 2版. 北京: 中国农业大学出版社, 2003.
|
| [9] |
DUFRASNE I, MARCHE C, CLINQUART A, et al. Effects of dietary vitamin E supplementation on performance and meat characteristics in fattening bulls from the Belgian Blue breed[J]. Livestock Production Science, 2000, 65(1/2): 197-201. |
| [10] |
ZHAO T Z, LUO H L, ZHANG Y W, et al. Effect of vitamin E supplementation on growth performance, carcass characteristics and intramuscular fatty acid composition of Longissimus dorsi muscle in Tan'sheep[J]. Chilean Journal Of Agricultural Research, 2013, 73(4): 358-365. DOI:10.4067/S0718-58392013000400005 |
| [11] |
FRY J M, SMITH G M, MCGRATH M C, et al. Plasma and tissue concentrations of α-tocopherol during vitamin E depletion in sheep[J]. British Journal of Nutrition, 1993, 69(1): 225-232. DOI:10.1079/BJN19930024 |
| [12] |
FRIER H I, GORGACZ E J, HALL R C, Jr, et al. Formation and absorption of cerebrospinal fluid in adult goats with hypo-and hypervitaminosis a[J]. American Journal of Veterinary Research, 1974, 35(1): 45-55. |
| [13] |
DONOGHUE S, KRONFELD D S, RAMBERG C F, Jr. Plasma retinol and clearance in hypervitaminosis A[J]. Journal of Dairy Science, 1979, 62(2): 326-332. DOI:10.3168/jds.S0022-0302(79)83243-9 |
| [14] |
SMITH B S, WRIGHT H, AITCHISON G U, et al. Effects in sheep of high dietary levels of vitamin D3 as measured by circulating concentrations of some vitamin D metabolites and skeletal examination[J]. Research in Veterinary Science, 1985, 38(3): 317-321. DOI:10.1016/S0034-5288(18)31802-2 |
| [15] |
MACHLIN L J. Handbook of vitamins[M]. 2nd ed. New York: Marcel Dekker, Inc, 1990.
|
| [16] |
AHMED Y A A.Nitrogen metabolism in ruminants[M].[S.l.]: [s.n.], 2002.
|
| [17] |
KAMALZADEH A, KOOPS W J, KIASAT A. Effect of qualitative feed restriction on energy metabolism and nitrogen retention in sheep[J]. South African Journal of Animal Science, 2009, 39(1): 30-39. |
| [18] |
杨奇慧, 周小秋. 饲料中高水平维生素A对幼建鲤生长、饲料利用及免疫反应的影响[J]. 水产学报, 2007, 31(6): 749-756. |




