2. 黑龙江省农产品加工与质量安全重点实验室, 大庆 163000
2. Key Laboratory of Agricultural Product Processing and Quality Safety in Heilongjiang Province, Daqing 163000, China
植物雌激素主要有3类:异黄酮类(isoflavones)、木酚素类(lignans)和黄豆素类(coumestans),存在于豆类物质、植物及其种子中,其中异黄酮含量较高[1]。异黄酮广泛存在于大豆及其他豆类中,是一种天然的生物活性成分,其生理功能主要表现在抗氧化性、雌激素作用和抗雌激素作用等方面[2-4]。近年来,流行病学研究表明,黑豆异黄酮在预防癌症、骨质疏松症以及在改善妇女绝经期症状方面起着重要作用[5-6]。目前对于黑豆异黄酮的研究主要集中在抗氧化、抗癌等方面,而对抗卵巢衰老方面的研究较少。
早期生长反应基因-1(early growth response gene-1,EGR-1)是一种核转录因子,属于即刻早期基因家族,在体内分布广泛,具有促进细胞生长、增殖、分化等多种生物功能[7-8]。通过调控与细胞生长增殖分化相关的基因来参与细胞生长及分化过程,在遇到刺激反应后被激活,在EGR-1被激活后细胞会快速增殖,对细胞的生长及损伤修复有一定的影响。EGR-1在机体的多种组织器官中均有表达,在组织发育、动物繁殖、机体免疫等生物学功能中均表现出生物学特性[9-10]。目前就EGR-1的相关研究多集中在肿瘤、炎症等方面,在正常机体、组织内的报道较少见,Park等[11]研究发现,EGR-1能够调控正常细胞的凋亡,参与卵泡从发育到闭锁全过程,在此过程中起着重要的调控作用。而前期的研究中发现,异黄酮可对多囊卵巢综合征大鼠、绝经期小鼠卵巢中细胞凋亡因子、关键酶等有显著的调节作用[12-15]。黑豆异黄酮提取的方法有很多,而使用微生物发酵法制备黑豆异黄酮的研究较少[16-17]。豆亚静等[18]采用超声波法提取黑豆异黄酮,得到的提取率仅为1.883%。本研究以脱脂黑豆粉为原料,利用里氏木霉发酵法对发酵时间、瓶装比例、菌液与豆粉的比例进行了研究,拟找到异黄酮适宜的提取条件。本试验为了进一步研究黑豆异黄酮的雌激素样作用对卵巢的影响,以不同日龄大鼠为研究对象,以与卵巢卵泡发育关系密切的反应因子EGR-1作为切入点进行研究,探究黑豆异黄酮对卵巢发育的影响。
1 材料与方法 1.1 试验方法 1.1.1 里氏木霉的活化固体培养基的制备与菌的活化:称取马铃薯葡萄糖琼脂培养基(PDA)粉末9.2 g,放入锥形瓶中,加入200 mL水,将锥形瓶放入微波炉中加热至粉末全部融化,加塞后与培养皿一起灭菌。灭菌后在无菌室内倒平板,待温度冷却后用接种环挑起原菌后划平板,将平板倒置放入DRP-9052型电热恒温培养箱内培养,1~2 d后观察菌的生长情况,未发现有杂菌污染后重复上述的操作再在固体培养基上将菌再培养1代。
液体培养基的制备与菌的活化:将马铃薯去皮、切块,按照配方称取40 g放入烧杯中加水200 mL煮沸30 min(可在煮沸时适时加入少量的水),煮沸后用玻璃棒与纱布将沸液过滤入锥形瓶中,加水至200 mL处,加塞后灭菌。待温度冷却后,在无菌室内用接种环将在固体培养基上培养2代的菌挑入液体培养基内,振荡后放入DRP-9052型电热恒温培养箱内培养1~2 d。
1.1.2 黑豆异黄酮的发酵根据预试验的结果,在确定要加入到锥形瓶中的比例为1 : 10之后,按照菌液与豆粉比例(体积质量比)7 : 1称取1 g脱脂黑豆粉放入其中,加塞灭菌后待温度冷却,在无菌室内加入菌液,放入DK-S24恒温水浴摇床上发酵。
1.1.3 标准品溶液的配制准确称取染料木素标准品1.31 mg,置于10 mL容量瓶中,以95%乙醇溶解,定容,摇匀,浓度为131 mg/L。
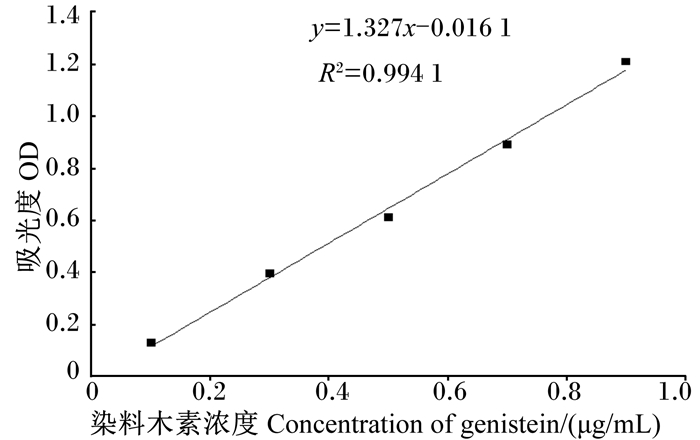
1.1.4 标准曲线的绘制准确吸取0.1、0.3、0.5、0.7、0.9 mL标准溶液分别置于10 mL的容量瓶中,各加10 mL 95%乙醇,再加蒸馏水定容至刻度,摇匀。在265 nm处测量溶液的吸光度(OD)值,重复3次,测定结果取平均值。以OD值为纵坐标,染料木素浓度为横坐标,绘制标准曲线,如图 1。
|
图 1 黑豆异黄酮标准曲线 Fig. 1 Standard curve of black bean isoflavones |
49日龄青年雌性SD大鼠40只,体重(200±20) g;12月龄老年雌性SD大鼠40只,体重(490±20) g,许可证号:SCXK(黑)2013-001。按照体重各分为5组,每组各8只,单笼饲养,根据人体每日摄入黑豆异黄酮的安全限量与大鼠进行换算,黑豆异黄酮和己烯雌酚均用花生油溶解,分别按体重以100、200、300 mg/(kg BW·d)的黑豆异黄酮灌胃,分别记为L、M和H组;阳性对照组根据独立试验结果按体重以0.5 mg/(kg BW·d)的己烯雌酚灌胃,记为PC组;空白组按体重以等剂量花生油灌胃,记为NC组。14 h的周期性光照,温度(20±2) ℃,相对湿度(45±10)%,饮水充足,基础饲粮为自由采食,持续30 d。30 d给药后,对所有大鼠进行阴道涂片观察,挑选出处于动情间期大鼠的,禁食不禁水12 h后,采集卵巢液氮速冻后放入-80 ℃冰箱保存。
1.2 试验材料主要试验仪器包括:DRP-9052型电热恒温培养箱(控温精度0.1 ℃,上海森信试验仪器有限公司)、LDZM-80KCS立式压力蒸汽灭菌锅(上海申安医疗器械厂)、DK-S24恒温水浴摇床(金坛市荣华仪器制造有限公司)、T6新世纪紫外可见分光光度计(北京普析通用仪器有限责任公司)、Anke TGL-16B离心机(上海安亭科学仪器厂)。
主要试验材料包括:脱脂黑豆粉、乙酸乙酯(分析纯),购自天津市大茂化学试剂厂;里氏木霉,黑龙江八一农垦大学食品学院微生物实验室提供;金雀异黄素(98%),购自上海融禾医药科技有限公司;己烯雌酚(99.4%),购自西安天正药用辅料有限公司;花生油,购自山东鲁花集团有限公司。基础饲粮组成及营养水平见表 1。
|
|
表 1 基础饲粮组成及营养水平(风干基础) Table 1 Composition and nutrient levels of the basal diet (air-dry basis) |
将发酵液离心后,取出上清液放入分液漏斗中,加入乙酸乙酯萃取一段时间,将下层液体漏出,保留上层液体倒入烧杯中。用乙酸乙酯作为空白样,使用紫外可见分光光度计在波长为265 nm下进行测定。
1.3.2 Western blot测定卵巢EGR-1蛋白质表达水平称取30 mg卵巢组织,每样本加入500 μL蛋白裂解液和5 μL蛋白酶抑制剂(PMSF),60 Hz匀浆90 s,置于冰上15 min,最后将裂解液转移至新EP管中,14 000 r/min离心10 min,取上清。
蛋白质变性:蛋白质用BCA蛋白质定量试剂盒进行蛋白质定量,酶标仪测定OD值,取等量蛋白质加入6×loading buffer 100 ℃孵育10 min。
电泳:利用垂直电泳仪进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE),蛋白质处于浓缩胶时电压设置为80 V,蛋白质进入分离胶之后电压调制120 V,电泳1 h。
转膜:将凝胶玻璃板置于盛有电泳转移缓冲液的容器中,浸泡15~20 min,裁剪好滤纸和聚偏二氟乙烯(PVDF)膜,滤纸和膜为83 mm×75 mm,尽量避免污染滤纸和膜,将裁剪好的滤纸和膜浸泡于电泳转移缓冲液中,驱除留于膜上的气泡。打开转移盒并放置浅盘中,用转移缓冲液将海绵垫完全浸透后将其放在转移盒壁上,海绵上再放置1张浸湿的滤纸。小心将凝胶放置于滤纸上,避免气泡。用去离子水清洗缓冲液槽,在缓冲液槽中放入搅拌子,将另一块海绵用转移缓冲液浸透后放在凝胶-膜“三明治”上,关上转移盒并插入转移槽。将冰盒装入缓冲液槽,注满4 ℃预冷的转移缓冲液。350 mA恒流转膜75 min。
电转完毕后,将PVDF膜置于5%的脱脂奶粉(TBST配制)中封闭,37 ℃、2 h。
一抗孵育:封闭结束之后,TBST清洗PVDF膜3遍,分别加入以下一抗4 ℃孵育过夜:
EGR-1(1 : 1 000,抗兔),β-肌动蛋白(β-actin)(1 : 5 000,抗小鼠)。
二抗孵育:一抗孵育结束后,用TBST洗3遍,抗小鼠/抗兔(1 : 2 000)二抗室温孵育2 h,TBST脱色摇床清洗3遍。
免疫检测:PVDF膜上均匀滴加ECL化学显色液,发光强度用ImageQuant LAS 4000mini化学发光成像检测仪检测拍照。
采用Quantity one处理照片,测定灰度值。
1.3.3 实时荧光定量PCR测定卵巢EGR-1基因表达水平采用NCBI primer designing tool设计引物,由上海生工生物技术有限公司合成,具体见表 2。
|
|
表 2 实时荧光定量PCR引物 Table 2 Primer of real-time RT-PCR |
Trizol试剂盒提取总RNA;Nanodrop 2000测定RNA的OD260/OD280值,1.8~2.0符合要求。cDNA转录条件如下。
总体积25 μL:RNA-Primer Mix 12 μL,5×RT Reaction Buffer 5 μL,25 mmol/L三磷酸碱基脱氧核苷酸(dNTPs)1 μL,25 U/μL RNase Inhibitor 1 μL,200 U/μL M-MLV Rtase 1 μL,Oligo(dt)18 1 μL,ddH2O 4 μL。
反应程序:37 ℃,60 min;85 ℃,5 min;4 ℃,5 min;-20 ℃保存。
实时荧光定量PCR反应条件:总体积25 μL,cDNA 2 μL,SYBR Green Mix 12.5 μL,上游引物0.5 μL,下游引物0.5 μL,ddH2O 9.5 μL。
反应程序:95 ℃,10 min (95 ℃,15 s;60 ℃,45 s)×40;95 ℃,15 s;60 ℃,1 min;95 ℃,15 s;60 ℃,15 s。
1.4 单因素试验每个因素的改变对结果的影响都不同,为了确定单因素对发酵提取量的影响,本试验以发酵时间、瓶装比例、菌液与豆粉的比例3个因子作为单因素的研究对象。
1.5 正交试验通过改变发酵条件:发酵时间、瓶装比例、菌液与豆粉的比例,以此3个因素中的各个因素的3个因素水平进行正交试验,确定在此3个因素水平中里氏木霉发酵提取黑豆异黄酮的最佳因素水平。
1.6 数据统计分析试验数据采用SPSS 19.0及Excel 2007软件进行统计分析和数据处理,进行单因素方差分析(one-way ANOVA),GraphPad Prism 5.0软件作图处理,并采用Origin 8.0软件绘制曲线。P < 0.05表示差异显著,P < 0.01表示差异极显著。
2 结果与分析 2.1 发酵时间的探究根据预试验的结果,确定不变量为瓶装比例为1 : 9,菌液与豆粉的比例为7 : 1,以发酵时间24、36、48、60、72 h为变量,探究发酵时间对黑豆异黄酮提取率的单因素试验。
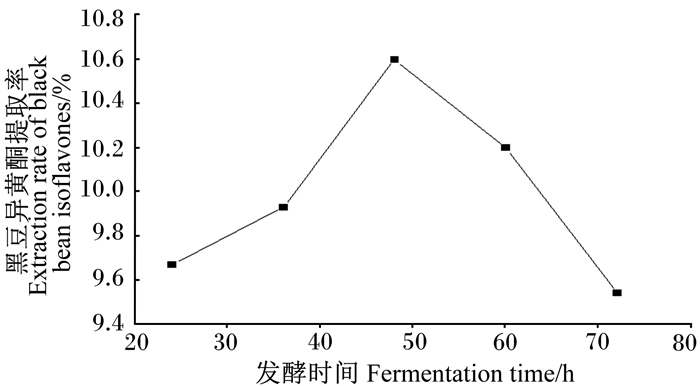
根据对发酵时间的单因素试验结果可以看出(图 2),当其他2个变量不变时,随着发酵时间的增加,曲线先呈上升趋势,在发酵时间为48 h时提取率达到最高值(10.60%),随后呈下降趋势,在发酵时间为72 h时提取率达到最低值(9.54%)。
|
图 2 发酵时间对黑豆异黄酮提取率的影响 Fig. 2 Effects of fermentation time on extraction rate of black bean isoflavones |
根据预试验结果,确定不变量为发酵时间48 h,菌液与豆粉的比例7 : 1,以瓶装比例1 : 10、1 : 9、1 : 8、1 : 7、1 : 6为变量,探究瓶装比例对黑豆异黄酮提取率的单因素试验。
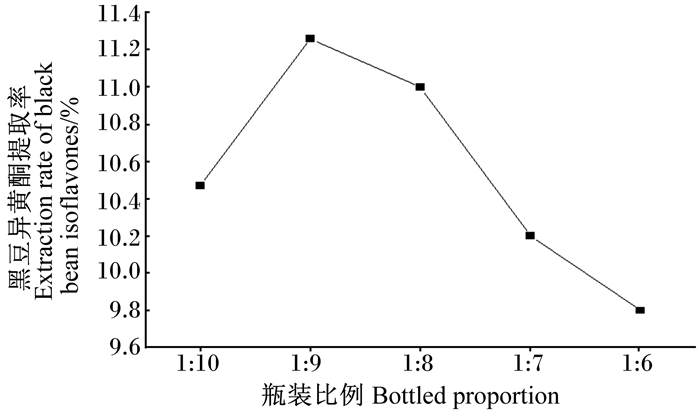
根据对瓶装比例的单因素试验结果可以看出(图 3),当其他2个变量不变时,随着瓶装比例的改变,曲线先呈上升趋势,在瓶装比例为1 : 9时提取率达到最高值(11.26%),随后呈下降趋势,在瓶装比例为1 : 6时提取率达到最低值(9.8%)。
|
图 3 瓶装比例对黑豆异黄酮提取率的影响 Fig. 3 Effects of bottled proportion on extraction rate of black bean isoflavones |
根据预试验的结果,确定不变量为发酵时间48 h,瓶装比例为1 : 9,以菌液与豆粉的比例5 : 1、6 : 1、7 : 1、8 : 1、9 : 1为变量,探究菌液与豆粉比例对黑豆异黄酮提取率的单因素试验。
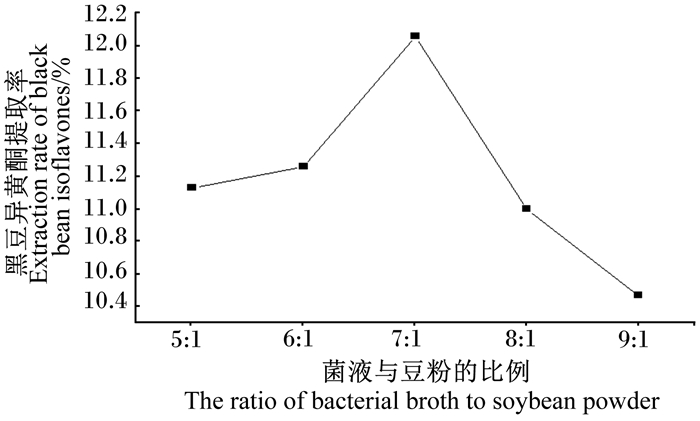
根据对菌液与豆粉比例的单因素试验结果可以看出(图 4),当其他2个变量不变时,随着菌液与豆粉比例的改变,曲线先呈上升趋势,在菌液与豆粉比例为7 : 1时提取率达到最高值(12.06%),随后呈下降趋势,在菌液与豆粉比例为9 : 1时提取率达到最低值(10.47%)。
|
图 4 菌液与豆粉的比例对黑豆异黄酮提取率的影响 Fig. 4 Effects of ratio of bacterial broth to soybean powder on extraction rate of black bean isoflavones |
为了全面考察影响因素,试验结果选用了L9(33)正交设计进行试验。里氏木霉发酵提取黑豆异黄酮正交试验因素水平见表 3。
|
|
表 3 里氏木霉发酵提取黑豆异黄酮正交试验因素水平 Table 3 Orthogonal experiment levels of extraction of black bean isoflavones by Trichoderma reesei fermentation |
运用极差分析法对里氏木霉发酵提取黑豆异黄酮的正交试验结果进行分析,由表 4可以看出:在所选的3个因素中影响异黄酮提取率大小的次序为A>C>B,即发酵时间>菌液与豆粉的比例>瓶装比例。比较k值可得出里氏木霉发酵提取黑豆异黄酮的最优组合为A2B1C2,即当发酵时间、瓶装比例、菌液与豆粉比例分别为48 h、1 : 10、7 : 1时,此时的黑豆异黄酮提取率最高,约为12.06%。
|
|
表 4 里氏木霉发酵提取黑豆异黄酮正交试验结果 Table 4 Orthogonal experiment results of extraction of black bean isoflavones by Trichoderma reesei fermentation |
按照正交试验所得到的最优条件(发酵时间、瓶装比例、菌液与豆粉比例分别为48 h、1 : 10、7 : 1时)进行发酵,利用AB-8大孔树脂吸附法对发酵液进行分离纯化,得到的黑豆异黄酮的纯度为60.2%。
2.5 黑豆异黄酮对大鼠体重和卵巢/体重的影响如表 5所示,在青年组中,L、M组与NC组比较,体重显著增加(P < 0.05);在老年组中,各组间体重差异不显著(P>0.05)。
|
|
表 5 青年和老年雌性大鼠体重 Table 5 Weight of young and old female rats (n=8) |
如表 6所示,在青年组中,M、PC组与NC组比较,卵巢/体重极显著降低(P<0.01);在老年组中,L组与NC组比较,卵巢/体重显著降低(P<0.05)。
|
|
表 6 青年和老年雌性大鼠卵巢/体重 Table 6 Ovarian/body weight of young and old female rats (n=8) |
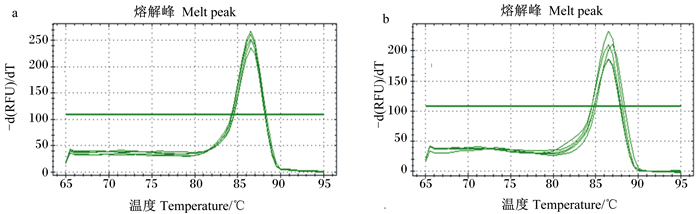
如图 5所示,青年和老年组EGR-1蛋白质的PCR溶解曲线呈现单一峰,引物的特异性较好。
|
a、b分别是青年、老年组EGR-1蛋白质的PCR溶解曲线。 a and b represent the PCR solubility curves of EGR-1 protein of young and old groups, respectively. 图 5 EGR-1蛋白质的PCR溶解曲线 Fig. 5 PCR solubility curves of EGR-1 protein |
如表 7所示,在青年组中,L、M、H组与NC组比较,EGR-1蛋白质表达水平极显著提高(P<0.01);在老年组中,L、M、H组与NC组比较,EGR-1蛋白质表达水平显著或极显著提高(P<0.05或P<0.01)。老年组与青年组之间比较,EGR-1蛋白质表达水平在L、M组差异极显著(P<0.01)。
|
|
表 7 青年和老年雌性大鼠卵巢EGR-1蛋白质的表达 Table 7 Expression of EGR-1 protein in ovary of young and old female rats (n=8) |
如表 8所示,在青年组中,M、H组与NC组比较,EGR-1 mRNA表达水平显著提高(P<0.05);在老年组中,L、M、H组与NC组比较,EGR-1 mRNA表达水平显著或极显著提高(P<0.05或P<0.01)。老年组与青年组之间比较,EGR-1 mRNA表达水平在L、H组差异显著或极显著(P<0.05或P<0.01)。
|
|
表 8 青年和老年雌性大鼠卵巢EGR-1 mRNA的表达 Table 8 Expression of EGR-1 mRNA in ovary of young and old female rats (n=8) |
异黄酮中只有游离型的苷元具有较高的活性,而异黄酮提取物主要为异黄酮苷,异黄酮苷元的含量极少[19]。大豆本身含有的β-葡萄糖苷酶可以将异黄酮苷水解成相应的苷元,但是水解效率极低,通过里氏木霉发酵可以提高β-葡萄糖苷酶的活性,提取率显著提高[20]。杨守凤等[21]在EM菌发酵豆粕转化大豆异黄酮的试验中得到了与本研究类似的结果;同样,许晶等[22]研究发现,影响里氏木霉β-葡萄糖苷酶水解大豆异黄酮效率的主次因素依次为水解时间>加酶量>pH>温度。不同的是,吴少杰等[23]利用海洋拟诺卡氏菌株HY-G转化大豆异黄酮苷的试验中发现,发酵条件影响因素的主次关系为培养温度>装液量>起始pH>培养时间。采用微生物转化法水解大豆异黄酮苷的研究较多,但采用的菌株多为霉菌和细菌类,采用里氏木霉发酵异黄酮的研究较少。本研究中,里氏木霉发酵黑豆异黄酮影响因素主次关系为发酵时间>菌液与豆粉的比例>瓶装比例。
EGR-1是重要的核转录因子,其编码多种蛋白质,在调控细胞的生长、分化、发育、增殖、炎性反应等方面发挥重要作用[24]。Wang等[25]研究表明,EGR-1可以通过诱导B淋巴细胞瘤-2相关X蛋白(Bax)作为胰腺癌细胞的促凋亡因子。也有学者发现,EGR-1在肝损伤的过程及损伤颈动脉内膜增生中还具有一定的保护效果[26-27],田图磊等[28]研究发现,在酒精性脂肪肝肝组织中EGR-1 mRNA表达水平明显上升,推测EGR-1可能参与了酒精性脂肪肝的发病机制,由此可以看出体内的EGR-1 mRNA表达水平与机体的状态密切相关。EGR-1也参与卵泡从发育到闭锁全过程,在此过程中起着重要的调控作用。黄舒颖等[29]研究发现,EGR-1在恶性卵巢肿瘤组织中的表达水平比正常卵巢要低,表示其可作为预后判断的指标,赖志文等[30]发现,EGR-1在卵泡的整个生长阶段均表达,且其强度逐渐增强,表明EGR-1参与了卵泡从发育到闭锁的全过程,并可能在此过程中起着重要的调控作用,这与我们研究的黑豆异黄酮对大鼠卵巢EGR-1表达的研究有相同之处。本试验中,黑豆异黄酮低、中、高剂量组的青年和老年大鼠卵巢内EGR-1蛋白质表达水平均较NC组显著升高。给予200和300 mg/kg的黑豆异黄酮后,青年和老年各剂量组大鼠卵巢EGR-1 mRNA表达水平较NC组显著升高;而给予100和200 mg/kg的黑豆异黄酮后,老年各剂量组大鼠卵巢EGR-1 mRNA表达水平较NC组显著升高,与PC组效果相似。100 mg/kg的黑豆异黄酮对青年大鼠卵巢EGR-1 mRNA表达水平无显著影响,但对老年大鼠影响显著,说明不同剂量的黑豆异黄酮对青年和老年大鼠的影响是不同的。以上研究说明黑豆异黄酮能显著提高EGR-1 mRNA表达水平,从而促进卵泡的发育。
4 结论① 各因素对里氏木霉发酵黑豆异黄酮影响的大小顺序为发酵时间>菌液与豆粉的比例>瓶装比例。当发酵时间、瓶装比例、菌液与豆粉比例分别为48 h、1 : 10、7 : 1时,黑豆异黄酮提取率最高,为12.06%。
② 黑豆异黄酮能增加青年大鼠的体重,200 mg/kg的黑豆异黄酮对青年大鼠的卵巢发育产生一定的影响。黑豆异黄酮可提高青年和老年大鼠的卵巢EGR-1 mRNA和蛋白质的表达水平,进而起到调节卵巢功能、修复卵巢的作用。
| [1] |
FERRER I, THURMAN E M, CHURLEY M, 等. 用Agilent 7000 GC/MS/MS分析豆奶中的八种植物雌激素[J]. 食品安全导刊, 2010(7): 36-38. |
| [2] |
余强, 郭传勇. 大豆异黄酮药理作用及其临床应用[J]. 世界临床药物, 2018, 39(9): 74-77. |
| [3] |
张翠芬. 大豆异黄酮对心血管疾病的研究综述[J]. 中国食品添加剂, 2018(9): 180-183. |
| [4] |
石群, 李波. 大豆异黄酮研究进展及前景展望[J]. 大豆科技, 2018(5): 41-43. |
| [5] |
刘春龙, 李忠秋, 孙海霞, 等. 大豆异黄酮的生理作用及其在医学方面的研究进展[J]. 大豆科学, 2008, 27(4): 693-696. |
| [6] |
王宁涛, 黄争美, 张志愿, 等. 大豆异黄酮抗骨质疏松作用的研究进展[J]. 中华实验外科杂志, 2018, 35(1): 176-178. DOI:10.3760/cma.j.issn.1001-9030.2018.01.057 |
| [7] |
BHATTACHARYYA S, WU M H, FANG F, et al. Early growth response transcription factors:key mediators of fibrosis and novel targets for anti-fibrotic therapy[J]. Matrix Biology, 2011, 30(4): 235-242. DOI:10.1016/j.matbio.2011.03.005 |
| [8] |
CALOGERO A, LOMBARI V, GREGORIO G D, et al. Inhibition of cell growth by EGR-1 in human primary cultures from malignant glioma[J]. Cancer Cell International, 2004, 4: 1. DOI:10.1186/1475-2867-4-1 |
| [9] |
朱涛涛, 朱宇旌, 张勇, 等. 早期生长反应因子-1生物学特性及功能[J]. 动物营养学报, 2013, 25(4): 685-691. DOI:10.3969/j.issn.1006-267x.2013.04.003 |
| [10] |
LU Y F, LI T, QURESHI H Y, et al. Early growth response 1 (EGR-1) regulates phosphorylation of microtubule-associated protein tau in mammalian brain[J]. Journal of Biological Chemistry, 2011, 286(23): 20569-20581. DOI:10.1074/jbc.M111.220962 |
| [11] |
PARK S E, LEE S W, HOSSAIN M A, et al. A chenodeoxycholic derivative, HS-1200, induces apoptosis and cell cycle modulation via EGR-1 gene expression control on human hepatoma cells[J]. Cancer Letters, 2008, 270(1): 77-86. DOI:10.1016/j.canlet.2008.04.038 |
| [12] |
CHI X X, ZHANG T, CHU X L, et al. The regulatory effect of Genistein on granulosa cell in ovary of rat with PCOS through Bcl-2 and Bax signaling pathways[J]. Journal of Veterinary Medical Science, 2018, 80(8): 1348-1355. DOI:10.1292/jvms.17-0001 |
| [13] |
迟晓星, 张明玉, 张涛, 等. 金雀异黄素对多囊卵巢综合征大鼠卵巢组织中Bcl-2及Bax mRNA表达的影响[J]. 动物营养学报, 2014, 26(4): 1120-1126. DOI:10.3969/j.issn.1006-267x.2014.04.034 |
| [14] |
迟晓星, 甄井龙, 张涛, 等. 金雀异黄素对围绝经期小鼠卵巢和子宫组织中芳香化酶和FSHR的调控作用[J]. 中国食品学报, 2017, 8(17): 86-91. |
| [15] |
甄井龙, 初晓丽, 丛莎, 等. 金雀异黄素对青年雌性大鼠卵巢组织中雄激素生成关键酶StAR、P450scc、CYP19基因表达的影响[J]. 食品科学, 2018, 39(11): 171-176. DOI:10.7506/spkx1002-6630-201811027 |
| [16] |
张星, 刘振春, 董欣, 等. 黑豆异黄酮超声波微波辅助提取工艺的响应面优化[J]. 西北农林科技大学学报(自然科学版), 2017, 45(6): 185-192. |
| [17] |
郭婕, 刘中华, 袁淑培, 等. 黑豆中大豆异黄酮微波提取工艺的优化[J]. 食品工业科技, 2015, 36(5): 255-257, 305. |
| [18] |
豆亚静, 张晓龙, 常丽新, 等. 响应面优化超声波法提取黑豆异黄酮的工艺研究[J]. 食品工业科技, 2013, 34(5): 259-263. |
| [19] |
王欣欣.利用黄浆水制备富含苷元型大豆异黄酮发酵乳的研究[D].硕士学位论文.青岛: 中国海洋大学, 2014. http://cdmd.cnki.com.cn/article/cdmd-10423-1014329367.htm
|
| [20] |
蒋大海, 田娟娟, 白志明. 固态发酵法制备大豆异黄酮苷元[J]. 食品科学, 2008, 29(4): 163-166. DOI:10.3321/j.issn:1002-6630.2008.04.031 |
| [21] |
杨守凤, 徐建雄. 基于微生物固态发酵豆粕转化大豆异黄酮的研究[J]. 现代食品科技, 2013, 29(8): 1867-1871. |
| [22] |
许晶, 孙艳梅, 张永忠. 里氏木霉β-葡萄糖苷酶水解大豆异黄酮糖苷的工艺研究[J]. 中国粮油学报, 2009, 24(3): 31-34. |
| [23] |
吴少杰, 焦豫良, 朱强, 等. 海洋拟诺卡氏菌株HY-G转化大豆异黄酮苷发酵条件的优化[J]. 食品科学, 2011, 32(7): 273-278. |
| [24] |
ZHANG Y X, BONZO J A, GONZALEZ F J, et al. Diurnal regulation of the early growth response 1 (EGR-1) protein expression by hepatocyte nuclear factor 4α (HNF4α) and small heterodimer partner (SHP) cross-talk in liver fibrosis[J]. Journal of Biological Chemistry, 2011, 286(34): 29635-29643. DOI:10.1074/jbc.M111.253039 |
| [25] |
WANG C, HUSAIN K, ZHANG A Y, et al. EGR-1/Bax pathway plays a role in vitamin E δ-tocotrienol-induced apoptosis in pancreatic cancer cells[J]. The Journal of Nutritional Biochemistry, 2015, 26(8): 797-807. DOI:10.1016/j.jnutbio.2015.02.008 |
| [26] |
PRITCHARD M T, COHEN J I, ROYCHOWDHURY S, et al. Early growth response-1 attenuates liver injury and promotes hepatoprotection after carbon tetrachloride exposure in mice[J]. Journal of Hepatology, 2010, 53(4): 655-662. DOI:10.1016/j.jhep.2010.04.017 |
| [27] |
张希, 苗驰. 构建颈动脉损伤模型大鼠早期生长反应因子1及组织因子的表达[J]. 中国组织工程研究, 2015, 19(27): 4293-4298. DOI:10.3969/j.issn.2095-4344.2015.27.006 |
| [28] |
田图磊, 洪汝涛, 徐德祥, 等. EGR-1在大鼠酒精性脂肪肝中的表达及水飞蓟素对其干预作用[J]. 安徽医药, 2013, 17(1): 18-21. DOI:10.3969/j.issn.1009-6469.2013.01.007 |
| [29] |
黄舒颖, 卿城, 朱元方. 早期生长反应因子1在正常卵巢及卵巢良、恶性肿瘤组织中的表达及意义[J]. 广东医学, 2015, 36(7): 1045-1048. |
| [30] |
赖志文, 罗爱月, 杨书红, 等. 小鼠卵泡发育不同阶段EGR-1、Gadd45α蛋白表达及相互关系[J]. 现代妇产科进展, 2009, 18(11): 836-839. |




