随着养猪业的不断发展,集约化养殖已经成为一种趋势,并且随着集约化规模越来越大,为了提高生产效率,早期断奶技术的应用也越来越多。但是,仔猪早期断奶会产生免疫功能抑制、代谢紊乱、肠胃功能紊乱以及生长性能下降的不利影响[1],尤其是早期断奶仔猪在断奶后的2周内对脂肪的消化能力很低,而在第3周或第4周之后就可以很好地消化[2]。精氨酸(arginine,Arg)是维持幼年动物最佳的生长和氮平衡的必需氨基酸[3]。有研究表明,一氧化氮合酶从精氨酸开始合成一氧化氮,而一氧化氮作为信号分子,其生理水平能够调控肝脏的脂肪酸氧化,促进脂代谢[4]。周笑犁等[5]研究表明,饲粮中添加精氨酸可显著下调环江香猪肝脏中乙酰辅酶A羧化酶(acetyl-CoA carboxylase,ACC)mRNA的表达,并显著上调肝脏中过氧化物酶体增殖物激活受体γ(peroxisome proliferator-activated receptor γ,PPARγ)mRNA的表达,从而促进脂代谢;胡诚军等[6]研究发现在饲粮中添加1%精氨酸和1%谷氨酸能够使皮下脂肪组织中ACC和脂肪酸转运蛋白4(fatty acid transporter 4,FATP4)mRNA的表达水平显著降低,背最长肌中脂蛋白脂肪酶(lipoprotein lipase,LPL)mRNA的表达水平显著升高。因此,我们推测哺乳期补饲精氨酸可能可以调节断奶仔猪的肝脏脂代谢功能。本实验室之前研究过血液中脂代谢的变化,在前期研究基础上,本研究进一步通过研究断奶仔猪肝脏脂代谢相关指标以及脂代谢相关基因指标,说明精氨酸对断奶仔猪肝脏脂代谢功能的影响,进一步探究其影响的机制,以期为后人研究断奶仔猪肝脏脂代谢提供相关参考。此外,由于猪与人的消化代谢模式相近,本研究也有助于为阐明人类脂肪代谢相关机理和提高人类自身的健康水平提供参考。
1 材料与方法 1.1 试验设计选择具有相似体重和相似胎次(3~4胎)的母猪所生的仔猪,成对选取7日龄时体重相似的健康“杜×长×大”哺乳仔猪40头,随机分为对照组(CON组)和精氨酸组(Arg组),每组20头猪(公母各占1/2)。7日龄起,在自然哺乳的同时,CON组仔猪每日灌服40 mL生理盐水,Arg组仔猪每日灌服40 mL精氨酸[250 mg/(kg·d)]。所有仔猪21日龄断奶,饲喂基础饲粮。每组分别在断奶当天(21日龄)和断奶后第3天(24日龄)每次随机选择8头仔猪(公母各占1/2)屠宰,然后对其肝脏组织进行甘油三酯(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)和高密度脂蛋白胆固醇(HDL-C)等相关指标的测定,以及LPL、脂肪酸合成酶(FAS)、过氧化物酶体增殖物激活受体α(PPARα)等基因的表达测定。根据NRC(2012)仔猪营养需求并结合生产实践制备仔猪的基础饲粮,其组成及营养水平见表 1。
|
|
表 1 基础饲粮组成及营养水平(风干基础) Table 1 Composition and nutrient levels of the basal diet (air-dry basis) |
该试验于2018年7月在太仓市金诸种猪场进行。7~20日龄期间CON组和Arg组仔猪自由哺乳,每日2次分别补饲0.9%生理盐水和精氨酸水溶液(灌服时间分别为08:00和14:00)。所用仔猪在21日龄时断奶,CON组和Arg组在21~24日龄期间饲喂基础饲粮,每日饲喂3次(饲喂时间分别为08:00、14:00和20:00),每次添加的量以料槽中略有剩余为宜,自由饮水。每天清理围场,保持围场清洁,日常管理、消毒、防疫生产按照养猪场的正常程序进行。
1.3 屠宰与样品采集在断奶当天(21日龄)和断奶后第3天(24日龄)每组随机选择8头仔猪(公母各占1/2)进行屠宰和采样,屠宰前对每头仔猪进行称重,电击后颈静脉放血致死,进行屠宰解剖,分离出肝脏,在肝脏中部用刀划出方块状肝脏组织,用4%多聚甲醛固定,用于光镜试验。同时另取肝脏组织存贮于2 mL冻存管,随后保存于液氮罐中,后移至-80 ℃保存待测。
1.4 测定指标与方法 1.4.1 肝脏指数测定试验断奶当天(21日龄)和断奶后第3天(24日龄),每头仔猪进行称重并记录下各组仔猪的体重。称重后经过重度电击屠宰解剖后,将肝脏分离,剥离胆囊,吸水纸吸收表面多余的血液,立即称重,记录并计算肝脏指数。肝脏指数计算公式如下:
肝脏指数(g/kg)=器官重(g)/活体重(kg)。
1.4.2 肝脏组织切片试验结束后取肝脏组织用4%多聚甲醛固定。制作肝脏组织切片。通过显微镜(Olympus CKX41, 日本)拍摄染色部分的代表性图像,使用Image-Pro Plus 6.0软件测量肝细胞的大小。将每个组织切成5个切片,每个切片计数3个不同视野中30个细胞的面积和粒径,最后取平均值。
1.4.3 脂代谢相关指标测定从-80 ℃冰箱取出肝脏样本,重约260 mg,以1 : 9(质量体积比)比例加入盐水溶液,冰浴条件下机械均质化,2 500 r/min离心10 min,取上清液待测。采用试剂盒测定TC、TG、HDL-C和LDL-C含量,试剂盒均购自南京建成生物工程研究所,严格按照试剂盒说明操作。
1.4.4 脂代谢相关基因表达测定从-80 ℃取出肝脏样品,使用Trizol提取样品的总RNA,测定纯度(Applied BiosystemsTM 7500),RNA质量通过琼脂糖凝胶电泳鉴定。将合格的RNA反转录为cDNA,存放于-80 ℃中待测,具体方案根据TaKaRa试剂盒说明书(TaKaRa RR047A)进行。通过NCBI PubMed获得所需的引物,引物序列如表 2所示。特异性引物由金维智生物科技有限公司(GENEWIZ,苏州)合成。以磷酸甘油醛脱氢酶(glyceraldehyde phosphate dehydrogenase, GAPDH)作为内参,对目的基因进行相对定量分析。使用2-ΔΔCt方法计算目的基因的相对表达水平。反转录和荧光定量试剂盒购自TaKaRa生物技术有限公司,并且严格按照说明书中规定的程序进行操作。
|
|
表 2 实时荧光定量PCR引物序列 Table 2 Primer sequences of real time quantitative PCR |
在用Excel 2016对测试数据进行初步计算后,采用SPSS 23.0软件对测试数据进行统计分析。肝脏指数、肝细胞粒径、脂代谢相关指标以及基因表达指标等数据采用两因素方差分析,时间和精氨酸作为固定效应。CON组和Arg组2组之间再用独立t检验进一步进行差异分析。显著性差异水平为P < 0.05,极显著性差异水平为P < 0.01。
2 结果 2.1 哺乳期补饲精氨酸对断奶仔猪肝脏器官发育的影响由表 3可知,断奶后第3天(24日龄)断奶仔猪的体重、肝脏重和肝脏指数均极显著低于断奶当天(21日龄)(P < 0.01);与CON组相比,Arg组仔猪断奶后第3天肝脏指数极显著提高(P < 0.01)。
|
|
表 3 哺乳期补饲精氨酸对断奶仔猪肝脏器官发育的影响 Table 3 Effects of arginine supplementation during the lactation period on liver organ development of weaned piglets |
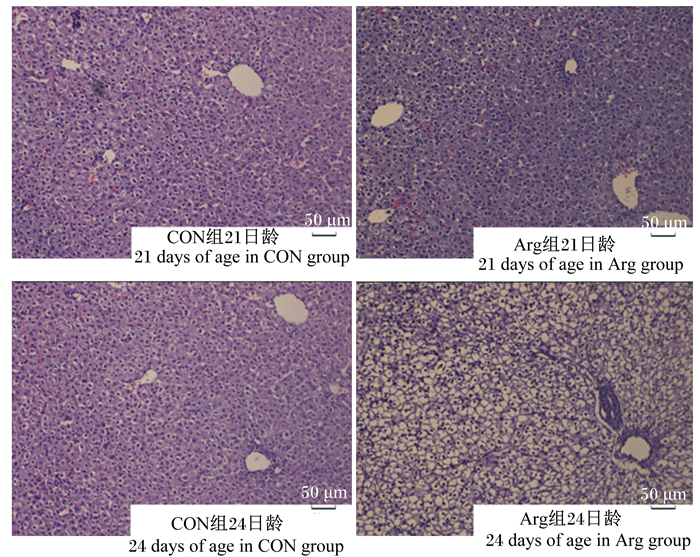
由图 1可知,Arg组仔猪肝脏细胞较清晰,排列较整齐。由表 4可知,与CON组相比,Arg组仔猪肝细胞粒径极显著提高(P < 0.01),肝细胞面积显著提高(P<0.05)。
|
图 1 断奶仔猪肝脏组织切片 Fig. 1 Liver tissue section of weaned piglets (400×) |
|
|
表 4 哺乳期补饲精氨酸对断奶仔猪肝脏细胞大小的影响 Table 4 Effects of arginine supplementation during the lactation period on liver cell size of weaned piglets |
由表 5可知,断奶后第3天仔猪肝脏中TC和TG含量极显著高于断奶当天(P < 0.01),Arg组仔猪肝脏中LDL-C含量极显著低于CON组(P < 0.01)。CON组和Arg组仔猪肝脏中TC和TG含量无显著差异(P>0.05)。断奶当天,Arg组仔猪肝脏中HDL-C含量显著高于CON组(P < 0.05)。
|
|
表 5 哺乳期补饲精氨酸对断奶仔猪肝脏脂代谢相关指标的影响 Table 5 Effects of arginine supplementation during the lactation period on liver lipid metabolism related indices of weaned piglets |
由表 6可知,断奶当天,Arg组仔猪肝脏LPL基因相对表达水平显著高于CON组(P < 0.05),其他脂代谢相关基因相对表达水平无显著差异(P>0.05)。
|
|
表 6 哺乳期补饲精氨酸对断奶仔猪肝脏脂代谢相关基因表达的影响 Table 6 Effects of arginine supplementation during the lactation period on expression of genes related to lipid metabolism in liver of weaned piglets |
肝脏作为能量代谢的中枢器官,在脂肪生成、糖异生和脂质的分解代谢上起着非常重要的作用[7],而且能量和脂质的代谢之间的平衡在维持肝功能方面十分重要。脂代谢与机体健康关系密切,并且它还为机体提供能量生成基质[8]。所以,肝脏是研究机体脂代谢合适的靶器官,它对机体中脂代谢相关酶以及脂蛋白的合成与释放有着十分重要的影响[9]。而器官指数是判断动物体器官发育状况的一种重要的指标,对我们判断动物器官健康状况具有一定指导意义[10]。本试验中,Arg组仔猪断奶后第3天肝脏指数极显著高于CON组。此结果表明,哺乳期补饲精氨酸能够有效缓解断奶应激对肝脏重的影响,这与彭瑛等[11]的研究结果基本一致,我们推断哺乳期补饲精氨酸能够对断奶仔猪肝脏发育有一定的促进作用。我们进一步通过苏木精-伊红(HE)染色切片,观察肝脏细胞发育情况,从而了解断奶仔猪的组织学的变化或者是否发生组织损伤。在正常生理条件下,肝组织HE染色图中的肝细胞排列整齐,放射状排列在中央静脉中央周围,肝细胞排列整齐,无细胞变性和异常[12]。本试验研究发现,2组仔猪肝细胞均清晰,无病理变化,Arg组仔猪肝细胞粒径和肝细胞面积显著提高,Arg组的断奶仔猪肝脏发育程度更好一些,从而推测其营养代谢功能(脂代谢)可能强于CON组断奶仔猪。本试验中,Arg组仔猪肝脏发育更好,但其脂代谢功能是否受到影响需要进一步研究。
3.2 哺乳期补饲精氨酸对断奶仔猪肝脏脂代谢的影响通过动物脂代谢相关产物含量以及相关基因表达水平的情况能够判断仔猪的脂代谢功能的强弱[13]。脂代谢功能的强弱与动物的生长、发育和繁殖有着重要的关系。TC是一种可以合成多种类固醇的脂,机体内的TC含量能够有效反映动物脂质代谢和吸收的状况[14]。TG是脂肪的重要组成成分,因此TG的含量一定程度上可以反映机体脂代谢的情况。HDL-C和LDL-C的含量与动物的健康有着密切的关系,HDL-C被公认为是抗动脉粥样硬化的保护因子,两者在适宜范围内均被认为与心血管事件风险有关[15]。有关于精氨酸对断奶仔猪肝脏脂代谢的影响的相关研究并未见刊,但是在方勇军[16]的研究中发现,添加0.5%精氨酸可以显著降低肉鸭血清TG含量。Jobgen等[17]发现饲粮添加精氨酸能够显著降低大鼠血清中TG含量。刘艳妍等[18]研究表明,在饲粮中添加精氨酸可显著提高獭兔血清HDL-C含量。本试验中,断奶后第3天的仔猪肝脏中TC与TG含量极显著高于断奶当天,说明断奶应激对仔猪肝脏脂代谢有明显的抑制作用;但是相比于CON组,Arg组仔猪肝脏中TG和TC含量增加幅度有限,说明补饲精氨酸能够有效缓解断奶应激对肝脏脂代谢的影响。对于HDL-C来说,断奶当天的Arg组仔猪肝脏中含量显著高于CON组,与此同时Arg组仔猪肝脏中LDL-C含量极显著低于CON组,说明哺乳期补饲精氨酸能够有效促进断奶仔猪肝脏脂代谢。上述试验结果表明在哺乳期补饲精氨酸对缓解断奶仔猪造成的影响有一定的缓解机制,但是对其机制尚不明确。
3.3 哺乳期补饲精氨酸对断奶仔猪肝脏脂代谢相关基因表达的影响FAS能够促进脂肪酸的合成,其基因表达量越高,动物体内的脂肪沉积越高[19]。研究表明,LPL是体内脂类代谢的关键酶之一,而且其水平的变化对脂类代谢有着重要影响,与脂类代谢异常、高脂血症的发生有重要的密切关系[20]。LPL表达上升能够降低TC、TG以及LDL-C等的含量,提高HDL-C的含量[21]。本试验中,Arg组仔猪断奶当天肝脏中LPL相对表达水平显著高于CON组。孟德连[22]研究发现,添加精氨酸能够显著提高LPL在肝脏中的基因表达,同时可以显著降低过氧化物酶体增殖物激活受体(PPAR)和FAS基因在肝脏中的表达。此结果表明了精氨酸能够显著提高仔猪肝脏中LPL的基因表达水平,进而促进断奶仔猪的脂代谢。
综上,在哺乳期对仔猪补饲精氨酸后,能够有效缓解断奶应激所带来的不利影响,同时,精氨酸能够促进断奶仔猪肝脏的发育,促进肝脏脂代谢的代谢能力。这可能一方面是因为仔猪断奶应激导致大量精氨酸消耗,而本身合成的精氨酸不能满足自身需要;另一方面可能是精氨酸能够通过促进LPL基因在肝脏中的表达量,进而加强了肝脏的脂代谢功能。
4 结论哺乳期补饲精氨酸能够促进断奶仔猪的肝脏发育,提高断奶仔猪肝脏中HDL-C含量,降低肝脏中LDL-C含量,同时能够提高肝脏中LPL基因的表达水平,一定程度上增强肝脏脂代谢的功能。
| [1] |
王恬. 仔猪断奶应激及营养调控措施的应用[J]. 畜牧与兽医, 2009, 41(5): 1-4. |
| [2] |
蒋宗勇. 仔猪早期断奶营养综合症及其防治(续)[J]. 广东畜牧兽医科技, 1993(4): 26-28. |
| [3] |
郭广伦, 刘玉兰. 精氨酸对动物免疫功能影响研究进展[J]. 中国饲料, 2006(20): 27-29, 36. DOI:10.3969/j.issn.1004-3314.2006.20.009 |
| [4] |
JOBGEN W S, FRIED S K, FU W J, et al. Regulatory role for the arginine-nitric oxide pathway in metabolism of energy substrates[J]. The Journal of Nutritional Biochemistry, 2006, 17(9): 571-588. DOI:10.1016/j.jnutbio.2005.12.001 |
| [5] |
周笑犁, 刘俊锋, 吴琛, 等. 精氨酸和N-氨甲酰谷氨酸对环江香猪脂质代谢的影响[J]. 动物营养学报, 2014, 26(4): 1055-1060. DOI:10.3969/j.issn.1006-267x.2014.04.026 |
| [6] |
胡诚军, 张婷, 李华伟, 等.饲粮添加精氨酸和谷氨酸对肥育猪脂代谢相关基因表达的影响[C]//中国畜牧兽医学会动物营养学分会第十二次动物营养学术研讨会论文集.武汉: 中国畜牧兽医学会动物营养学分会, 2016: 47.
|
| [7] |
BECHMANN L P, HANNIVOORT R A, GERKEN G, et al. The interaction of hepatic lipid and glucose metabolism in liver diseases[J]. Journal of Hepatology, 2012, 56(4): 952-964. DOI:10.1016/j.jhep.2011.08.025 |
| [8] |
LI Y X, KANG H F, CHU Y, et al. Cidec differentially regulates lipid deposition and secretion through two tissue-specific isoforms[J]. Gene, 2018, 641: 265-271. DOI:10.1016/j.gene.2017.10.069 |
| [9] |
李丹丹, 刘佳佳, 吴玉泓, 等. 黄芪多糖联合二甲双胍对衰老2型糖尿病模型小鼠肝脏糖脂代谢的影响[J]. 中国中医药信息杂志, 2019, 26(2): 47-51. DOI:10.3969/j.issn.1005-5304.2019.02.011 |
| [10] |
RIVAS A L, FABRICANT J. Indications of immunodepression in chickens infected with various strains of Marek's disease virus[J]. Avian Diseases, 1988, 32(1): 1-8. DOI:10.2307/1590941 |
| [11] |
彭瑛, 蔡力创. 精氨酸和精氨酸生素对断奶仔猪生长性能、器官重及生化指标的影响[J]. 中国畜牧兽医, 2011, 38(8): 23-26. |
| [12] |
XIANG Q S, LIU Z G, WANG Y T, et al. Carnosic acid attenuates lipopolysaccharide-induced liver injury in rats via fortifying cellular antioxidant defense system[J]. Food and Chemical Toxicology, 2013, 53: 1-9. DOI:10.1016/j.fct.2012.11.001 |
| [13] |
KOTRONEN A, YKI-JÄRVINEN H. Fatty liver:a novel component of the metabolic syndrome[J]. Arteriosclerosis, Thrombosis, and Vascular Biology, 2008, 28(1): 27-38. DOI:10.1161/ATVBAHA.107.147538 |
| [14] |
赵水平. 血脂代谢基础及临床相关问题[J]. 临床荟萃, 2006(14): 989-993. DOI:10.3969/j.issn.1004-583X.2006.14.001 |
| [15] |
官宝怡, 赵福海. 高密度脂蛋白胆固醇与心血管风险研究进展[J]. 心血管病学进展, 2019, 40(3): 317-320. |
| [16] |
方勇军.精氨酸对肉鸭生长性能、免疫机能、胴体品质和血液脂质的影响[D].硕士学位论文.武汉: 武汉工业学院, 2009: 1-37. http://cdmd.cnki.com.cn/Article/CDMD-10496-2009203492.htm
|
| [17] |
JOBGEN W, MEININGER C J, JOBGEN S C, et al. Dietary L-arginine supplementation reduces white fat gain and enhances skeletal muscle and brown fat masses in diet-induced obese rats[J]. The Journal of Nutrition, 2009, 139(2): 230-237. DOI:10.3945/jn.108.096362 |
| [18] |
刘艳妍, 朱飞, 邹梅, 等. L-精氨酸对3-5月龄獭兔脂代谢的影响[J]. 饲料研究, 2017(11): 44-49. |
| [19] |
DONKIN S S, CHIU P Y, YIN D, et al. Porcine somatotropin differentially down-regulates expression of the GLUT4 and fatty acid synthase genes in pig adipose tissue[J]. The Journal of Nutrition, 1996, 126(10): 2568-2577. DOI:10.1093/jn/126.10.2568 |
| [20] |
万文涛, 郭红卫, 薛琨, 等. 脂蛋白脂酶基因多态性与代谢综合征的膳食易感性研究[J]. 营养学报, 2009, 31(4): 325-329. |
| [21] |
杨武英, 吴磊燕, 洪艳平, 等. 芦荟蒽醌对高脂血症小鼠脂代谢及LPL、MTTP基因mRNA表达的影响[J]. 中国食品学报, 2018, 18(12): 13-21. |
| [22] |
孟德连.精氨酸家族对肉鸡生长和脂肪代谢及肉品质相关基因转录表达水平的影响研究[D].博士学位论文.杨凌: 西北农林科技大学, 2010: 1-85. http://cdmd.cnki.com.cn/Article/CDMD-10712-1011070892.htm
|




