油莎草(Cyperus esculentus L.)又名油沙豆,为莎草科多年生草本植物,茎叶柔软无绒毛,须根系,根部末端膨大而成椭圆状块茎,有“地下核桃”的称号[1]。其分蘖能力较强,地上茎叶高达1.0~1.5 m,无茎秆,叶片细长,含有较高营养成分,粗蛋白质含量9.8%、粗脂肪含量8.9%、糖类化合物含量10.6%、粗纤维含量19.3%,可直接饲喂草食动物[2]。油莎草适应性强、生育期短、产量大、价值高,2018年种植面积近1.33万hm2,亩产鲜草750~1 250 kg,广泛分布于我国20多个省、市、自治区,以东北、西北、华北及长江流域为主产区[3]。大庆杜尔伯特草原位于油莎草主产区之一的东北寒区,目前该地区对油莎草地上部分的主要利用方式为直接饲喂牲畜或制作干草,容易造成牧草营养成分的损耗,而青贮能在最大程度保留牧草营养成分的前提下满足地区间牧草的季节性调度。大庆地区油莎草收获期主要集中在9月末至10月初,平均室外温度为10 ℃左右,青贮进程较为缓慢,因此添加剂选择尤为关键。副干酪乳杆菌和植物乳杆菌具有耐酸力强和耐受温度范围广的特性,故本研究选取此2种乳酸菌并设置不同温度,对油莎草发酵品质、微生物组成、化学成分及体外干物质消失率等进行研究,以筛选更适用于东北寒区油莎草青贮的添加剂,并为油莎草青贮开发与利用提供理论参考依据。
1 材料与方法 1.1 试验材料青贮原料为油莎草地上茎叶,由杜尔伯特蒙古族自治县王彦喜芦苇种植专业合作社提供,收获期为2018年9月28日,收获方式为距离地面2~3 cm刈割,其化学组成见表 1。试验选用的2种乳酸菌制剂均由日本国立畜产研究所提供,分别为副干酪乳杆菌(Lactobacillus paracasei)Master-AC和植物乳杆菌(Lactobacillus plantarum)Master-LP。使用时将菌粉与无菌水以1 : 400比例混合配制成菌液,并以菌液形式按1 : 100添加于青贮原料中,即菌剂最终添加量为0.002 5%,活菌数约为105 CFU/mL。
|
|
表 1 油莎草化学组成 Table 1 Chemical composition of Cyperus esculentus |
采用双因素试验设计,将含水量为70.50%的油莎草原料切碎至2~3 cm,分为3组,分别进行副干酪乳杆菌和植物乳杆菌添加及无添加处理,每组设10个重复。将以上处理的样品200 g装入食品级聚乙烯袋(16 cm×25 cm)中进行真空密封,各取5袋分别置于常温(20±2) ℃和低温4 ℃(置于低温库中)贮藏35 d。
1.3 样品采集及指标测定每个处理(5个重复)选取3袋开封,进行相关指标测定。
1.3.1 感官品质评定油莎草原料经35 d发酵后,开封,对颜色、气味、质地及有无霉变进行感官评定[4]。
1.3.2 发酵品质测定在聚乙烯袋中装入20 g油莎草原样,并加180 mL灭菌蒸馏水,用均质器(BagMixer-400VW,法国)拍打90 s使袋中内容物充分混合。采用便携式pH计(FG-2,Mettler Toledo,上海)测混合液pH。取袋中部分混合液进行过滤,所获得滤液经高速冷冻离心机(6 500×g,4 ℃)离心5 min,再经0.45 μm滤膜过滤,用高效液相色谱仪(HPLC,Jasco Corp.,日本)分析测定乳酸、乙酸、丙酸及丁酸含量[5]。
1.3.3 微生物数量的分析如Cai等[6]所述,通过平板计数法进行青贮饲料中乳酸菌、酵母菌、霉菌、大肠杆菌、梭菌、好氧细菌和芽孢杆菌计数。将青贮饲料样品10 g在90 mL无菌蒸馏水中匀浆90 s,并将混合样品连续稀释(10~105倍数)。用移液枪吸取各20 μL,滴加至预先准备的培养基。在厌氧培养箱中30 ℃培养48~72 h,MRS Ager培养基和Differential Reinforced Clostridial Agar培养基(青岛海博生物科技有限公司)上分别计数乳酸菌和梭菌数量。在恒温培养箱中30 ℃培养48~72 h,Potato Dextrose Ager培养基、Blue Light Broth Agar培养基和Standard Method Ager培养基(Nissui Ltd.,日本)上分别计数酵母和霉菌(通过菌落外观和细胞形态将酵母与霉菌或细菌区分开来)、大肠杆菌、好氧细菌和芽孢杆菌(在75 ℃下处理15 min)数量。适当稀释倍数下产生30~300个菌落的情况下,计数菌落。菌落数是指活微生物的数量[lg (CFU/g FM)]
1.3.4 化学成分分析取发酵后油莎草于电热恒温鼓风干燥箱(DGG-920B,上海森信实验仪器有限公司)内65 ℃下烘至恒重,并于室内回潮24 h,过1 mm筛粉碎,此样品即为风干样品,依据AOAC (1990)[7]中方法采用电热恒温鼓风干燥箱测定干物质(DM)含量,采用茂福炉(SX2-4-10,天津中环实验电炉有限公司)测定有机物(OM)含量,采用全自动凯氏定氮仪(K1100F,济南海能仪器股份有限公司)测定粗蛋白质(CP)含量,采用索氏提取器测定粗脂肪(EE)含量,依据Van Soest等[8]方法采用纤维分析仪(ANKOM A200i,美国)测定中性洗涤纤维(NDF)和酸性洗涤纤维(ADF)含量。
1.4 体外培养 1.4.1 试验动物饲养管理选取4头2周龄、体重为(32.0±1.3) kg、安装永久瘤胃瘘管的绵羊羯羊为瘤胃液供体,饲粮配制参照《肉羊饲养标准》(NY/T 816—2004),其组成(风干基础)为:羊草70.00%,玉米蛋白粉7.43%,玉米8.21%,麦麸3.00%,豆粕9.02%,磷酸氢钙0.94%,食盐0.40%,预混料1.00%。每日06:00和18:00分2次饲喂,自由饮水,正常光照。
1.4.2 培养液的配制通过真空负压装置,于晨饲后2 h分别从4头羊瘤胃内采集200 mL瘤胃液,使用4层纱布过滤,等体积混合,通入二氧化碳(CO2)保持厌氧环境。缓冲液与培养液配制参照Mcdougall[9]方法并添加还原剂L-半胱氨酸盐酸盐及指示剂刃天青钠盐。缓冲液配制:KCl 0.57 g/L、NaCl 0.47 g/L、NaHCO3 9.80 g/L、Na2HPO4·12H2O 9.30 g/L、CaCl2 0.04 g/L、MgCl2 0.06 g/L、L-半胱氨酸盐酸盐0.25 g/L、刃天青钠盐0.001 g/L,配制完成的缓冲液持续通入CO2至无色透明方可使用。培养液配制:瘤胃液与缓冲液以1 : 4的体积比均匀混合成培养液,通入CO2保持厌氧环境,放置于39 ℃水浴锅备用。
1.4.3 体外发酵参数测定每个开封袋称取0.5 g青贮样品于容量125 mL的血清瓶中(每个开封袋试验2次,试验预留3个血清瓶不加入青贮样品作为空白,其他操作如常),注入上述培养液50 mL,通入CO2排出空气并密封置于恒温培养振荡摇床(39 ℃,100 r/min),连续培养48 h,将血清瓶置于冰水中终止试验,并对产气量、pH、干物质消失率、氨态氮及乳酸、挥发性脂肪酸含量进行测定。
将头皮针插入血清瓶橡胶封口,通过与之相连的100 mL玻璃注射器记录产气量;采用便携式pH计测定pH;通过已恒重的快速定性滤纸过滤培养物,并将之移至铝盒于电热恒温鼓风干燥箱内102 ℃下烘至恒重,通过培养前后样品失重计算体外干物质消失率;参照冯宗慈等[10]的方法通过比色法测定氨态氮含量;参照贾鹏禹等[11]的方法对瘤胃液进行前处理并通过高效液相色谱仪测定乳酸及挥发性脂肪酸含量。
1.5 统计分析试验数据经Excel 2010整理,根据3×2双因素设计模型,使用SAS 9.0统计软件的GLM程序进行方差分析,建立模型:
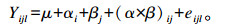
|
式中:Yijl代表青贮品质和体外干物质消失率;μ为总体平均数;αi为添加处理i(i=1,2,3)的效应;βj为温度处理j(j=常温,低温)的效应;(α×β)ij为添加处理与温度处理的互作效应;eijl为试验误差。采用Tukey法比较均值差异显著性,P < 0.05为差异显著。
2 结果 2.1 发酵35 d油莎草青贮的感官品质由表 2可知,常温组油莎草青贮颜色主要呈黄绿色至灰黄色,气味为芳香至酸香味;低温组颜色主要呈绿色至淡绿色,气味为草香至酸香味;不同温度下,均质地柔软,水分少,无霉变。与对照组相比,乳酸菌组颜色偏黄,芳香与酸香味更浓厚。
|
|
表 2 乳酸菌处理对不同温度下油莎草青贮感官品质的影响 Table 2 Effects of lactic acid bacteria treatment on sensory quality of Cyperus esculentus silage under different temperatures |
由表 3可知,在温度处理方面,低温组pH显著高于常温组(P < 0.05),其余指标组间无显著差异(P>0.05),各组均未检出丁酸。在添加处理方面,与对照组相比,常温处理下,AC组与LP组的pH显著降低(P < 0.05),低温处理下,LP组的pH显著降低(P < 0.05);不同温度处理下,各添加组间乳酸含量差异显著(P < 0.05),常温处理下AC组>LP组>对照组,低温处理下LP组>AC组>对照组;各添加组间乙酸与丙酸含量无显著差异(P>0.05)。乳酸菌添加和温度处理在pH方面表现出极显著的交互作用(P < 0.01),在乳酸含量方面表现出显著的交互作用(P < 0.05)。综合上述结果发现,常温及低温处理下最优添加组均为LP组。
|
|
表 3 乳酸菌处理对不同温度下油莎草青贮发酵品质的影响 Table 3 Effects of lactic acid bacteria treatment on fermentation quality of Cyperus esculentus silage under different temperatures |
由表 4可知,在温度处理方面,低温组的乳酸菌、酵母菌、好氧菌及芽孢杆菌数量均显著低于常温组(P < 0.05),各处理均未检出大肠杆菌、霉菌和梭菌。在添加处理方面,与对照组相比,AC组与LP组的乳酸菌、酵母菌和好氧菌数量显著降低(P < 0.05),芽孢杆菌数量显著升高(P>0.05)。乳酸菌添加和温度处理在乳酸菌、酵母菌、好氧菌及芽孢杆菌数量方面表现出极显著的交互作用(P < 0.01)。综合上述结果发现,常温及低温处理下最优添加组均为LP组。
|
|
表 4 乳酸菌处理对不同温度下油莎草青贮微生物数量的影响 Table 4 Effects of lactic acid bacteria treatment on the number of microorganisms of Cyperus esculentus silage under different temperatures |
由表 5可知,在温度处理方面,低温组粗蛋白质、粗脂肪含量及氨态氮/总氮显著低于常温组(P < 0.05),其余指标均无显著差异(P>0.05)。在添加处理方面,与对照组相比,不同温度处理下,AC组与LP组的有机物、粗蛋白质含量均显著升高(P < 0.05),氨态氮/总氮均显著降低(P < 0.05);不同温度处理下,各添加组间粗脂肪含量差异显著(P < 0.05),常温处理下LP组>AC组>对照组,低温处理下LP组>对照组>AC组;同时,常温处理下AC组与LP组的中性洗涤纤维含量均降低了1.6%,酸性洗涤纤维含量分别降低了6.0%、6.9%(P>0.05)。乳酸菌添加和温度处理在有机物含量、粗蛋白质含量、氨态氮/总氮、粗脂肪含量方面表现出极显著的交互作用(P < 0.01)。综合上述结果发现,常温及低温处理下最优添加组均为LP组。
|
|
表 5 乳酸菌处理对不同温度下油莎草青贮化学成分的影响 Table 5 Effects of lactic acid bacteria treatment on chemical composition of Cyperus esculentus silage under different temperatures |
由表 6可知,在温度处理方面,低温组的产气量、体外干物质消失率及乳酸、丙酸含量显著低于常温组(P < 0.05),pH显著高于常温组(P < 0.05),丁酸含量无显著差异(P>0.05)。在添加处理方面,常温及低温处理下,AC组和LP组产气量、体外干物质消失率、丙酸含量均显著高于对照组(P < 0.05);常温处理下,AC组和LP组乙酸含量均显著低于对照组(P < 0.05),LP组氨态氮含量显著低于对照组和LP组(P < 0.05);低温处理下,LP组乙酸含量显著高于对照组和AC组(P < 0.05),AC组氨态氮含量显著低于对照组和LP组(P>0.05)(P < 0.05);乳酸、丁酸含量无显著差异(P>0.05)。乳酸菌添加和温度处理在油莎草青贮体外发酵产气量、干物质消失率及乳酸、乙酸、丙酸含量方面表现出极显著的交互作用(P < 0.01),在pH方面表现为显著的交互作用(P < 0.05)。综合上述结果发现,常温及低温处理下最优添加组均为LP组。
|
|
表 6 乳酸菌处理对不同温度下油莎草青贮体外发酵参数的影响 Table 6 Effects of lactic acid bacteria treatment on in vitro fermentation parameters of Cyperus esculentus silage under different temperatures |
青贮过程的初始阶段,好氧性微生物和植物本身进行的呼吸作用消耗青贮窖中氧气形成厌氧环境,乳酸菌利用原料中可溶性糖产生乳酸,降低pH,抑制腐败菌的繁殖,降低青贮营养物质的损耗,从而达到长期保存和改善品质的目的[12-13]。优质青贮饲料颜色应为黄绿色或绿色,气味酸醇有芳香,质地柔软稍湿润,且无霉变发生[14]。本试验油莎草青贮颜色、气味和质地等均在正常范围,乳酸菌添加青贮的芳香与酸香气味较对照组浓厚,且无霉变现象,说明各组的青贮效果均较好。乳酸菌添加显著提高乳酸菌数量,降低酵母菌和好氧菌的数量。张相伦等[15]在全株玉米青贮中添加乳酸菌制剂发现乳酸菌数量显著提高,霉菌数量显著降低。万学瑞等[16]在玉米青贮中分别添加5株优良抑菌活性乳酸菌同样发现乳酸菌数量显著提高,霉菌、好氧菌和酵母菌数量显著降低。乳酸菌的添加可以迅速扩大青贮中乳酸菌基数,促使其成为青贮过程中的优势菌群,降低好氧性微生物的活动,抑制腐败微生物活性与增殖,改善青贮中微生物菌群[17-18]。乳酸菌处理可显著提高青贮饲料中乳酸含量。青贮饲料中乳酸含量增加,pH迅速降低,同时乳酸能分解为乙酸和丙二醇,进一步促使乙酸含量的增加,乙酸等挥发性脂肪酸是一类有效抗真菌及霉菌的酸类,更能促进青贮饲料的有氧稳定性[19]。姜伯玲等[20]在不同温度对甜高粱饲料发酵品质的研究中发现,高温及中温发酵品质优于低温。常温条件青贮效果在一定程度上优于低温状态,可能原因为常温状态处于乳酸菌的最适温度19~37 ℃,乳酸菌发酵旺盛,发酵效果优于低温状态下效果。本研究中,乳酸菌的添加增加青贮中乳酸菌数量,缩短好氧性微生物的生产繁殖,提高了乳酸的含量,降低了青贮pH,抑制了腐败菌的活性与增殖,提高了青贮饲料的有氧稳定性,改善了青贮的品质。
3.2 不同温度及乳酸菌处理对油莎草青贮营养成分的影响油莎草青贮的营养水平是评价青贮饲料品质的另一项重要参数。青贮饲料中氨态氮主要由植物酶对原料中蛋白质的降解以及微生物在有氧条件下分解利用蛋白质和氨基酸产生,总氮中氨态氮含量反映了青贮饲料蛋白质降解程度,被广泛应用于衡量青贮饲料发酵品质的好坏,其比值越大,说明被分解的氨基酸和蛋白质越多,青贮效果越差[21]。本研究中,乳酸菌的添加在一定程度上提高油莎草青贮有机物和粗蛋白质的含量,降低氨态氮的比例。Silva等[22]在苜蓿青贮中添加乳酸片球菌和戊糖片球菌发现可显著提高粗蛋白质含量,降低氨态氮比例。董志浩等[23]在桑叶青贮中添加乳酸菌发现其对粗蛋白质含量无显著影响,但显著降低氨态氮比例。粗蛋白质含量升高,可能是乳酸菌的添加导致其代谢活动增强,大量乳酸产生,pH迅速下降,有效抑制蛋白质水解酶的活性,致使蛋白质水解和脱氨基反应减缓,减少油莎草青贮粗蛋白质的降解和微生物的分解作用[24],从而降低总氮中氨态氮含量,间接提高油莎草青贮中粗蛋白质含量,改善其营养价值。
3.3 不同温度及乳酸菌处理对油莎草青贮体外发酵参数的影响干物质消失率反映底物在发酵体系中被微生物降解的程度,产气量可以反映其可发酵程度,是动物瘤胃发酵粗饲料利用率的重要指标[25]。其中底物中粗蛋白质较易发酵,而中性洗涤纤维难以被利用。研究表明,体外发酵的产气量与底物的粗蛋白质含量呈正相关,与底物中性洗涤纤维含量呈负相关[26]。本试验中乳酸菌添加的油莎草青贮粗蛋白质含量高于无添加组,所以在产气量方面也表现出优势,进而油莎草青贮的干物质降解率也得以提高。玉柱等[27]在尖叶胡枝子青贮中添加乳酸菌发现其显著提高干物质的降解率,这与本试验研究结果一致。低温处理的油莎草青贮体外发酵参数不及常温处理,可能是常温状态下油莎草的青贮饲料品质较好,营养成分得以改善,其发酵程度更容易提高。
4 结论本试验条件下,乳酸菌添加可以改善油莎草青贮品质,提高营养价值及体外干物质消失率。同时,低温环境下植物乳杆菌组发酵效果最优。
| [1] |
王瑞元, 王晓松, 相海. 一种多用途的新兴油料作物——油莎豆[J]. 中国油脂, 2019, 44(1): 1-4. |
| [2] |
阳振乐. 油莎豆的特性及其研究进展[J]. 北方园艺, 2017(17): 192-201. |
| [3] |
张学昆. 我国油莎豆产业研发进展报告[J]. 中国农村科技, 2019(4): 67-69. |
| [4] |
刘建新, 杨振海, 叶均安, 等. 青贮饲料的合理调制与质量评定标准[J]. 饲料工业, 1999, 20(4): 3-5. |
| [5] |
CAO Y M, CAI Y M, HIRAKUBO T, et al. Fermentation characteristics and microorganism composition of total mixed ration silage with local food by-products in different seasons[J]. Animal Science Journal, 2011, 82(2): 259-266. |
| [6] |
CAI Y, BENNO Y, OGAWA M, et al. Effect of applying lactic acid bacteria isolated from forage crops on fermentation characteristics and aerobic deterioration of silage[J]. Journal of Dairy Science, 1999, 82(3): 520-526. |
| [7] |
AOAC.Official methods of analysis[M]. 15th ed.Artington: Association of Official Analytical Chemists, 1990.
|
| [8] |
VAN SOEST P J, ROBERTSON J B, LEWIS B A. Methods for dietary fiber, neutral detergent fiber, and nonstarch polysaccharides in relation to animal nutrition[J]. Journal of Dairy Science, 1991, 74(10): 3583-3597. |
| [9] |
MCDOUGALL E I. Studies on ruminant saliva.1.The composition and output of sheep's saliva[J]. Biochemical Journal, 1948, 43(1): 99-109. |
| [10] |
冯宗慈, 高民. 通过比色测定瘤胃液氨氮含量方法的改进[J]. 内蒙古畜牧科学, 1993(4): 40-41. |
| [11] |
贾鹏禹, 孙蕊, 李井春, 等. 离子排斥色谱法测定瘤胃液中乳酸和挥发性脂肪酸的含量[J]. 黑龙江畜牧兽医, 2017(3): 43-46. |
| [12] |
张红梅, 段珍, 李霞, 等. 青贮饲料乳酸菌添加剂的应用现状[J]. 草业科学, 2017, 34(12): 2575-2583. |
| [13] |
KUNG L Jr, SHAVER R D, GRANT R J, et al. Silage review:interpretation of chemical, microbial, and organoleptic components of silages[J]. Journal of Dairy Science, 2018, 101(5): 4020-4033. |
| [14] |
MUCK R. Recent advances in silage microbiology[J]. Agricultural and Food Science, 2013, 22(1): 3-15. |
| [15] |
张相伦, 游伟, 赵红波, 等. 乳酸菌制剂对全株玉米青贮品质及营养成分的影响[J]. 动物营养学报, 2018, 30(1): 336-342. |
| [16] |
万学瑞, 吴建平, 雷赵民, 等. 优良抑菌活性乳酸菌对玉米青贮及有氧暴露期微生物数量和pH的影响[J]. 草业学报, 2016, 25(4): 204-211. |
| [17] |
MUCH R E, NADEAU E M G, MCALLISTER T A, et al. Silage review:recent advances and future uses of silage additives[J]. Journal of Dairy Science, 2018, 101(5): 3980-4000. |
| [18] |
牛化欣, 常杰, 胡宗福, 等. 青贮微生物的发掘及其应用的研究进展[J]. 动物营养学报, 2018, 30(11): 4279-4285. |
| [19] |
贾婷婷, 吴哲, 玉柱. 不同类型乳酸菌添加剂对燕麦青贮品质和有氧稳定性的影响[J]. 草业科学, 2018, 35(5): 1266-1272. |
| [20] |
姜伯玲, 王曙阳, 陈积红, 等. 发酵温度对复合微生物菌剂青贮饲料品质的影响[J]. 中国草食动物科学, 2016, 36(2): 29-32. |
| [21] |
HASHEMZADEH-CIGARI F, KHORVASH M, GHORBANI G R, et al. Interactive effects of molasses by homofermentative and heterofermentative inoculants on fermentation quality, nitrogen fractionation, nutritive value and aerobic stability of wilted alfalfa (Medicago sativa L.) silage[J]. Journal of Animal Physiology and Animal Nutrition, 2014, 98(2): 290-299. |
| [22] |
SILVA V P, PEREIRA O G, LEANDRO E S, et al. Effects of lactic acid bacteria with bacteriocinogenic potential on the fermentation profile and chemical composition of alfalfa silage in tropical conditions[J]. Journal of Dairy Science, 2016, 99(3): 1895-1902. |
| [23] |
董志浩, 原现军, 闻爱友, 等. 添加乳酸菌和发酵底物对桑叶青贮发酵品质的影响[J]. 草业学报, 2016, 25(6): 167-174. |
| [24] |
桂荣, 刘晗璐. 披碱草和老芒麦附着微生物检测及添加乳酸菌对其青贮发酵品质的影响[J]. 中国饲料, 2007(13): 39-42. |
| [25] |
于满满, 姜雨轩, 张美美, 等. 利用体外产气法评定不同比例氨化秸秆替代苜蓿的组合效应[J]. 中国畜牧兽医, 2017, 44(12): 3497-3504. |
| [26] |
NSAHLAI I V, SIAW D, OSUJI P O. The relationships between gas production and chemical composition of 23 browses of the genus Sesbania[J]. Journal of the science of food and agriculture, 1994, 65(1): 13-20. |
| [27] |
玉柱, 魏馨, 于艳冬, 等. 添加剂对尖叶胡枝子青贮发酵品质及体外消化率的影响[J]. 草业学报, 2009, 18(5): 73-79. |




