2. 辽宁省现代农业生产基地建设工程中心, 辽阳 111000
2. Liaoning Province Modern Agricultural Production Base and Construction Engineering Center, Liaoyang 111000, China
山羊绒源于次级毛囊,次级毛囊是绒山羊皮肤组织的重要器官[1],次级毛囊的生长发育对羊绒的产量和质量有重要影响,因此体外培养毛囊对进一步研究营养因素对毛囊生长发育的作用提供了良好的研究模型[2]。羊毛中硫的含量为2.7%~5.4%,羊毛越细,含硫就越高,硫是羊生长的必需元素,也是角蛋白前体物合成所必需的原料[3]。蛋氨酸(methionine,Met)和生物素(biotin)都是含硫营养素,因此Met和生物素对山羊绒的生长十分重要。Souri等[4]体外培养绒山羊次级毛囊时,在培养基中添加了胱氨酸和Met,研究结果发现Met是次级毛囊生长毛发时所必需的。Tahmasbi等[5]在体外培养绵羊毛囊时,培养基中添加不同水平的生物素,发现生物素在控制毛囊生长和活力中起重要作用。本试验旨在通过体外添加不同水平Met、生物素,探讨其对毛囊形态、毛囊生长、DNA合成影响的剂量效应,为进一步研究Met、生物素对绒山羊绒毛生长及营养调控作用提供科学依据。
1 材料与方法 1.1 试验材料试验皮肤样品采自1.5周岁左右健康雄性辽宁绒山羊,在9月份绒毛生长期于羊只肩胛骨后缘处采集1 cm2左右样品。采集的样品尽量除去绒毛和皮下组织,放入75%酒精中消毒30~40 s,取出后加入含双抗(青、链霉素)的生理盐水中反复冲洗3遍,置于含双抗的生理盐水中带回无菌室。
1.2 试验试剂Met、生物素(北京某生物技术有限公司);Williams E培养液、牛胰岛素(Sigma,美国);亚硒酸钠(北京鼎国昌盛生物技术有限公司);氢化可的松、L-谷氨酰胺、Hepes、双抗(青霉素-链霉素)(上海生物工程股份有限公司);微量DNA提取试剂盒(北京全氏金生物公司)。
1.3 培养液组成基础培养液组成:Williams E培养液、L-谷氨酰胺2 mmol/L、Hepes 20 mmol/L、牛胰岛素10 μg/mL、亚硒酸钠10 ng/mL、氢化可的松10 μg/mL、转铁蛋白10 μg/mL、青霉素100 μg/mL、链霉素100 μg/mL。
1.4 试验设计采用显微解剖分离法[6]分离次级毛囊,挑选毛乳头圆润、光滑、饱满,真皮组织鞘完好并与外皮根鞘无分离的完整次级毛囊用于培养试验。试验共分为2部分,均采用单因素试验设计。试验1:将分离出来的完整毛囊随机分为5组,每组4个重复,每个重复12根毛囊,共240根次级毛囊,对照组为Williams E基础培养液,试验组在基础培养液中依次添加7.5、15.0、30.0和60.0 mg/L Met。试验2:将分离出来的完整毛囊随机分为4组,每组3个重复,每个重复10根毛囊,共120根次级毛囊,对照组为Williams E基础培养液,试验组在基础培养液中依次添加0.25、0.50和1.00 mg/L生物素。在每组的24孔细胞培养板中每个孔加入相应的培养液1 mL,然后小心地移入每1根新鲜剥离的次级毛囊,最后在二氧化碳(CO2)培养箱内培养7 d。培养期间每隔24 h在倒置显微镜下观察毛囊形态结构变化,用目镜测微尺测量毛囊生长长度,试验结束后提取各组毛囊DNA。
1.5 测定指标和方法毛囊生长长度的测定:每间隔24 h在装有目镜测微尺的倒置显微镜下测量毛囊底部至毛发顶部长度,并记录数据。

|
毛囊DNA含量的测定:试验结束后提取各组毛囊DNA含量。将各组培养结束的毛囊分别置于无菌的1.5 mL离心管中,55 ℃孵育直至完全裂解大约需要1 h,为得到更多的DNA,重复洗脱2次,所得样品用Nanodrop 2000进行检测,按照微量DNA提取试剂盒说明书进行。
1.6 数据统计分析采用SPSS 17.0软件中的单因素方差分析(one-way ANOVA)对数据进行分析处理,试验数据用平均值、合并标准误(SEM)和P值表示。当数据差异显著时,采用Duncan氏法进行多重比较,并进行线性和二次项趋势分析,对差异显著的数据进行回归分析。P < 0.01表示差异极显著,P < 0.05表示差异显著。
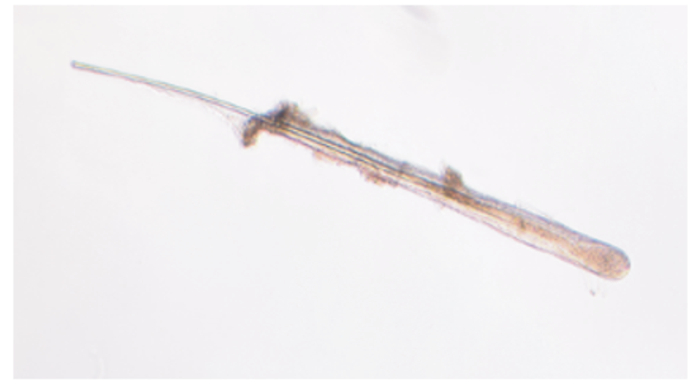
2 结果与分析 2.1 添加Met和生物素对次级毛囊形态的影响挑选新鲜分离的完整无损毛囊即毛球部位饱满光滑并呈现圆形,毛乳头清晰、真皮组织鞘等组织完整并与外皮根鞘无分离,毛干与内外根鞘之间界限清楚。图 1所示为新鲜完整的毛囊,可用于体外培养。
|
图 1 分离完整的次级毛囊 Fig. 1 Completely separated secondary follicles |
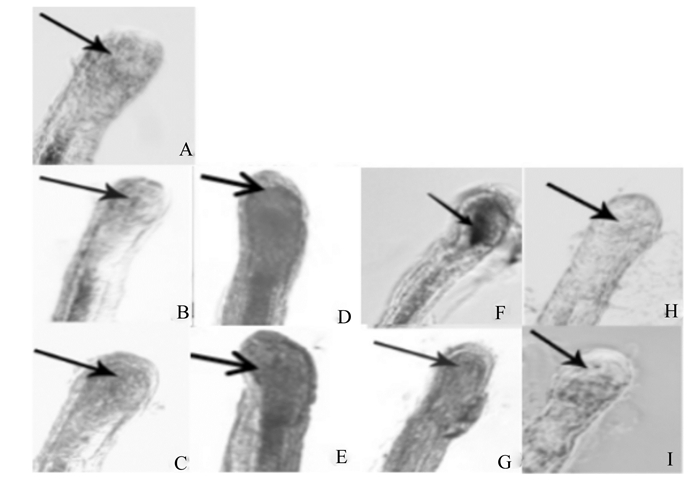
在Met、生物素不同添加水平的培养条件下,毛囊的生长长度、生长速度以及毛球部的形态情况均有所不同,体外培养次级毛囊形态变化见图 2。对照组的次级毛囊体外培养至第4天,毛球形态逐渐变的不规则,并且毛母质与毛乳头二者之间的界限开始变得模糊,毛囊生长速度从这时候开始逐渐变缓慢(图 2-B)。体外培养次级毛囊第7天时,次级毛囊毛球部位结构变得松散且逐渐模糊,毛母质开始萎缩并与毛乳头距离变大(图 2-C)。30.0 mg/L Met组毛囊形态变化第4天(图 2-D)毛囊毛乳头细胞分裂增殖使毛干及内外根鞘延长,毛乳头与毛母质界限逐渐模糊,外层真皮鞘上皮细胞结构松散,但不如对照组明显,结缔组织鞘无明显变化。培养第7天(图 2-E),毛乳头与毛母质界限模糊,但仍能看清毛乳头轮廓,毛干与内皮根鞘之间和毛球部结构层次的界限模糊。0.25 mg/L生物素组次级毛囊体外培养至第4天时(图 2-F),毛囊形态发生明显变化,内外根鞘界限不清晰,在培养第7天时毛囊整体结构变得更加模糊松散(图 2-G),但不如对照组明显。培养到第7天时(图 2-I),0.5 mg/L生物素促进了毛乳头和毛母质细胞分裂增殖。
|
A:新鲜分离毛囊freshly isolated secondary follicles;B:对照组第4天control group on day 4;C:对照组第7天control group on day 7;D:30.0 mg/L Met组第4天30.0 mg/L Met group on day 4;E:30.0 mg/L Met组第7天30.0 mg/L Met group on day 7;F:0.25 mg/L生物素组第4天0.25 mg/L biotin group on day 4;G:0.25 mg/L生物素组第7天0.25 mg/L biotin group on day 7;H:0.50 mg/L生物素组第4天0.50 mg/L biotin group on day 4;I:0.50 mg/L生物素组第7天0.50 mg/L biotin group on day 7。 图 2 体外培养绒山羊次级毛囊第1、4和7天形态观察结果 Fig. 2 Morphological results of secondary follicles of cashmere goats cultured in vitro at days 1, 4 and 7 (200×) |
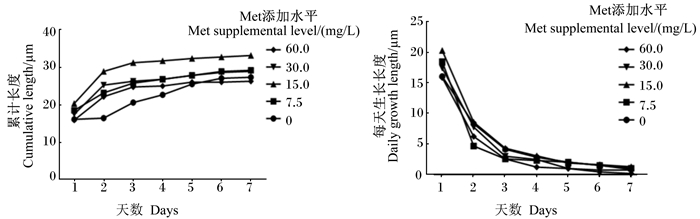
由图 3和表 1可知,添加Met对绒山羊次级毛囊累计长度和生长速度有极显著影响(P < 0.01)。15.0 mg/L Met促次级毛囊体外生长效果最好,次级毛囊累计长度最大、生长速度最快,分别达到了31.25 μm和为5.3 μm/d;与对照组相比,其累计长度提高了15.40%,生长速度提高了16.81%。
|
图 3 不同Met添加水平次级毛囊累计长度和每天生长长度折线图 Fig. 3 Line graph of cumulative length and daily growth length of secondary follicles at different Met supplemental levels |
|
|
表 1 Met对次级毛囊体外生长和DNA合成的影响 Table 1 Effects of methionine on growth and DNA synthesis of secondary follicles in vitro |
由表 1可知,添加Met对体外培养的绒山羊次级毛囊累计长度和生长速度有二次曲线关系(P < 0.05)。进一步进行回归分析,得到累计长度的回归方程为y=-0.004 3x2+0.174 4x+27.826(R2=0.698 8),根据拟合曲线得出Met最适添加水平为20.27 mg/L。生长速度的回归方程为y=-0.000 2x2+0.007 5x+1.157 7(R2=0.625 0),根据拟合曲线得出Met最适添加水平为18.75 mg/L。因此,当Met添加水平为20.27和18.75 mg/L时,辽宁绒山羊次级毛囊累计长度和生长速度较好。
由表 1可知,添加Met对体外培养的绒山羊次级毛囊的DNA含量呈显著的二次曲线关系(P < 0.05)。其回归方程为y=-0.024 7x2+1.569 2x+45.232(R2=0.690 8),根据拟合曲线得出Met最适添加水平为31.77 mg/L。随着Met添加水平的提高,次级毛囊DNA含量呈低-高-低的趋势,其中15.0 mg/L Met促次级毛囊DNA合成效果最好,与对照组相比, 平均每根次级毛囊DNA含量提高了76.44%。
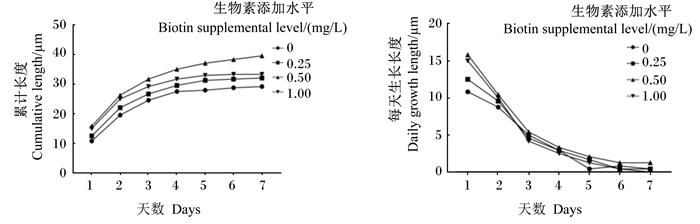
2.3 添加生物素对体外培养次级毛囊生长长度和DNA含量的影响由图 4和表 2可知,培养液中添加生物素对绒山羊次级毛囊累计长度和生长速度有显著影响(P < 0.05)。0.50 mg/L生物素促次级毛囊体外生长效果最好,与对照组相比,次级毛囊累计长度最大、生长速度最快,分别达到了39.58 μm和5.48 μm/d。
|
图 4 不同生物素添加水平对次级毛囊累计长度和每天生长长度折线图 Fig. 4 Line chart of cumulative length and daily growth length of secondary follicles at different biotin supplemental levels |
|
|
表 2 生物素对次级毛囊体外生长和DNA合成的影响 Table 2 Effects of biotin on growth and DNA synthesis of secondary follicles in vitro |
由表 2得知,添加不同水平生物素对次级毛囊累计长度和生长速度有线性(P < 0.05)和二次曲线关系(P < 0.05)。进一步进行回归分析,得到累计长度的回归方程为y=-18.333x2+23.75x+23.423(R2=0.858 2),根据拟合曲线得出生物素最适添加水平为0.65 mg/L。生长速度的回归方程为y=-3.852 8x2+4.629 9x+4.030 3(R2=0.807 4),根据拟合曲线得出生物素最适添加水平为0.60 mg/L。因此,当生物素添加水平为0.65和0.60 mg/L时,辽宁绒山羊次级毛囊累计长度和生长速度最好。
由表 2可知,生物素对体外培养的绒山羊次级毛囊对DNA含量呈显著的线性相关(P < 0.05),其回归方程为y=8.716 6x+60.454(R2=0.203 1)。随着生物素添加水平的提高,次级毛囊DNA含量呈由低-高-低的趋势,其中0.5 mg/L生物素促次级毛囊DNA合成效果最好,与对照组相比,平均每根次级毛囊DNA含量提高了33.40%。
3 讨论 3.1 挑选健康完好无损的处于生长期的毛囊是体外毛囊培养的首要问题李蘅等[7]表示体外培养毛囊生长发育机理和周期性变化受多种因素调控,影响着毛发的生长,因此建立健康的体外毛囊培养模型就显得尤为重要,所以在进行体外培养毛囊时进行的第1步要剥离并选择出健康完好的次级毛囊。毛乳头圆润、光滑、饱满、清晰可见以及毛干与内外根鞘之间的界限清晰是建立理想的体外培养次级毛囊的模型的关键[8],这也可以为进一步研究羊毛生长规律奠定基础。而且毛囊的分离方法、毛囊的生长时期和取样的部位以及取样前的处理都对毛囊的分离效果有影响,但最主要的是毛囊的分离方法[9]。汪长寿等[10]指出常用的毛囊分离方法有显微解剖分离法、剪刀法、酶消化法,根据不同物种、不同毛囊生长的皮质和分离毛囊工具的不同,不同研究者采用不同的分离方法。而本试验采用了研究者较常用的Philpott显微解剖法来分离辽宁绒山羊的次级毛囊,此种方法分离速度快,可以保留完整的毛囊,但机械法分离毛囊不仅对试验人员操作的熟练程度有较高要求,还过于耗费体力[11]。因此在操作过程中要求必须轻柔,以避免毛囊发生机械损伤导致其内部结构中断进而影响细胞之间或表真皮间的相互作用,这是成功培养游离毛囊的关键。刘海静等[6]研究表明,在处理小块羊皮时尽量用眼科剪去除浮毛和皮下脂肪并随时用生理盐水冲洗剪掉的组织,因为取样的羊皮毛长度越短,皮下脂肪越少,毛囊越容易分离。采样时尽量用刀片刮干净皮肤,但注意不要用力过度破坏到皮肤。
3.2 Met、生物素对体外培养次级毛囊形态的影响范卫新等[12]提出大部分哺乳动物毛发的生长过程非常复杂,而且其毛囊的生长状态和速度会受到动物的年龄、性别、自身营养以及周围环境等很多因素的影响。因此采用体外培养辽宁绒山羊次级毛囊的模型可在较大程度上有效控制一些外界因素的影响,有利于对毛囊生长调控机制的研究。Galbraith[13]通过测量体外分离的生长期次级毛囊的研究发现,Met可以在没有半胱氨酸和胱氨酸的支持下促进羊绒纤维的增长,表明Met对于次级毛囊产生纤维至关重要。南韦肖等[14]研究发现,通过在体外培养水貂毛囊的培养基中添加8 μg/mL Met可以明显提高毛囊生长长度。
对照组的毛囊较生物素组的毛囊活性差,原因可能是由于生物素缺乏导致这些毛囊中异常代谢物浓度的增加,毛囊的鳞茎细胞可能比皮肤中的其他类型的细胞(如成纤维细胞)对毒性更敏感[15]。Liu等[16]认为毛囊存活率差可能是由于异常代谢产物如有机酸(3-甲基巴豆酰基甘氨酸和3-羟基异戊酸)的积累引起的,这些疾病与亮氨酸代谢必不可少的生物素依赖性酶3-甲基巴豆酰辅酶A羧化酶缺乏有关,该物质缺乏可导致亮氨酸降解途径产生异常的有机酸代谢物,这可能引起毛囊毒性并降低毛囊生存力。Tahmasbi等[17]研究发现,在培养基中添加生物素对毛囊活性有显著影响,且随着培养基中生物素添加水平的增加,毛囊活性增强,生物素添加水平为0.5 mg/L时毛囊活性最好。
3.3 Met对体外培养次级毛囊生长长度和DNA合成的影响培养基Met添加水平的增加,会使毛囊生长长度及生长速度增加,是因为在培养基中添加Met,可以在毛囊组织中合成胱氨酸及聚胺,从而促进细胞的分裂并为相应的蛋白质的合成奠定基础,较对照组能更好地促进一些相关蛋白质的合成[18]。众多学者做了大量关于将Met添加到毛皮动物饲粮中从而观察毛囊品质的试验,堵光莹等[19]研究发现,在獭兔饲粮中添加Met有助于次级毛囊的发育以及毛囊密度的提高;袁绍有等[20]在皖西白鹅活拔鹅毛后的精料补充料中添加适量的Met,研究发现Met有利于鹅新生羽毛、羽绒的生长;谢实勇等[21]研究发现,在内蒙古绒山羊的饲粮中添加包被Met可以提高羊绒的生长速度、产绒量及羊绒细度;刘逍等[22]在吉林白鹅的饲粮中添加0.5%的Met,试验结果表明吉林白鹅绒的千朵重显著增加;高晔等[23]研究发现,在陕北白绒山羊妊娠期母羊和羔羊中添加2%过瘤胃Met可促进羊绒生长。本试验在离体条件下培养次级毛囊,通过每天测量毛囊长度来更加直观地观察出Met对次级毛囊生长的影响,结果表明随着培养基中Met添加水平的增加,毛囊的发育存在显著差异,并且累计长度和生长速度与Met添加水平有二次曲线关系,拟合曲线后得到Met的最适添加水平分别为18.75和20.27 mg/L。
Galbraith[24]和Souri等[4]指出Met有助于体外培养次级毛囊的毛纤维生长发育,并且在体外培养次级毛囊过程中能够提高其DNA合成量,效果较好的组Met添加水平为100 μmol/L。本试验结果表明,通过在培养基中添加不同水平Met能够影响次级毛囊DNA含量,其中15 mg/L Met组次级毛囊DNA含量最多,次级毛囊DNA含量达到了平均每根73.43 ng。
3.4 生物素对体外培养次级毛囊生长长度和DNA合成的影响毛囊是哺乳动物独特的皮肤附属物,具有再生和自我更新的能力,是周期生长的[25]。在许多动物试验中已经确立了生物素的缺乏会导致蹄、皮肤和脱发的皮肤病学损伤,然而这些机制仍有待阐明。Tahmasbi等[26]进行了一项体外培养试验,研究生物素在控制羊毛囊生长和活力中的作用。把分离出的次级毛囊保存在Williams E培养液中,补充0、0.25和0.50 mg/L生物素。研究发现,随着培养基中生物素添加水平的提高,毛囊生长速度增加。本试验在基础培养液中添加不同水平的生物素影响次级毛囊的累计长度以及生长速率,其中0.50 mg/L生物素组毛囊生长速度最快、累计长度最长。
Moskowitz等[27]研究表明,生物素缺乏可显著降低在无血清培养基中培养的肉瘤病毒转化细胞中DNA合成的速率。DNA含量随着培养液中生物素添加水平的增加而增加,48 h(每个毛囊47 ng)在对照组中培养的毛囊DNA含量比补充0.50 mg/L生物素(每个毛囊72 ng)培养基中培养的低35%,但差异不显著。Tahmasbi等[26]试验中平均每根绵羊次级毛囊的DNA含量为65 ng;Souri[4]试验结果中表明,马海毛的每根毛囊DNA含量为65~76 ng;Philpott等[28]研究发现,大鼠每根毛囊的DNA含量为75~100 ng,与本试验结果相似。本试验在培养基中添加不同水平生物素能够影响次级毛囊DNA含量,其中0.50 mg/L生物素组毛囊生长速度最快、累计长度最长、DNA含量最多,每根毛囊可达到75.77 ng,但差异不显著。
4 结论① Met对绒山羊次级毛囊体外生长和DNA含量有影响。其中15.0 mg/L Met促次级毛囊体外生长效果最好,其累计长度和生长速度最大,同时毛球部形态保持相对较好,且DNA含量最多。
② 生物素能够影响绒山羊次级毛囊体外生长和DNA含量。0.50 mg/L生物素促次级毛囊体外生长效果最好,其累计长度和生长速度最大,且DNA含量最多。
| [1] |
史雷, 屈雷, 刘锦旺, 等. 陕北白绒山羊皮肤毛囊形态结构及其特征参数与产绒性状的相关性分析[J]. 中国畜牧兽医, 2018, 45(10): 2814-2822. |
| [2] |
张婧婧, 王德光, 周小兵, 等. VEGF对体外培养绒山羊次级毛囊外根鞘细胞的影响[J]. 畜牧兽医学报, 2018, 49(6): 1124-1133. |
| [3] |
王志有, 魏著莪, 周韶, 等. 青海藏羊、细毛羊羊毛不同区段含硫量的测定[J]. 青海大学学报(自然科学版), 2004, 22(1): 11-12, 24. |
| [4] |
SOURI M, GALBRAITH H, SCAIFE J R.Conversion of methionine to cysteine by transulphuration in isolated angagen secondary hair follicles of the Angoragoat[C]//Proceedings of the British Society of Animal Science, [s.l.]: [s.n.], 1998: 139.
|
| [5] |
TAHMASBI A M, GALBRAITH H, SCAIFE J R. Investigation of the role of biotin in the regulation of wool growth in sheep hair follicles cultured in vitro[J]. Research Journal of Animal Sciences, 2007, 1(1): 9-19. |
| [6] |
刘海静, 刘海英, 杨桂芹, 等. LiCl对绒山羊毛囊生长和β-catenin表达的影响[J]. 沈阳农业大学学报, 2016, 47(6): 722-727. |
| [7] |
李蘅, 李金泉, 曹贵方, 等. 不同条件对绒山羊体外培养初级毛囊生长的影响[J]. 安徽农业科学, 2008, 36(5): 15965-15967. |
| [8] |
ANTONINI M. Hair follicle characteristics and fibre production in South American camelids[J]. Animal, 2010, 4(9): 1460-1471. DOI:10.1017/S1751731110001035 |
| [9] |
MAGERL M, KAUSER S, PAUS R, et al. Simple and rapid method to isolate and culture follicular papillae from human scalp hair follicles[J]. Experimental Dermatology, 2002, 11(4): 381-385. |
| [10] |
汪长寿, 曹贵方. 不同的体外培养条件对绵羊毛囊生长的影响[J]. 安徽农业科学, 2008, 36(10): 4070-4071, 4100. |
| [11] |
张铁佳, 王岩, 王琳, 等. 褪黑激素对内蒙古绒山羊初级毛囊体外培养影响的研究[J]. 中国农业大学学报, 2016, 21(11): 64-69. |
| [12] |
范卫新, 朱文元. 小鼠触须毛囊体外培养的研究[J]. 中华皮肤科杂志, 1999, 32(1): 28-30. |
| [13] |
GALBRAITH H. Protein and sulphur amino acid nutrition of hair fibre-producing Angora and Cashmere goats[J]. Livestock Production Science, 2000, 64(1): 81-93. DOI:10.1016/S0301-6226(00)00177-9 |
| [14] |
南韦肖, 张海华, 司华哲, 等. 不同培养条件对水貂毛囊体外培养的影响[J]. 畜牧与兽医, 2016, 48(5): 97-100. |
| [15] |
FRATER R. Inhibition of growth of hair follicles by a lectin-like substance from rat skin[J]. Australian Journal of Biological Sciences, 1983, 36(4): 411-418. DOI:10.1071/BI9830411 |
| [16] |
LIU Y Y, SHIGEMATSU Y, NAKAI A, et al. The effects of biotin deficiency on organic acid metabolism:increase in propionyl coenzyme A-related organic acids in biotin-deficient rats[J]. Metabolism, 1993, 42(11): 1392-1397. DOI:10.1016/0026-0495(93)90188-T |
| [17] |
TAHMASBI A M, GALBRAITH H, SCAIFE J R, et al.The detection of apoptosis and BCL2 in isolated secondary hair follicles (growing and quiescent) cultured in vitro in the presence or absence of biotin[C]//Proceedings of the British Society of Animal Science, [s.l.]: [s.n.], 1999: 159.
|
| [18] |
吴振宇.生长獭兔毛囊发育规律及蛋氨酸调控机制研究[D].博士学位论文.泰安: 山东农业大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10434-1017075046.htm
|
| [19] |
堵光莹, 畅丽芳, 迟玉杨, 等. 不同蛋氨酸水平对獭兔各项指标的影响[J]. 饲料研究, 2014(5): 1-3, 6. |
| [20] |
袁绍有, 左瑞华. 日粮蛋氨酸水平对皖西白鹅拔毛后产毛性能的影响[J]. 中国草食动物, 2007, 27(4): 36-37. |
| [21] |
谢实勇, 贾志海, 朱晓萍, 等. 包被蛋氨酸对内蒙古白绒山羊氮代谢及产绒性能的影响[J]. 中国农业大学学报, 2003, 8(3): 73-76. |
| [22] |
刘逍, 滕战伟, 娄玉杰. 蛋氨酸对70日龄吉林白鹅产绒性能及IGF-Ⅰ基因mRNA相对表达量的影响[J]. 中国畜牧杂志, 2017, 53(1): 75-78. |
| [23] |
高晔, 闫海龙, 闫玉清, 等. 妊娠期绒山羊母羊饲粮添加过瘤胃蛋氨酸对羔羊绒毛品质的影响[J]. 家畜生态学报, 2019, 40(8): 37-41. |
| [24] |
GALBRAITH H. Fundamental hair follicle biology and fine fibre production in animals[J]. Animal, 2010, 4(9): 1490-1509. DOI:10.1017/S175173111000025X |
| [25] |
王洪阳.初步探究雄激素对和田羊毛囊及角蛋白的影响[D].硕士学位论文.阿拉尔: 塔里木大学, 2019. http://cdmd.cnki.com.cn/Article/CDMD-10757-1019150142.htm
|
| [26] |
TAHMASBI M, GALBRAITH H, SCAIFE J R. The effect of biotin deficiency in the pre-ruminant and immediately post-ruminant Angora and cashmere kids[J]. Journal of Animal and Veterinary Advances, 2007, 6(4): 539-548. |
| [27] |
MOSKOWITZ M, CHENG D K S. Growth and G1 arrest of sarcoma virus transformed cells in serum free media[J]. Journal of Cellular Physiology, 1979, 100(3): 589-601. DOI:10.1002/jcp.1041000320 |
| [28] |
PHILPOTT M P, GREEN M R, KEALEY T. Human hair growth in vitro[J]. Journal of Cell Science, 1990, 97(3): 463-471. |




