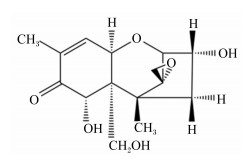
全世界谷物粮食受霉菌毒素污染非常严重,霉菌毒素不但引起动物肝脏和肾脏病变、肠毒综合征、繁殖障碍等疾病,给畜牧业造成巨大经济损失,而且毒素及其代谢产物能在肉、蛋、奶中残留,严重威胁食品安全和人的健康。霉菌毒素是霉菌在生长过程中产生的一类有毒的次生代谢产物[1]。其中,污染最严重的是镰刀菌毒素,包括脱氧雪腐镰刀菌烯醇(deoxynivalenol,DON)、T-2毒素和玉米赤霉烯酮(zearalenone,ZEN)等[2]。DON因其在谷类作物最常见,给食品行业及畜牧业造成巨大经济损失而成为研究的重点。DON是由镰刀菌属(Fusarium spp.)霉菌包括禾谷镰刀菌(F. graminearum)、黄色镰刀菌(F. culmorum)等产生的有毒次级代谢产物[3],因其能引发母猪呕吐和拒食,故也将其命名为呕吐毒素,化学名为3α, 7α, 15-三羟基-12,13-环氧单端孢霉-9-烯-8-酮,其化学结构式如图 1所示。
|
图 1 DON的化学结构式 Fig. 1 Chemical structural formula of deoxynivalenol |
DON对饲料的污染率和污染水平均居镰刀菌毒素之首,对畜禽生产及人类健康造成严重威胁[4],世界各国都对其污染情况进行过调研。2018年中国饲料原料及饲料霉菌毒素检测报告显示霉菌毒素污染普遍存在,其中DON总检出率为99.39%,小麦及麸皮是DON污染最为严重的原料,超标率高达24.55%,平均含量高达1 708.69 μg/kg[5]。Mishra等[6]总结世界范围内DON在食品中的污染情况,结果表明DON在小麦、玉米或燕麦等谷物和以谷物为基础的产品以及婴儿食品中污染率很高。各国针对DON的污染制定了限量标准。我国《饲料卫生标准》(GB 13078—2017)规定犊牛、羔羊泌乳期精料补充料及猪配合饲料中DON含量不可超过1 mg/kg,植物性饲料原料中DON限量值为5 mg/kg[7]。我国《食品安全国家标准》(GB 2761—2017)规定人类玉米(粉)、大麦、小麦(粉)和麦片中DON的限量值为1 mg/kg[8]。美国食品和药物管理局(FDA)规定食品中DON的安全标准为1 mg/kg[9],而欧盟限定谷物及其副产品中的DON限量标准为0.75 mg/kg[10]。
饲料或食品中的DON可引起人和动物细胞毒性[11-12]、免疫毒性[13-14]、肠道毒性[15-16]、神经毒性[17]和生殖遗传毒性[18]等一系列急性和慢性中毒症。其中,动物DON慢性中毒症状主要表现为厌食、体增重减少、营养吸收不良、神经内分泌及免疫系统改变等[19];敏感动物急性DON中毒后的症状主要包括腹痛、腹泻、唾液增多和呕吐等[20]。此外,DON在肉、蛋、奶中的残留还会引发一系列的动物源性食品安全问题。因此,如何有效控制和解决DON对粮食和饲料的污染,降低其对动物的潜在危害,对畜禽健康养殖和食品安全有非常重要的意义。
尽管已将危害分析的临界控制点(hazard analysis critical control point,HACCP)风险防控体系用于谷物从种植到收获的各个环节,但谷物还是不可避免受到霉菌毒素污染且存在含量超标现象。人们习惯上将不符合食用标准、毒素超标的谷物用作饲料原料。因此,霉菌毒素对饲料安全的影响远高于其对食品安全的直接影响。为了降低DON对人和动物健康造成的危害,研究人员开发了各种物理和化学去毒方法,包括吸附剂吸附[21]、辐照处理[22-23]、臭氧熏蒸[24-25]和碱处理[26]等方法。由于这些方法存在二次污染、吸附效率低、适口性差、营养流失等问题,并不利于动物实际生产中霉菌毒素脱毒的应用。生物转化法因其具有特异性强、催化效率高、不产生二次污染等特点成为国内外霉菌毒素污染削减研究的重点。生物转化是指霉菌毒素被微生物或生物酶(来源于微生物、植物或动物体)催化后化学结构发生改变的代谢过程,生物转化可通过破坏霉菌毒素的毒性基团使其毒性降低(生物解毒),也可使霉菌毒素的结构性质发生变化从而使其毒性增加(生物活化)。生物转化后的产物毒性增加或降低需进行细胞或动物体的毒性评价来验证。试验证实DON经生物转化后,绝大多数产物毒性降低或消除,因此,生物转化法是一种非常有前途的饲料和食品中DON脱毒的方法[27]。早先关于DON生物转化的研究多集中于筛选功能性微生物,随着科学技术的进步,近5年来能够催化DON的生物酶被分离鉴定出来,且其基因克隆、外源表达及催化机制方面的工作也有了新的进展。本文将从DON生物转化的作用类型,对DON发挥生物转化的功能性微生物、生物酶,DON转化产物的毒性及生物转化在动物生产中的应用等方面进行综述,以期为饲料和食品中DON的生物脱毒提供理论和实践参考。
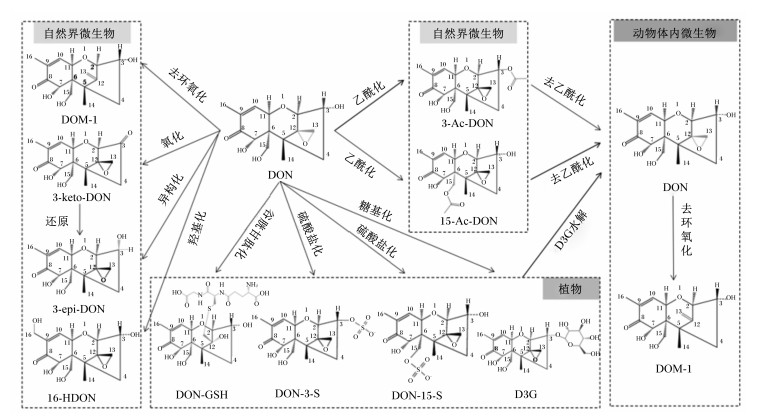
1 DON生物转化作用类型研究表明,C12、C13位的环氧结构[28-29]和C3-OH基团[30-32]是DON的主要毒性基团,因此,这2个基团是DON生物转化中主要的研究靶点。目前报道的对DON发生生物转化的生物材料主要有来源于自然界和动物体内的微生物以及微生物和植物产生的生物酶,其转化DON的作用方式可归为8类(图 2、表 1和表 2),包括:1)C12, 13位上的环氧基去环氧化作用,产物为去环氧DON(deepoxy-deoxynivalenol,DOM-1);2)C3位上的羟基氧化作用,产物为3-酮基-DON(3-keto-deoxynivalenol,3-keto-DON);3)C3位上的羟基差向异构化作用,产物为3-异构化-DON(3-epi-deoxynivalenol,3-epi-DON);4)C16位上甲基羟基化作用,产物为16-羟基-DON(16-hydroxy-deoxynivalenol,16-HDON);5)C3位上羟基糖基化作用,产物为DON-3-O-葡萄糖苷(DON-3-O-glucoside,D3G);6)乙酰化作用,C3位上羟基乙酰化产物为3-乙酰-DON(3-acetyl-deoxynivalenol,3-Ac-DON),C15位上羟基乙酰化产物为15-乙酰-DON(15-acetyl-deoxynivalenol,15-Ac-DON);7)谷胱甘肽化作用,C12, 13位上的环氧基谷胱甘肽化作用产物为DON-谷胱甘肽(deoxynivalenol-glutathione,DON-GSH);8)硫酸盐化作用,C3位上羟基硫酸盐化产物为DON-3-硫酸盐(deoxynivalenol-3-sulfate,DON-3-S),C15位上羟基硫酸盐化产物为DON-15-硫酸盐(deoxynivalenol-15-sulfate,DON-15-S)。
|
DOM-1:去环氧DON deepoxy-deoxynivalenol;3-keto-DON:3-酮基-DON 3-keto-deoxynivalenol;3-epi-DON:3-异构化-DON 3-epi-deoxynivalenol;16-HDON:16-羟基-DON 16-hydroxy-deoxynivalenol;D3G:DON-3-O-葡萄糖苷DON-3-O-glucoside;3-Ac-DON:3-乙酰-DON 3-acetyl-deoxynivalenol;15-Ac-DON:15-乙酰-DON 15-acetyl-deoxynivalenol;DON-GSH:DON-谷胱甘肽deoxynivalenol-glutathione;DON-3-S:DON-3-硫酸盐deoxynivalenol-3-sulfate;DON-15-S:DON-15-硫酸盐deoxynivalenol-15-sulfate。表 1和表 2同the same as Table 1 and Table 2。 图 2 DON的生物转化途径 Fig. 2 Biotransformation pathway of DON |
|
|
表 1 具有DON生物转化作用的微生物 Table 1 Microbes with DON-biotransformation |
|
|
表 2 具有DON生物转化作用的酶 Table 2 Enzymes with DON-biotransformation |
DON的C12, 13环氧基团被认为是导致DON毒性必不可少的基团[33]。动物的肠道和瘤胃微生物可代谢DON形成去环氧化合物DOM-1,在暴露于DON的猪、牛和羊的血浆或排泄物中均发现DOM-1[34-37]。
2.1.1 微生物早在1997年,Binder等[38]在奶牛瘤胃液中通过富集培养程序分离到1株真杆菌属(Eubacterium sp.)菌株BBSH797,该菌可在厌氧条件下转化DON及6种A型单端孢霉烯族毒素。随后Fuchs等[39]采用气相色谱-质谱联用技术(GC-MS)和液相色谱-离子束接口-质谱联用技术(LC-PB-MS)确定DOM-1是菌株BBSH797降解DON的产物。从鸡肠道中分离到的伊格尔兹氏菌属(Eggerthella sp.)菌株DII-9[40]、芽孢杆菌属(Bacillus sp.)菌株LS100[41]、梭菌属(Clostridium sp.)菌株WJ06[42]和史雷克氏菌属(Slackia sp.)菌株[43]D-G9均可在厌氧条件下将DON转化为DOM-1。由于从动物胃肠道中分离到的细菌需在严格厌氧条件下才能发挥将DON转化为DOM-1的作用,这在一定程度上限制了其在实际生产中的应用。为了扩大菌种资源,一些在有氧条件下也能发挥DON去环氧化作用的菌株被陆续分离报道。一些来自土壤的微生物混合物可在有氧条件下对DON进行去环氧化作用。He等[44]在麦田土壤中分离到具有DON去环氧功能的混合菌群PGC-3,经16S rDNA测序发现该菌群由10个属构成,其中脱亚硫酸杆菌属(Desulfitobacterium sp.)在去环氧化过程中可能发挥了重要的作用,之后对该混合菌群进行分离纯培养,得到脱亚硫酸杆菌属细菌PGC-3-9,可将DON完全转化为DOM-1[45]。
2.1.2 生物酶尽管距离首次分离出具有DON去环氧化作用的菌株已过去20多年,但到目前为止,仍没有关于DON去环氧化的酶被报道。Gao等[43]通过对史雷克氏菌属(Slackia sp.)菌株D-G9进行基因组测序并结合比较基因组学分析,鉴定出13个具有DON去环氧化潜力的基因,选取其中2个具有氧化还原活性和3个功能未知的基因分别进行克隆和外源重组表达验证其对DON的去环氧化活性,结果表明以上重组酶均不能催化DON发生去环氧化作用。DON的去环氧化作用可能是一种复杂的过程,今后还应继续对DON去环氧化酶进行挖掘鉴定。
2.1.3 产物DOM-1毒性不同类型细胞的毒性试验结果均表明DOM-1的毒性极低。Sundstøl等[28]通过使用5-溴-2-脱氧尿嘧啶核苷(5-bromo-20-deoxyuridine,BrdU)法测定DOM-1和DON对瑞士小鼠成纤维细胞的细胞毒性,发现DOM-1的半抑制浓度(IC50)值比DON的IC50值高54倍,DOM-1的细胞毒性远小于DON。Mayer等[46]探究了DON及DOM-1对5种不同的细胞系,包括鱼腮细胞(RTgill-W1)、2种猪肠细胞(IPEC-1和IPEC-J2)、小鼠巨噬细胞(RAW 264.7)以及人肝细胞(HepG2)的毒性,结果表明,DOM-1对RTgill-W1、IPEC-1、IPEC-J2和HepG2这4种细胞的细胞活力均没有影响。体内试验结果也表明DOM-1对仔猪无毒,Bracarense等[47]通过DOM-1饲喂断奶仔猪试验探究其对断奶仔猪的毒性,结果表明相较于DON处理,DOM-1处理仔猪的小肠、肝脏和淋巴器官均无损伤。以上结果表明在体内外试验中DOM-1的毒性均较低。
2.2 C3羟基的氧化作用 2.2.1 微生物DON的C3位上的羟基被认为在DON的毒性中发挥了重要的作用,羟基可被多种微生物氧化从而产生3-keto-DON。具有C3位羟基氧化作用的菌株大多分离于土壤中[31, 48-51]。Shima等[31]通过土壤细菌富集培养程序获得菌株根瘤农杆菌(Agrobacterium-Rhizobium)E3-39可氧化DON C3位上的OH基团产生3-keto-DON,这是关于转化产物3-keto-DON的首次报道。Wang等[48]从麦田土壤中分离到菌株德沃斯氏菌(Devosia insulae)A16可在有氧条件下将DON转化为3-keto-DON。除德沃斯氏菌A16外,李笑樱[49]筛选到的德沃斯氏菌(Devosia sp.)ANSB714也可高效转化DON生成3-keto-DON。He等[51]在麦田土壤中分离到的鞘氨醇单胞菌(Sphingomonas sp.)S3-4可将DON氧化为3-keto-DON,但在该反应体系中3-keto-DON仅为中间产物,最终产物为3-epi-DON。除在土壤中分离DON转化菌外,Zhang等[50]在海水中筛选到1株能够将DON转化为3-keto-DON的耐盐海杆菌(Pelagibacterium halotolerans)ANSP101。
2.2.2 生物酶除了DON转化菌的筛选外,关于挖掘菌中的DON生物转化酶基因的工作也在开展。He等[51]通过BAC文库筛选和比较基因组学方法靶到鞘氨醇单胞菌(Sphingomonas sp.)S3-4中负责将DON氧化为3-keto-DON的醛酮还原酶基因AKR18A1,并将其进行基因克隆及外源表达,这是克隆到的首个参与氧化DON C3-OH基团的基因,且该酶需要辅酶氧化型烟酰胺腺嘌呤二核苷酸磷酸(NADP+)的参与发挥催化作用。之后,Carere等[52]通过一系列的分离纯化方法从德沃斯氏菌(Devosia mutans)17-2-E-8中分离出DON转化酶,之后对其进行质谱鉴定并在基因组中得到参与氧化DON生成3-keto-DON的转化酶基因DepA,它编码吡咯喹啉醌(pyrroloquinoline quinone,PQQ)依赖的脱氢酶,该反应的进行依赖于辅酶PQQ。He等[53]利用比较基因组学结合转录组学在DON转化菌德沃斯氏菌(Devosia sp.)D6-9中筛选出1个负责将DON转化为3-keto-DON的醌依赖的脱氢酶基因QDDH。
2.2.3 产物3-keto-DON毒性不同的细胞试验结果均表明DON转化产物3-keto-DON的细胞毒性较低[31, 54]。Shima等[31]以小鼠脾脏淋巴细胞为研究对象,探究DON及3-keto-DON对其细胞增殖的影响,结果表明,3-keto-DON的免疫抑制毒性相较于DON至少降低了90%。He等[54]通过MTT比色法评估DON与3-keto-DON对人结肠癌细胞Caco-2细胞活力的影响,结果表明,3-keto-DON的IC50值是DON的3.03倍;使用BrdU法比较DON与3-keto-DON对小鼠成纤维细胞增殖的影响,发现3-keto-DON的IC50值是DON的4.54倍,结果表明,相较于DON,3-keto-DON的细胞毒性有所降低。除此之外,He等[51]以小麦幼苗为研究对象,通过胚芽鞘接种的方法探究3-keto-DON的植物毒性作用,结果表明,与空白对照组相比,DON显著抑制小麦幼苗生长,而3-keto-DON对其生长无影响。之后通过qRT-PCR测定小麦幼苗中响应DON相关基因的表达水平,结果显示,相较于DON处理,5个DON响应基因(P450、221、C12、C7和C14)在3-keto-DON处理中的表达量均下调。综上所述,3-keto-DON对小麦幼苗的植物毒性较低。
2.3 C3羟基的异构化作用 2.3.1 微生物DON的C3位羟基经异构化后生成3-epi-DON,3-epi-DON是DON的差向异构体。Ikunaga等[30]从麦田土壤中首次分离到具有DON差向异构化能力的菌株类诺卡氏菌属(Nocardioides sp.)菌株WSN05-2。Wang等[55]从麦田土壤中分离到菌株Paradevosia shaoguanensis DDB001可将DON转化为3-epi-DON。具有DON差向异构化能力的菌株大多分离于土壤中。除此之外,Qu等[56]从母乳中分离到鼠李糖乳杆菌(Lactobacillus rhamnosus)SHA113也可将DON转化为3-epi-DON。据报道,分别从麦田土壤和苜蓿土壤中分离得到的鞘氨醇单胞菌(Sphingomonas sp.)S3-4[51]、德沃斯氏菌(Devosia sp.)D6-9[53]和德沃斯氏菌(Devosia mutans)17-2-E-8[57]均可通过两步反应将DON转化为3-epi-DON,DON首先被氧化为3-keto-DON,3-keto-DON进一步被还原为3-epi-DON。但在菌株WSN05-2、DDB001和SHA113的催化过程中,均没有检测到3-keto-DON的存在,原因可能是菌株将DON氧化为中间产物3-keto-DON后,中间产物迅速被还原为3-epi-DON,使得中间产物3-keto-DON不积累,因此没有检测到3-keto-DON;也可能是存在其他转化途径,即DON可直接被差向异构为3-epi-DON[55],具体的原因还尚未可知。
2.3.2 生物酶目前报道的参与DON C3羟基差向异构第2步反应的酶有还原型烟酰胺腺嘌呤二核苷酸磷酸(NADPH)依赖的脱氢酶[58]和醛酮还原酶[53]2种。Carere等[58]通过硫酸铵分级沉淀,阴离子交换柱层析等方法从德沃斯氏菌(Devosia mutans)17-2-E-8中得到将3-keto-DON还原为3-epi-DON反应的酶DepB,之后将其进行基因克隆和外源表达,发现DepB是一种NADPH依赖的脱氢酶,反应的进行需要辅酶NADPH,这是首个克隆出的参与第2步反应的酶基因。随后,He等[53]利用比较基因组学结合转录组学在DON转化菌德沃斯氏菌(Devosia sp.)D6-9中筛选出2个负责将3-keto-DON转化为3-epi-DON的醛酮还原酶基因AKR13B2和AKR6D1。
2.3.3 产物3-epi-DON毒性He等[54]通过MTT法和BrdU法分别比较DON和3-epi-DON对细胞活力及细胞增殖的影响,结果显示,MTT法测得的3-epi-DON的IC50值是DON的357倍,而BrdU法测得的3-epi-DON的IC50值是DON的1 181倍,3-epi-DON的细胞毒性显著降低。人肠上皮细胞的结果表明,3-epi-DON不具有细胞毒性,不会改变细胞的耗氧量,且不会损伤其屏障功能[59]。除细胞试验外,He等[51]通过胚芽鞘接种小麦幼苗的方法评估3-epi-DON的植物毒性,结果表明,3-epi-DON对小麦幼苗的生长无显著抑制作用。此外,利用qRT-PCR检测3-epi-DON接种后小麦响应DON相关基因的表达水平,结果表明,相较于DON处理,P450、221、C12、C7和C14这5个DON响应基因在3-epi-DON处理中的表达量均下调。这些试验结果表明,3-epi-DON的细胞毒性及植物毒性均远低于DON。断奶仔猪饲喂试验结果显示,3-epi-DON可提高断奶仔猪血液中免疫球蛋白M(IgM)的含量,对肠道、肝脏和淋巴器官均无毒性作用,表明3-epi-DON是一种低毒物质[47]。在小鼠饲喂试验中也得到了类似的结果,连续14 d口服3-epi-DON的小鼠与对照组相比体重和器官重量、耗料量、血液和器官的组织病理学均无显著差异[54]。以上体内外试验结果均表明3-epi-DON是一种毒性较低的DON转化产物。
2.4 C16甲基的羟基化作用 2.4.1 微生物C16甲基的羟基化作用是指DON的C16甲基经羟基化生成16-HDON的过程。目前仅有1株鞘氨醇单胞菌(Sphingomonas sp.)KSM1被报道具有C16羟基化作用,该菌株分离自日本湖泊的淡水样品,在需氧条件下可同时催化DON和雪腐镰刀菌烯醇(nivalenol,NIV)生物转化,其中DON被转化为16-HDON[60]。
2.4.2 生物酶Ito等[60]通过筛选菌株KSM1基因组DNA的cosmid文库,鉴定出由1个细胞色素P450蛋白DdnA、1个黄素腺嘌呤二核苷酸(flavin adenine dinucleotide,FAD)依赖性铁氧还蛋白还原酶Kdx以及1个线粒体型[2Fe-2S]的铁氧还蛋白KdR构成的3组分酶系统可降解DON产生16-HDON,将这3组分酶进行外源表达后需添加辅酶烟酰胺腺嘌呤二核苷酸磷酸(NADP)才可发挥羟基化作用。
2.4.3 产物16-HDON毒性Ito等[60]通过小麦发芽试验系统检测DON及16-HDON的植物毒性,结果表明,10 μmol/L DON可显著降低小麦幼苗的重量和长度,增加DON浓度可进一步抑制其生长,而100 μmol/L 16-HDON对小麦幼苗的生长仍没有影响,表明DON经羟基化后对小麦的植物毒性显著降低,16-HDON的植物毒性小于DON的1/10。
2.5 C3羟基的糖基化作用C3羟基的糖基化作用是指DON的C3位羟基经糖基化后生成D3G的过程。植物自身为降低DON产生的毒性可通过自身防御机制形成DON功能化共轭形式,其中C3位羟基糖基化和乙酰化是植物防御机制对DON的解毒形式[61]。作为解毒方式之一,DON可在植物体内经酶的作用进行生物转化形成D3G。研究还发现,一些霉菌也可对DON发生类似的转化作用。Tian等[62]将木霉(Trichoderma)与禾谷镰刀菌(F.graminearum)混合培养,结果表明木霉对禾谷镰刀菌的菌丝生长和霉菌毒素的产生均有明显的抑制作用,且在反应体系中检测到D3G,推测霉菌菌株在与禾谷镰刀菌竞争时产生类似植物的自我保护机制将DON转化为D3G。
2.5.1 生物酶D3G是植物对DON最常见的修饰形式之一,抗赤霉病的拟南芥[61]、大麦[63]及水稻[64]等植物中均存在UDP-葡萄糖基转移酶(UDP glucosyltransferase,UGTs)。Poppenberger等[61]在模式植物拟南芥中分离并鉴定出一种UGT DOGT1,可催化内源葡萄糖从UDP-葡萄糖转移至DON的C3位羟基上从而生成D3G,拟南芥中DOGT1的过表达增强了幼苗对DON的抗性。来自大麦的UGT HvUGT13248可通过将DON转化为D3G从而增强大麦对DON的抗性[63]。来源于水稻的UGT OsUGT79经大肠杆菌重组表达后也可将DON转化为D3G[64]。
2.5.2 产物D3G毒性Pierron等[65]以人肠上皮Caco-2细胞和猪空肠外植体为试验对象,探究D3G诱导核毒性应激和肠道毒性的能力,结果表明,D3G不能与DON的毒性作用位点核糖体肽基转移酶中心的A位点结合。在Caco-2细胞上的研究发现D3G对其细胞活力及屏障功能均无影响,且不会激活c-jun氨基末端激酶(c-jun N-terminal kinases,JNK)和p38丝裂原激活蛋白激酶(p38 mitogen-activated protein kinases,p38 MAPKs)途径从而产生毒性;以猪空肠外植体为研究对象发现D3G对其组织形态无影响。虽然D3G不抑制蛋白质合成,但它经断奶仔猪摄入后,在肠道中几乎完全水解为原型毒素DON,并被吸收和参与体内代谢,从而对机体产生毒性作用[66]。
2.6 乙酰化作用植物对DON的防御机制除糖基化外,还可发生乙酰化。DON C3位上羟基乙酰化产物为3-Ac-DON,C15位上羟基乙酰化产物为15-Ac-DON。
2.6.1 生物酶早在1998年,Kimura等[67]将来自禾谷镰刀菌的C3羟基乙酰转移酶TRI101在大肠杆菌进行重组表达,结果显示TRI101以乙酰辅酶A依赖的方式特异性催化DON C3位羟基的乙酰化。除TRI101外,在一些不具有TRI101乙酰化功能的镰刀菌中,C3乙酰转移酶的活性仍被检测到,这是由TRI201基因编码的乙酰转移酶导致的[68]。Khatibi等[69]通过从7种不同的镰刀菌克隆乙酰转移酶TRI101和TRI201基因,基因同源性为66%~98%,将以上基因进行酵母转化表明,所有TRI101/TRI201均能催化DON乙酰化生成3-Ac-DON,转化效率为50.5%~100.0%,转化效率取决于基因来源的镰刀菌种类。
2.6.2 产物3-Ac-DON和15-Ac-DON毒性目前体外研究报道证实,相较于DON,3-Ac-DON的毒性显著降低[28, 70]。Sundstøl等[28]通过BrdU法测定3-Ac-DON对瑞士小鼠成纤维细胞的细胞毒性,结果表明,3-Ac-DON的IC50值是DON的10倍,3-Ac-DON的细胞毒性相较于DON显著降低。因此,DON C3位羟基乙酰化是一种解毒过程。Broekaert等[70]以猪肠上皮细胞为研究对象,探究3-Ac-DON、D3G和DON对其细胞毒性,结果表明,对增殖细胞的细胞毒性排序为:D3G < 3-Ac-DON < DON。虽然体外试验结果表明3-Ac-DON是一种低毒转化产物,但在体内试验中,肉鸡和猪经口摄入3-Ac-DON后,3-Ac-DON可完全被水解为DON从而对动物发挥毒性作用[71]。
相较于C3位羟基的乙酰化解毒作用,C15位羟基乙酰化通过激活MAPK通路使其产生更强的毒性[72]。BrdU法测定15-Ac-DON对瑞士小鼠成纤维细胞的细胞毒性结果显示,15-Ac-DON的IC50值与DON相同,表明15-Ac-DON的细胞毒性与DON相当[28]。Kadota等[73]以人肠上皮细胞Caco-2细胞为试验对象探究2种乙酰化DON对其细胞毒性作用,结果显示暴露于15-Ac-DON后,肠道的通透性显著增强,跨膜电阻值显著降低,并且会诱导白细胞介素-8(IL-8)的产生从而破坏肠道屏障功能。在猪和肉鸡的体内试验中,与3-Ac-DON类似,15-Ac-DON在猪和鸡静脉注射后,可被去乙酰化形成原型DON发挥毒性作用[71]。
2.7 谷胱甘肽化作用谷胱甘肽化也是植物对DON的一种防御机制。DON的C12, 13环氧基可在谷胱甘肽巯基转移酶(GSH-S-transferease,GST)的催化作用下与谷胱甘肽共轭结合生成DON-GSH。Kluger等[74]发现小麦可将DON转化为DON-GSH。DON转化成DON-GSH这一过程同样存在于大麦中,Gardiner等[75]发现DON能够诱导大麦谷胱甘肽巯基转移酶和半胱氨酸合成酶基因表达上调,半胱氨酸是合成谷胱甘肽的前体,GST负责催化DON和GSH共轭形成DON-GSH;另外,他们还发现DON可以上调ATP结合盒(ATP-binding cassette,ABC)转运体基因表达,ABC转运体能够促进DON-GSH向细胞液泡中转移。
Wang等[76]通过对小麦远缘杂交育种中使用的长穗偃麦草的基因组进行组装,克隆出抗赤霉病的基因Fhb7,并通过构建突变体和转基因小麦验证了该基因的功能。Fhb7编码的谷胱甘肽巯基转移酶通过打开DON的C12, 13环氧基团,并催化其形成DON-GSH降低DON对植物的毒性,降低小麦赤霉病的发生。
2.8 硫酸盐化作用植物对DON的防御机制除糖基化、谷胱甘肽化外,硫酸盐化也是一种防御机制。Warth等[77]在经DON处理过的小麦中检测到DON-3-S和DON-15-S,同时在接种禾谷镰刀菌的小麦中检测到DON-3-S。体外试验表明DON硫酸盐衍生物对小麦核糖体蛋白合成抑制作用远低于DON,因此DON硫酸盐化也是植物体内DON解毒过程的一部分,不过目前尚不清楚DON转化成DON-硫酸盐是否和小麦赤霉病抗性存在关联,也不清楚哪种酶在DON硫酸盐化作用过程中发挥作用。DON硫酸盐化和DON谷胱甘肽化是植物体内的一种解毒方式,产物DON-3-S、DON-15-S和DON-GSH对动物是否具有毒性,在动物胃肠道内是否会像D3G、3-Ac-DON及15-Ac-DON一样被代谢为原型DON继续发挥毒性作用,需要进行动物试验验证。
3 DON生物转化在动物生产中的应用关于DON生物转化的研究已有40余年,目前已有不少关于DON生物转化菌株应用于动物生产中的实例被报道。动物试验结果均表明具有DON生物转化能力的真杆菌属菌株BBSH797[39]、芽孢杆菌属(Bacillus sp.)菌株LS100[41]、梭菌属(Clostridium sp.)菌株WJ06[42]和德沃斯氏菌属(Devosia sp.)[80-81]等菌株能够显著降低DON对试验动物带来的毒性作用。李笑樱[49]对从土壤中筛选到的德沃斯氏菌ANSB714进行毒理学和安全性评价,确认该菌株无毒,之后在小鼠[80]和生长育肥猪[81]上的饲养试验结果均表明菌株ANSB714可明显缓解饲料中DON对动物的毒副作用。青年母猪饲养试验结果表明,在含DON和ZEN霉变饲料中添加由DON转化菌德沃斯氏菌ANSB714和ZEN转化菌枯草芽孢杆菌(Bacillus subtilis)ANSB01G组成的霉菌毒素生物降解剂,可减少2种毒素对母猪生长性能、免疫功能及生殖器官和组织产生的不利影响[82]。将黄曲霉毒素B1(AFB1)转化菌枯草芽孢杆菌ANSB060、ZEN转化菌枯草芽孢杆菌ANSB01G和DON转化菌德沃斯氏菌ANSB714复配成霉菌毒素生物降解剂(mycotoxin biodegradation agent,MBA),试验结果证实MBA可缓解自然霉变饲料(含AFB1、ZEN和DON)对小鼠造成的毒性作用,消除小鼠肾脏中DON的残留[83]。梭菌属细菌WJ06的添加可缓解采食DON污染饲料引起的生长猪生长性能下降,肝脏、肾脏器官指数增加,肠道屏障的完整性受损等毒性作用,且梭菌属细菌WJ06还可调节生长猪的肠道微生态环境[42]。Li等[41]探究了DON转化菌芽孢杆菌LS100处理后的DON污染饲料对猪的作用效果,结果表明芽孢杆菌LS100可消除DON对猪的毒副作用,且单独添加芽孢杆菌LS100对猪消化吸收能力无影响,表明芽孢杆菌LS100是一种安全的微生物。以上研究为微生物生物转化DON在动物实际生产中的应用提供了理论依据。
虽然已有不少关于DON生物转化菌株在动物生产中应用的实例被报道,但目前仅有真杆菌属(Eubacterium sp.)菌株BBSH797作为一种饲料添加剂用于动物DON脱毒的生产实践中[39]。
4 小结与展望DON被各种生物酶转化后的产物D3G、3-Ac-DON和15-Ac-DON进入动物体后,会被动物胃肠道中的一些微生物或生物酶水解或者去乙酰化,重新生成原型毒素DON,因此,DON糖基化和乙酰化生物转化方式并不适用于动物饲料中DON的生物脱毒。目前对于饲料DON的生物转化需重点考虑DON的去环氧化、羟基氧化和差向异构化作用方式,筛选能够发生这几种生物转化作用的微生物或者挖掘生物酶基因。
DON的微生物转化在应用中受到菌株稳定性、作用环境复杂、不在益生菌范畴、饲用安全性和有效性等多方面因素的影响,在一定程度上限制了DON生物转化菌株在动物实际生产中的应用。目前已报道的具有DON生物转化能力的益生菌仅有芽孢杆菌LS100[41]和鼠李糖乳杆菌SHA113[56]2株,因此,通过原位富集、选择性培养及抗生素筛选等方法筛选能够生物转化DON的益生菌,并将其开发成生物转化DON的微生态制剂是饲料DON生物脱毒最经济有效的方法。
此外,还可从已报道的生物转化DON的微生物基因组中挖掘和克隆生物酶基因,从生物酶的角度考虑对饲料DON进行生物脱毒。目前关于DON降解酶的生物信息非常稀缺,限制了新的降解酶基因的挖掘。随着科技的进步,微生物基因组学及代谢组学的联合应用为转化DON生物酶的挖掘提供了理论和技术支持。运用现代分子生物学技术和酶工程技术对生物酶基因进行克隆外源表达和定向进化,提高酶的产量和活性,最终将其开发成一种高效、安全的能够应用于饲料和食品中DON生物脱毒的生物酶制剂。
| [1] |
HUSSEIN H S, BRASEL J M. Toxicity, metabolism, and impact of mycotoxins on humans and animals[J]. Toxicology, 2001, 167(2): 101-134. |
| [2] |
MARESCA M, YAHI N, YOUNÈS-SAKR L, et al. Both direct and indirect effects account for the pro-inflammatory activity of enteropathogenic mycotoxins on the human intestinal epithelium:stimulation of interleukin-8 secretion, potentiation of interleukin-1β effect and increase in the transepithelial passage of commensal bacteria[J]. Toxicology and Applied Pharmacology, 2008, 228(1): 84-92. DOI:10.1016/j.taap.2007.11.013 |
| [3] |
PESTKA J J. Deoxynivalenol:mechanisms of action, human exposure, and toxicological relevance[J]. Archives of Toxicology, 2010, 84(9): 663-679. DOI:10.1007/s00204-010-0579-8 |
| [4] |
BAI G H, SHANER G. Management and resistance in wheat and barley to Fusarium head blight[J]. Annual Review of Phytopathology, 2004, 42: 135-161. DOI:10.1146/annurev.phyto.42.040803.140340 |
| [5] |
雷元培, 周建川, 王利通, 等. 2018年中国饲料原料及配合饲料中霉菌毒素污染调查报告[J]. 饲料工业, 2020, 41(10): 60-64. |
| [6] |
MISHRA S, SRIVASTAVA S, DEWANGAN J, et al. Global occurrence of deoxynivalenol in food commodities and exposure risk assessment in humans in the last decade:a survey[J]. Critical Reviews in Food Science and Nutrition, 2020, 60(8): 1346-1374. DOI:10.1080/10408398.2019.1571479 |
| [7] |
中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会.GB13078-2017饲料卫生标准[S].北京: 中国标准出版社, 2017.
|
| [8] |
国家卫生和计划生育委员会, 国家食品药品监督管理总局.GB2761-2017食品安全国家标准食品中真菌毒素限量[S].北京: 中国标准出版社, 2017.
|
| [9] |
USFDA.Guidance for industry and FDA: Advisory levels for deoxynivalenol (DON) in finished wheat products for human consumption and grains and grain by-products used for animal feed[S].Rockville, MD: USFDA, 2010.
|
| [10] |
European Communities.Commission Regulation (EC) No 1881/2006 of 19 December 2006 setting maximum levels for certain contaminants in foodstuffs[S].[s.l.]: [s.n.], 2006.
|
| [11] |
LEE J Y, LIM W, PARK S, et al. Deoxynivalenol induces apoptosis and disrupts cellular homeostasis through MAPK signaling pathways in bovine mammary epithelial cells[J]. Environmental Pollution, 2019, 252: 879-887. DOI:10.1016/j.envpol.2019.06.001 |
| [12] |
WANG X C, FAN M X, CHU X Y, et al. Deoxynivalenol induces toxicity and apoptosis in piglet hippocampal nerve cells via the MAPK signaling pathway[J]. Toxicon, 2018, 155: 1-8. DOI:10.1016/j.toxicon.2018.09.006 |
| [13] |
ZHANG H, DENG X W, ZHOU C, et al. Deoxynivalenol induces inflammation in IPEC-J2 cells by activating P38 MAPK and Erk1/2[J]. Toxins, 2020, 12(3): 180. DOI:10.3390/toxins12030180 |
| [14] |
LIU D D, WANG Q, HE W M, et al. Two-way immune effects of deoxynivalenol in weaned piglets and porcine alveolar macrophages:due mainly to its exposure dosage[J]. Chemosphere, 2020, 249: 126464. DOI:10.1016/j.chemosphere.2020.126464 |
| [15] |
LI X G, ZHU M, CHEN M X, et al. Acute exposure to deoxynivalenol inhibits porcine enteroid activity via suppression of the Wnt/β-catenin pathway[J]. Toxicology Letters, 2019, 305: 19-31. DOI:10.1016/j.toxlet.2019.01.008 |
| [16] |
GRAZIANI F, PINTON P, OLLEIK H, et al. Deoxynivalenol inhibits the expression of trefoil factors (TFF) by intestinal human and porcine goblet cells[J]. Archives of Toxicology, 2019, 93(4): 1039-1049. DOI:10.1007/s00204-019-02425-6 |
| [17] |
WANG X C, CHEN X F, CAO L, et al. Mechanism of deoxynivalenol-induced neurotoxicity in weaned piglets is linked to lipid peroxidation, dampened neurotransmitter levels, and interference with calcium signaling[J]. Ecotoxicology and Environmental Safety, 2020, 194: 110382. DOI:10.1016/j.ecoenv.2020.110382 |
| [18] |
SALAHIPOUR M H, HASANZADEH S, MALEKINEJAD H, et al. Deoxynivalenol reduces quality parameters and increases DNA damage in mice spermatozoa[J]. Andrologia, 2019, 51(5): e13238. DOI:10.1111/and.13238 |
| [19] |
WACHÉ Y J, HBABI-HADDIOUI L, GUZYLACK-PIRIOU L, et al. The mycotoxin deoxynivalenol inhibits the cell surface expression of activation markers in human macrophages[J]. Toxicology, 2009, 262(3): 239-244. DOI:10.1016/j.tox.2009.06.014 |
| [20] |
YOUNG L G, MCGIRR L, VALLI V E, et al. Vomitoxin in corn fed to young pigs[J]. Journal of Animal Science, 1983, 57(3): 655-664. DOI:10.2527/jas1983.573655x |
| [21] |
SAVI G D, CARDOSO W A, FURTADO B G, et al. Antifungal activities against toxigenic Fusarium specie and deoxynivalenol adsorption capacity of ion-exchanged zeolites[J]. Journal of Environmental Science and Health, 2018, 53(3): 184-190. DOI:10.1080/03601234.2017.1405639 |
| [22] |
LI M M, GUAN E Q, BIAN K. Detoxification of deoxynivalenol by 60Co γ-ray irradiation and toxicity analyses of radiolysis products[J]. Journal of AOAC International, 2019, 102(6): 1749-1755. DOI:10.1093/jaoac/102.6.1749 |
| [23] |
BAI X J, SUN C P, LIU D, et al. Photocatalytic degradation of deoxynivalenol using graphene/ZnO hybrids in aqueous suspension[J]. Applied Catalysis B-Environmental, 2017, 204: 11-20. DOI:10.1016/j.apcatb.2016.11.010 |
| [24] |
WANG L, WANG Y, SHAO H L, et al. In vivo toxicity assessment of deoxynivalenol-contaminated wheat after ozone degradation[J]. Food Additives & Contaminants:Part A, 2017, 34(1): 103-112. |
| [25] |
XU Y, JI J, WU H, et al. Untargeted GC-TOFMS-based cellular metabolism analysis to evaluate ozone degradation effect of deoxynivalenol[J]. Toxicon, 2019, 168: 49-57. DOI:10.1016/j.toxicon.2019.06.022 |
| [26] |
REMPE I, KERSTEN S, VALENTA H, et al. Hydrothermal treatment of naturally contaminated maize in the presence of sodium metabisulfite, methylamine and calcium hydroxide; effects on the concentration of zearalenone and deoxynivalenol[J]. Mycotoxin Research, 2013, 29(3): 169-175. DOI:10.1007/s12550-013-0166-y |
| [27] |
HE J W, ZHOU T, YOUNG J C, et al. Chemical and biological transformations for detoxification of trichothecene mycotoxins in human and animal food chains:a review[J]. Trends in Food Science & Technology, 2010, 21(2): 67-76. |
| [28] |
ERIKSEN G S, PETTERSSON H, LUNDH T. Comparative cytotoxicity of deoxynivalenol, nivalenol, their acetylated derivatives and de-epoxy metabolites[J]. Food and Chemical Toxicology, 2004, 42(4): 619-624. DOI:10.1016/j.fct.2003.11.006 |
| [29] |
DESJARDINS A E, HOHN T M, MCCORMICK S P. Trichothecene biosynthesis in Fusarium species:chemistry, genetics, and significance[J]. Microbiological Reviews, 1993, 57(3): 595-604. DOI:10.1128/MMBR.57.3.595-604.1993 |
| [30] |
IKUNAGA Y, SATO I, GROND S, et al. Nocardioides sp. strain WSN05-2, isolated from a wheat field, degrades deoxynivalenol, producing the novel intermediate 3-epi-deoxynivalenol[J]. Applied Microbiology and Biotechnology, 2011, 89(2): 419-427. |
| [31] |
SHIMA J, TAKASE S, TAKAHASHI Y, et al. Novel detoxification of the trichothecene mycotoxin deoxynivalenol by a soil bacterium isolated by enrichment culture[J]. Applied and Environmental Microbiology, 1997, 63(10): 3825-3830. DOI:10.1128/AEM.63.10.3825-3830.1997 |
| [32] |
SATO I, ITO M, ISHIZAKA M, et al. Thirteen novel deoxynivalenol-degrading bacteria are classified within two genera with distinct degradation mechanisms[J]. FEMS Microbiology Letters, 2012, 327(2): 110-117. DOI:10.1111/j.1574-6968.2011.02461.x |
| [33] |
ROTTER B A. Invited review:toxicology of deoxynivalenol (vomitoxin)[J]. Journal of Toxicology and Environmental Health, 1996, 48(1): 1-34. |
| [34] |
DÄNICKE S, VALENTA H, DÖLL S. On the toxicokinetics and the metabolism of deoxynivalenol (don) in the pig[J]. Archives of Animal Nutrition, 2004, 58(2): 169-180. DOI:10.1080/00039420410001667548 |
| [35] |
SEELING K, DÄNICKE S, VALENTA H, et al. Effects of Fusarium toxin-contaminated wheat and feed intake level on the biotransformation and carry-over of deoxynivalenol in dairy cows[J]. Food Additives & Contaminants, 2006, 23(10): 1008-1020. |
| [36] |
PRELUSKY D B, VEIRA D M, TRENHOLM H L, et al. Metabolic fate and elimination in milk, urine and bile of deoxynivalenol following administration to lactating sheep[J]. Journal of Environmental Science and Health (Part B), 1987, 22(2): 125-148. DOI:10.1080/03601238709372550 |
| [37] |
HE P, YOUNG L G, FORSBERG C. Microbially detoxified vomitoxin-contaminated corn for young pigs[J]. Journal of Animal Science, 1993, 71(4): 963-967. DOI:10.2527/1993.714963x |
| [38] |
BINDER J, HORVATH E M, SCHATZMAYR G, et al. Screening for deoxynivalenol-detoxifying anaerobic rumen microorganisms[J]. Cereal Research Communications, 1997, 25(31): 343-346. |
| [39] |
FUCHS E, BINDER E M, HEIDLER D, et al. Structural characterization of metabolites after the microbial degradation of type A trichothecenes by the bacterial strain BBSH 797[J]. Food Additives & Contaminants, 2002, 19(4): 379-386. |
| [40] |
GAO X J, MU P Q, WEN J K, et al. Detoxification of trichothecene mycotoxins by a novel bacterium, Eggerthella sp. DⅡ-9[J]. Food and Chemical Toxicology, 2018, 112: 310-319. DOI:10.1016/j.fct.2017.12.066 |
| [41] |
LI X Z, ZHU C, DE LANGE C F M, et al. Efficacy of detoxification of deoxynivalenol-contaminated corn by Bacillus sp. LS100 in reducing the adverse effects of the mycotoxin on swine growth performance[J]. Food Additives & Contaminants, 2011, 28(7): 894-901. |
| [42] |
LI F C, WANG J Q, HUANG L B, et al. Effects of adding Clostridium sp. WJ06 on intestinal morphology and microbial diversity of growing pigs fed with natural deoxynivalenol contaminated wheat[J]. Toxins, 2017, 9(12): 383. DOI:10.3390/toxins9120383 |
| [43] |
GAO X J, MU P Q, ZHU X H, et al. Dual function of a novel bacterium, Slackia sp. D-G6:detoxifying deoxynivalenol and producing the natural estrogen analogue, equol[J]. Toxins, 2020, 12(2): 85. |
| [44] |
HE W J, YUAN Q S, ZHANG Y B, et al. Aerobic de-epoxydation of trichothecene mycotoxins by a soil bacterial consortium isolated using in situ soil enrichment[J]. Toxins, 2016, 8(10): 277. DOI:10.3390/toxins8100277 |
| [45] |
HE W J, SHI M M, YANG P, et al. Novel soil bacterium strain Desulfitobacterium sp. PGC-3-9 detoxifies trichothecene mycotoxins in wheat via de-epoxidation under aerobic and anaerobic conditions[J]. Toxins, 2020, 12(6): 363. DOI:10.3390/toxins12060363 |
| [46] |
MAYER E, NOVAK B, SPRINGLER A, et al. Effects of deoxynivalenol (DON) and its microbial biotransformation product deepoxy-deoxynivalenol (DOM-1) on a trout, pig, mouse, and human cell line[J]. Mycotoxin Research, 2017, 33(4): 297-308. DOI:10.1007/s12550-017-0289-7 |
| [47] |
BRACARENSE A P F L, PIERRON A, PINTON P, et al. Reduced toxicity of 3-epi-deoxynivalenol and de-epoxy-deoxynivalenol through deoxynivalenol bacterial biotransformation:in vivo analysis in piglets[J]. Food and Chemical Toxicology, 2020, 140: 111241. DOI:10.1016/j.fct.2020.111241 |
| [48] |
WANG G, WANG Y X, JI F, et al. Biodegradation of deoxynivalenol and its derivatives by Devosia insulae A16[J]. Food Chemistry, 2019, 276: 436-442. DOI:10.1016/j.foodchem.2018.10.011 |
| [49] |
李笑樱.降解呕吐毒素德沃斯氏菌的饲用安全性和有效性评价[D].博士学位论文.北京: 中国农业大学, 2015: 39-44. http://cdmd.cnki.com.cn/Article/CDMD-10019-1016305045.htm
|
| [50] |
ZHANG J, QIN X J, GUO Y P, et al. Enzymatic degradation of deoxynivalenol by a novel bacterium, Pelagibacterium halotolerans ANSP101[J]. Food and Chemical Toxicology, 2020, 140: 111276. DOI:10.1016/j.fct.2020.111276 |
| [51] |
HE W J, ZHANG L M, Yi S Y, et al. An aldo-keto reductase is responsible for Fusarium toxin-degrading activity in a soil Sphingomonas strain[J]. Scientific Reports, 2017, 7: 9549. DOI:10.1038/s41598-017-08799-w |
| [52] |
CARERE J, HASSAN Y I, LEPP D, et al. The enzymatic detoxification of the mycotoxin deoxynivalenol:identification of DepA from the DON epimerization pathway[J]. Microbial Biotechnology, 2018, 11(6): 1106-1111. DOI:10.1111/1751-7915.12874 |
| [53] |
HE W J, SHI M M, YANG P, et al. A quinone-dependent dehydrogenase and two NADPH-dependent aldo/keto reductases detoxify deoxynivalenol in wheat via epimerization in a Devosia strain[J]. Food Chemistry, 2020, 321: 126703. DOI:10.1016/j.foodchem.2020.126703 |
| [54] |
HE J W, BONDY G S, ZHOU T, et al. Toxicology of 3-epi-deoxynivalenol, a deoxynivalenol-transformation product by Devosia mutans 17-2-E-8[J]. Food and Chemical Toxicology, 2015, 84: 250-259. DOI:10.1016/j.fct.2015.09.003 |
| [55] |
WANG Y, ZHANG H H, ZHAO C, et al. Isolation and characterization of a novel deoxynivalenol-transforming strain Paradevosia shaoguanensis DDB001 from wheat field soil[J]. Letters in Applied Microbiology, 2017, 65(5): 414-422. DOI:10.1111/lam.12790 |
| [56] |
QU R, JIANG C M, WU W Q, et al. Conversion of DON to 3-epi-DON in vitro and toxicity reduction of DON in vivo by Lactobacillus rhamnosus[J]. Food & Function, 2019, 10(5): 2785-2796. |
| [57] |
HASSAN Y I, HE J W, PERILLA N, et al. The enzymatic epimerization of deoxynivalenol by Devosia mutans proceeds through the formation of 3-keto-DON intermediate[J]. Scientific Reports, 2017, 7: 6929. DOI:10.1038/s41598-017-07319-0 |
| [58] |
CARERE J, HASSAN Y I, LEPP D, et al. The identification of DepB:an enzyme responsible for the final detoxification step in the deoxynivalenol epimerization pathway in Devosia mutans 17-2-E-8[J]. Frontiers in Microbiology, 2018, 9: 1573. DOI:10.3389/fmicb.2018.01573 |
| [59] |
PIERRON A, MIMOUN S, MURATE L S, et al. Microbial biotransformation of DON:molecular basis for reduced toxicity[J]. Scientific Reports, 2016, 6: 29105. DOI:10.1038/srep29105 |
| [60] |
ITO M, SATO I, ISHIZAKA M, et al. Bacterial cytochrome P450 system catabolizing the Fusarium toxin deoxynivalenol[J]. Applied and Environmental Microbiology, 2013, 79(5): 1619-1628. DOI:10.1128/AEM.03227-12 |
| [61] |
POPPENBERGER B, BERTHILLER F, LUCYSHYN D, et al. Detoxification of the Fusarium mycotoxin deoxynivalenol by a UDP-glucosyltransferase from Arabidopsis thaliana[J]. The Journal of Biological Chemistry, 2003, 278(48): 47905-47914. DOI:10.1074/jbc.M307552200 |
| [62] |
TIAN Y, TAN Y L, LIU N, et al. Detoxification of deoxynivalenol via glycosylation represents novel insights on antagonistic activities of Trichoderma when confronted with Fusarium graminearum[J]. Toxins, 2016, 8(11): 335. DOI:10.3390/toxins8110335 |
| [63] |
SCHWEIGER W, BODDU J, SHIN S, et al. Validation of a candidate deoxynivalenol-inactivating UDP-glucosyltransferase from barley by heterologous expression in yeast[J]. Molecular Plant-Microbe Interactions, 2010, 23(7): 977-986. DOI:10.1094/MPMI-23-7-0977 |
| [64] |
MICHLMAYR H, MALACHOVÁ A, VARGA E, et al. Biochemical characterization of a recombinant UDP-glucosyltransferase from rice and enzymatic production of deoxynivalenol-3-O-β-D-glucoside[J]. Toxins, 2015, 7(7): 2685-2700. DOI:10.3390/toxins7072685 |
| [65] |
PIERRON A, MIMOUN S, MURATE L S, et al. Intestinal toxicity of the masked mycotoxin deoxynivalenol-3-β-D-glucoside[J]. Archives of Toxicology, 2016, 90(8): 2037-2046. DOI:10.1007/s00204-015-1592-8 |
| [66] |
NAGL V, WOECHTL B, SCHWARTZ-ZIMMERMANN H E, et al. Metabolism of the masked mycotoxin deoxynivalenol-3-glucoside in pigs[J]. Toxicology Letters, 2014, 229(1): 190-197. |
| [67] |
KIMURA M, KANEKO I, KOMIYAMA M, et al. Trichothecene 3-O-acetyltransferase protects both the producing organism and transformed yeast from related mycotoxins:cloning and characterization of Tri101[J]. Journal of Biological Chemistry, 1998, 273(3): 1654-1661. DOI:10.1074/jbc.273.3.1654 |
| [68] |
KIMURA M, TOKAI T, MATSUMOTO G, et al. Trichothecene nonproducer Gibberella species have both functional and nonfunctional 3-O-acetyltransferase genes[J]. Genetics, 2003, 163(2): 677-684. |
| [69] |
KHATIBI P A, NEWMISTER S A, RAYMENT I, et al. Bioprospecting for Trichothecene 3-O-acetyltransferases in the fungal genus Fusarium yields functional enzymes with different abilities to modify the mycotoxin deoxynivalenol[J]. Applied and Environmental Microbiology, 2011, 77(4): 1162-1170. DOI:10.1128/AEM.01738-10 |
| [70] |
BROEKAERT N, DEVREESE M, DEMEYERE K, et al. Comparative in vitro cytotoxicity of modified deoxynivalenol on porcine intestinal epithelial cells[J]. Food and Chemical Toxicology, 2016, 95: 103-109. DOI:10.1016/j.fct.2016.06.012 |
| [71] |
BROEKAERT N, DEVREESE M, DE MIL T, et al. Oral bioavailability, hydrolysis, and comparative toxicokinetics of 3-acetyldeoxynivalenol and 15-acetyldeoxynivalenol in broiler chickens and pigs[J]. Journal of Agricultural and Food Chemistry, 2015, 63(39): 8734-8742. DOI:10.1021/acs.jafc.5b03270 |
| [72] |
PINTON P, TSYBULSKYY D, LUCIOLI J, et al. Toxicity of deoxynivalenol and its acetylated derivatives on the intestine:differential effects on morphology, barrier function, tight junction proteins, and mitogen-activated protein kinases[J]. Toxicological Sciences, 2012, 130(1): 180-190. DOI:10.1093/toxsci/kfs239 |
| [73] |
KADOTA T, FURUSAWA H, HIRANO S, et al. Comparative study of deoxynivalenol, 3-acetyldeoxynivalenol, and 15-acetyldeoxynivalenol on intestinal transport and IL-8 secretion in the human cell line Caco-2[J]. Toxicology in Vitro, 2013, 27(6): 1888-1895. DOI:10.1016/j.tiv.2013.06.003 |
| [74] |
KLUGER B, BUESCHL C, LEMMENS M, et al. Biotransformation of the mycotoxin deoxynivalenol in Fusarium resistant and susceptible near isogenic wheat lines[J]. PLoS One, 2015, 10(3): e0119656. DOI:10.1371/journal.pone.0119656 |
| [75] |
GARDINER S A, BODDU J, BERTHILLER F, et al. Transcriptome analysis of the barley-deoxynivalenol interaction:evidence for a role of glutathione in deoxynivalenol detoxification[J]. Molecular Plant-Microbe Interactions, 2010, 23(7): 962-976. DOI:10.1094/MPMI-23-7-0962 |
| [76] |
WANG H W, SUN S L, GE W Y, et al. Horizontal gene transfer of Fhb7 from fungus underlies Fusarium head blight resistance in wheat[J]. Science, 2020, 368(6493): eaba5435. DOI:10.1126/science.aba5435 |
| [77] |
WARTH B, FRUHMANN P, WIESENBERGER G, et al. Deoxynivalenol-sulfates:identification and quantification of novel conjugated (masked) mycotoxins in wheat[J]. Analytical and Bioanalytical Chemistry, 2015, 407(4): 1033-1039. DOI:10.1007/s00216-014-8340-4 |
| [78] |
GUAN S, HE J W, YOUNG J C, et al. Transformation of trichothecene mycotoxins by microorganisms from fish digesta[J]. Aquaculture, 2009, 290(3/4): 290-295. |
| [79] |
ISLAM R, ZHOU T, YOUNG J C, et al. Aerobic and anaerobic de-epoxydation of mycotoxin deoxynivalenol by bacteria originating from agricultural soil[J]. World Journal of Microbiology and Biotechnology, 2012, 28(1): 7-13. |
| [80] |
ZHAO L H, LI X Y, JI C, et al. Protective effect of Devosia sp. ANSB714 on growth performance, serum chemistry, immunity function and residues in kidneys of mice exposed to deoxynivalenol[J]. Food and Chemical Toxicology, 2016, 92: 143-149. DOI:10.1016/j.fct.2016.03.020 |
| [81] |
LI X Y, GUO Y P, ZHAO L H, et al. Protective effects of Devosia sp. ANSB714 on growth performance, immunity function, antioxidant capacity and tissue residues in growing-finishing pigs fed with deoxynivalenol contaminated diets[J]. Food and Chemical Toxicology, 2018, 121: 246-251. DOI:10.1016/j.fct.2018.09.007 |
| [82] |
SHI D H, ZHOU J C, ZHAO L H, et al. Alleviation of mycotoxin biodegradation agent on zearalenone and deoxynivalenol toxicosis in immature gilts[J]. Journal of Animal Science and Biotechnology, 2018, 9: 42. DOI:10.1186/s40104-018-0255-z |
| [83] |
GUO Y P, HUO X T, ZHAO L H, et al. Protective effects of Bacillus subtilis ANSB060, Bacillus subtilis ANSB01G, and Devosia sp. ANSB714-based mycotoxin biodegradation agent on mice fed with naturally moldy diets[J]. Probiotics and Antimicrobial Proteins, 2019, 12(3): 994-1001. |




