2. 塔里木大学动物科学技术学院, 阿拉尔 843300
2. College of Animal Science of Tarim University, Alar 843300, China
哺乳期反刍动物胃肠道发育迅速[1],此阶段充足的营养物质摄入可促进其胃肠道发育,发挥生长潜能[2]。在羔羊哺乳阶段实施早期断奶,并补饲营养充足且易消化的代乳粉是一种提高羔羊生长性能的营养调控途径。通过早期营养调控动物后期生理及生长性能的表观遗传反应称为代谢印记[3],探究早期断奶产生的代谢印记对羔羊早期培育具有重要意义。前人研究表明,早期断奶可以促进羔羊瘤胃发育,提高生长性能[4]。柴建民[5]研究发现,羔羊20日龄断奶,补饲代乳粉期间日增重与随母哺乳羔羊无显著差异,且断代乳粉后羔羊生长性能优于随母哺乳羔羊,肉品质得到改善。但Emsen等[6]用代乳粉对羔羊进行超早期断奶,发现2~4周龄羔羊体重和日增重均显著低于随母哺乳组,而6周龄后2组体重接近。与自然断奶相比,早期断奶对羔羊各项生理机能的影响更显著[7-8]。有关羔羊早期营养的代谢印记研究已有不少报道[9-10]。Soberon等[11]通过对比2个牛场的生产记录,研究奶牛营养摄入与第1次泌乳量的关系发现,断奶时奶牛日增重对奶牛第1次泌乳量的贡献率达22%。羔羊早期断奶研究多集中于羔羊断奶前后短时期的生理变化,而对羔羊后期生长性能的持续影响鲜见报道。羔羊实行早期断奶目的在于发挥肉羊整个生长周期的潜力,最大化养殖效益,因此研究早期断奶对羔羊生长育肥阶段的持续影响显得极为迫切。本试验以20日龄羔羊为研究对象,研究早期断奶并补饲代乳粉对羔羊生长性能、消化性能、血清生化指标及肉品质的持续影响,旨在探究早期断奶对羔羊生理的持续作用,更科学评价早期断奶的生产意义。
1 材料与方法 1.1 试验时间和地点于2018年7月至2019年1月在山东聊城临清润林牧业有限公司开展动物试验。
1.2 试验动物与分组试验选取体重[(8.26±2.14) kg]、日龄[(20±1)日龄]接近的健康湖羊公羔60只,随机分成随母哺乳组(ER组,作为对照)和早期断奶组(EW组),每组6个重复,每个重复5只羔羊。ER组羔羊饲喂母乳+开食料;EW组羔羊饲喂代乳粉+开食料。所有羔羊从20日龄开始补饲开食料至65日龄,之后过渡至育肥颗粒料(66~120日龄:育肥前期颗粒料;121~180日龄:育肥后期颗粒料),开食料与育肥颗粒料均自由采食。
1.3 试验饲粮试验用羔羊代乳粉(配方见专利ZL201210365927.6)由北京精准动物研究中心提供;羔羊开食料由润林牧业有限公司提供,颗粒直径为5 mm,长度为4~6 cm。育肥颗粒料直径为7 mm,长度为4~6 cm,葵花籽壳纤维长度为3~5 mm,由北京三元禾丰牧业有限公司加工制作。试验饲粮组成及营养水平见表 1。
|
|
表 1 试验饲粮组成及营养水平(干物质基础) Table 1 Composition and nutrient levels of experimental diets (DM basis) |
所有试验羔羊均打耳标,免疫程序按羊场正规程序实施,每隔15 d对羊舍全面消毒(5%聚维酮碘、2%稀戊二醛)1次。每个重复1个栏位,每栏5只羊,自由采食及饮水。
所有试验羔羊出生至20日龄均随母哺乳,20日龄后进行分组试验。ER组羔羊55日龄开始减少母乳摄入,至60日龄完全断奶。EW组羔羊断奶日龄选择参照柴建民[5]的试验结果,按羔羊体重的1%饲喂代乳粉,具体饲喂操作参照祁敏丽等[13]试验中的方法进行,即羔羊20~35日龄阶段代乳粉每天饲喂3次(07:00、13:00、17:00),35日龄后代乳粉每天饲喂2次(08:00、16:00)。当羔羊开食料采食量达300 g/d时停止饲喂代乳粉[14]。整个试验期开食料均自由采食,每天补料2次(08:00和16:00)。所有试验羔羊65日龄后逐渐停止饲喂开食料,过渡至育肥颗粒料,所有羔羊66~120日龄饲喂育肥前期颗粒料,121~180日龄饲喂育肥后期颗粒料。羔羊断奶及饲粮更换时均有5 d的过渡期。试验预试期5 d,正试期155 d,羔羊25日龄正式开始试验。试验期间所有试验羔羊自由饮水。
1.5 消化代谢试验于羔羊55~65日龄、115~125日龄、170~180日龄采用全收粪法进行消化代谢试验。每个重复随机选取1只羔羊(体重接近该重复羊平均体重,健康无病)进行消化代谢试验,预试期5 d,正试期5 d。正试期内准确地记录每只羔羊每日的采食量、排粪量。收集全部粪样,按照100 g鲜粪加入10%的稀硫酸10 mL对样品进行固氮,-20 ℃保存。
1.6 样品采集与指标测定 1.6.1 饲粮常规营养物质含量的测定饲粮常规营养物质含量的测定方法:使用氧弹量热仪(Parr-6400)测定总能;采用全自动凯氏定氮仪(KDY-9830)测定粗蛋白质含量;除代乳粉中粗脂肪含量采用国标法(GB/T 6433—2006)测定外,饲粮干物质、粗脂肪、粗灰分、中性洗涤纤维、酸性洗涤纤维、钙和磷含量均参考《饲料分析及饲料质量检测技术》[15]测定。
1.6.2 生长性能的测定记录所有试验羔羊25、35、45、55、65、90、120、150、180日龄晨饲前体重,根据各阶段的始末体重计算平均日增重(ADG)。每天准确称量并记录羔羊开食料投料量及前1天的剩料量,计算羔羊开食料采食量和干物质采食量(DMI)。根据各阶段始末体重和采食量计算饲料转化率(FCR)。
1.6.3 营养物质消化率的测定试验结束后,将每只羔羊5 d的粪样全部均匀混合,并取适量于65 ℃烘箱烘干,按照1.6.1中方法测定干物质、粗蛋白质、粗脂肪、中性洗涤纤维、酸性洗涤纤维含量及总能,计算营养物质消化率,计算公式如下:

|
在羔羊65、120、180日龄晨饲前(08:00)颈静脉采血8 mL,收集于10 mL含二氧化硅的促凝管中,静置30 min后,放于低速离心机在3 000 r/min下离心20 min,收集2 mL上层血清,-20 ℃冰箱保存待测。采用全自动生化分析仪(日立7600,日本)测定血清中尿素氮(UN)、葡萄糖(GLU)和游离脂肪酸(NEFA)含量,采用酶联免疫吸附测定(ELISA)试剂盒测定血清中β-羟丁酸(BHBA)、生长激素(GH)和胰岛素样生长因子-1(IGF-1)含量。
1.6.5 肉品质的测定在羔羊180日龄时每个重复选取1只羔羊进行屠宰,试验羊屠宰时,记录宰前活重(LWBS)、胴体重,并计算屠宰率。试验羊屠宰后,取左侧背最长肌,测定肉品质指标。
pH:用Testo 206型pH计测定背最长肌pH。
剪切力:用肌肉嫩度仪(北京龙德泰达生物技术有限公司,C-LM3型)测定背最长肌剪切力。
滴水损失率:切取长×宽×厚为5 cm×3 cm×2 cm的背最长肌肉样2块称重,记为m1,用铁丝悬挂于倒扣的一次性纸杯内,编号,样品不沾杯侧壁且不超过杯口,置于4 ℃冰箱中静置,24 h取出肉样,用吸水纸将表面的水分吸干并称重,记为m2。滴水损失率计算公式为:
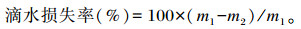
|
熟肉率:切取长×宽×厚为5 cm×3 cm×2 cm的背最长肌肉样2块称重,记为m3,放入自封袋后编号,在80 ℃水浴锅中加热30 min,冷却后置于4 ℃冰箱过夜,用吸水纸吸干肉样水分后称重,记为m4。熟肉率计算公式如下:
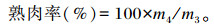
|
眼肌面积:用硫酸纸轻贴倒数第1~2脊柱上的眼肌(背最长肌)横截面,描绘肌肉轮廓,并计算眼肌面积。
GR值(代表胴体脂肪含量):用游标卡尺测量第12~13肋骨间距离背脊中线11 cm处的组织厚度。
1.7 数据统计与分析试验数据采用Excel 2010进行整理,采用SPSS 19.4进行统计分析。试验数据进行正态分布和方差齐性检验后,进行独立样本t检验(independent t-test),以P < 0.05作为差异显著的判断标准,0.05≤P < 0.10作为差异具有显著趋势的判断标准。羔羊体重和平均日增重变化折线图采用GraphPad Prism 8.0软件绘制。
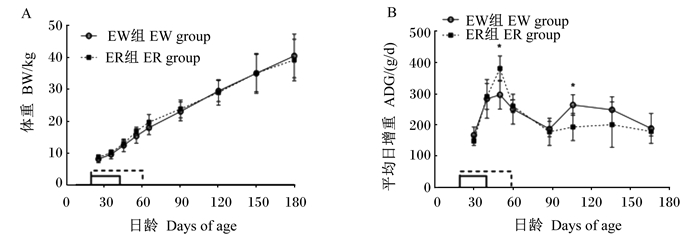
2 结果与分析 2.1 早期断奶并补饲代乳粉对羔羊生长性能的持续影响2组羔羊试验初始体重无显著差异(P>0.05,表 2),符合试验设计要求。在25~180日龄阶段,2组羔羊体重变化趋势一致,不同日龄时均无显著差异(P>0.05,图 1-A)。羔羊25~65日龄阶段的平均日增重表现为EW组显著低于ER组(P < 0.05),通过图 1-B可知,2组羔羊断奶前的平均日增重主要在46~55日龄阶段产生差异,表现为EW组显著低于ER组(P < 0.05)。25~65日龄阶段,EW组羔羊开食料采食量显著高于ER组(P < 0.05)。
|
|
表 2 早期断奶并补饲代乳粉对羔羊生长性能的持续影响 Table 2 Persistent effects of early weaning and supplementary feeding milk replacer on growth performance of lambs |
|
数据点标注“*”表示2组间差异显著(P < 0.05)。横坐标轴上虚线表示ER组羔羊随母哺乳时间,实线表示EW组羔羊饲喂代乳粉时间。 Data points with "*" mean significant difference between 2 groups (P < 0.05). The dotted line on the abscissa axis represents the time on breastfeeding of ER group with the mother, and the solid line represents the time for EW group to feed the milk replacer. 图 1 羔羊体重(A)和平均日增重变化趋势(B) Fig. 1 Variation trends of BW (A) and ADG (B) of lambs |
本试验中,早期断奶羔羊在42日龄开食料采食量达300 g/d,由图 1-B可知,羔羊断奶进入育肥阶段后平均日增重变化趋势发生反转,91~120日龄阶段EW组显著高于ER组(P < 0.05),121~150日龄阶段EW组比ER组高出48 g/d。从整个育肥阶段(66~180日龄)来看,2组羔羊的平均日增重和体重无显著差异(P>0.05)。在25~65日龄阶段,EW组羔羊的开食料采食量显著高于ER组(P < 0.05),高出145 g/d;在66~120日龄阶段,EW组羔羊的干物质采食量显著高于ER组(P < 0.05),高出107 g/d;而在121~180日龄阶段,2组羔羊干物质采食量未出现显著差异(P>0.05)。整个育肥期(包括66~120日龄和121~180日龄阶段)2组羔羊的饲料转化率均没有显著差异(P>0.05)。
2.2 早期断奶并补饲代乳粉对羔羊营养物质消化率的持续影响根据中表 3消化代谢试验数据可知,2组羔羊55~65日龄阶段各营养物质消化率均未出现显著差异(P>0.05),这一营养物质消化率相近的趋势持续了整个育肥期,具体表现为EW、ER组羔羊在115~125日龄、170~180日龄阶段各营养物质消化率均未出现显著差异(P>0.05)。
|
|
表 3 早期断奶并补饲代乳粉对羔羊营养物质消化率的持续影响 Table 3 Persistent effects of early weaning and supplementary feeding milk replacer on nutrient digestibility of lambs |
由表 4可知,在65、120日龄时,EW组羔羊血清UN含量显著高于ER组(P < 0.05)。在65日龄时,EW组羔羊血清IGF-1含量相比ER组差异虽未达到显著水平(P>0.05),但有升高趋势(P=0.053),同时血清GH含量显著高于ER组(P < 0.05);在120日龄时,EW组羔羊血清IGF-1、GH含量均显著高于ER组(P < 0.05);至180日龄时,2组羔羊血清IGF-1、GH含量的差异不再显著(P>0.05),但EW组血清BHBA含量显著低于ER组(P < 0.05)。
|
|
表 4 早期断奶并补饲代乳粉对羔羊血清生化指标的持续影响 Table 4 Persistent effects of early weaning and supplementary feeding milk replacer on serum biochemical indices of lambs |
由表 5可知,2组羔羊宰前活重、屠宰率无显著差异(P>0.05),背最长肌的pH均在6.5~6.6。EW组羔羊背最长肌的熟肉率相比ER组差异虽未达到显著水平(P>0.05),但有升高趋势(P=0.061)。2组羔羊背最长肌的滴水损失率、眼肌面积、GR值和剪切力均无显著差异(P>0.05)。
|
|
表 5 早期断奶并补饲代乳粉对180日龄羔羊肉品质的影响 Table 5 Effects of early weaning and supplementary feeding milk replacer on meat quality of lambs at 180 days of age |
羔羊的生长性能与养殖效益紧密联系[16],评判养殖工艺的实用性首先要明确其对提高羔羊生长性能的贡献率[17]。早期断奶并补饲代乳粉提高了羔羊对营养物质的摄入量,促进了羔羊采食,并促进了瘤胃发育,提高了生长性能[18-19],张乃锋等[10]通过相关分析发现羔羊断奶前后体重和日增重、采食量存在显著正相关关系,呈现出代谢印记。值得关注的是,饲养因素并非总以同一种影响趋势持续作用于羔羊的生长,解彪等[20]试验表明早期断奶羔羊饲喂较高中性洗涤纤维含量的饲粮对羔羊育肥前期生长性能有促进作用,但羔羊在育肥后期增重速度反而降低,促生长作用仅持续1个月。Moallem等[21]发现,犊牛完全断奶后,饲喂代乳粉组与饲喂牛奶组相比,60~150日龄阶段平均日增重接近,15~45日龄阶段平均日增重有提高趋势,46~60日龄阶段平均日增重增长趋势相同,表明通过观察羔羊整个生长周期的增重及生理变化评价饲养工艺实用性更加科学。
通过各阶段的平均日增重折线图并结合表 2数据,可从羔羊3个生长阶段(20~65日龄、66~120日龄、121~180日龄)讨论早期断奶并补饲代乳粉对羔羊增重的影响。EW组羔羊相比ER组在46~55日龄平均日增重显著下降,可能是因为提早断奶会加剧断奶应激,通过抑制羔羊免疫应答和消化功能减缓增重[22],试验中EW组羔羊20日龄断奶,42日龄停止饲喂代乳粉完全饲喂固体饲粮,产生了断代乳粉应激,虽早期断奶增加羔羊开食料采食量,但哺乳阶段与母羊分离、采食固体饲粮等应激限制了羔羊对固体饲粮消化能力[23],导致羔羊饲料转化效率低,抑制羔羊哺乳阶段的生长[24]。柴建民等[14]探究了适宜的断代乳粉时间,试验发现代乳粉饲喂时间长可能导致羔羊对代乳粉的依赖性增加,断代乳粉应激增大,但该阶段持续时间短(10 d),并未对2组羔羊体重造成显著差异。
本试验发现,早期断奶羔羊的增重优势体现在育肥前期(66~120日龄),羔羊出现补偿生长效应。Kamalzadeh等[25]试验发现营养限制阶段羔羊增重速度减缓,恢复正常营养水平饲粮后羔羊采食量和增重相比对照组显著增加,出现完全生长补偿。本试验中,早期断奶应激导致55日龄前羔羊饲料转化效率低,抑制增重,进入育肥期后断奶应激减缓至消失,66~120日龄阶段早期断奶羔羊采食量剧增,营养物质摄入量增加,造成66~120日龄阶段早期断奶羔羊平均日增重相比随母哺乳羔羊显著增加。进入育肥后期(121~180日龄阶段),早期断奶羔羊与随母哺乳羔羊在采食量、增重等方面均相似,说明补偿效应到育肥后期大大降低甚至消失。
综合分析生长性能数据后可知,早期断奶并补充代乳粉提高了羔羊哺乳阶段的采食量,但断奶应激的存在抑制了该阶段羔羊的生长;提高了羔羊育肥前期的采食量,同时促进了羔羊增重;对羔羊育肥后期生长性能无显著影响。
3.2 早期断奶并补饲代乳粉对羔羊营养物质消化率的持续影响研究表明,早期断奶羔羊由于补饲代乳粉,固体饲粮采食量增加,导致其与随母哺乳羔羊相比瘤胃重量、容积增加,瘤胃代谢能力增强[26-27],导致早期断奶羔羊消化系统与随母哺乳羔羊存在一定的差异。而随着瘤胃功能的完善,这种差异是否还存在,如何反映在各个生长阶段,有待于探究。表 3展示了3个生长阶段2组羔羊营养物质消化率的对比,在55~65日龄阶段2组羔羊瘤胃发育基本成熟,营养物质消化率相近,这与羔羊该阶段平均日增重的变化趋势一致,说明此阶段早期断奶应激减缓甚至消失,羔羊已适应固体饲粮饲喂方式。反刍动物摄入饲粮的中性洗涤纤维和酸性洗涤纤维含量是影响机体营养物质消化的关键因素,饲粮营养物质消化率与摄入的中性洗涤纤维和酸性洗涤纤维量呈负相关。66~120日龄阶段早期断奶羔羊采食量增加,而营养物质消化率2组羔羊一致,间接表明育肥前期早期断奶羔羊营养物质消化能力增强。柴建民等[14]的试验发现,早期断奶促进羔羊瘤胃发育,增加瘤胃微生物种类和数量,这便可以解释早期断奶羔羊在66~120日龄阶段平均日增重显著增加的现象,但早期断奶对瘤胃微生物的影响随日龄增加而减弱,本试验中2组羔羊育肥后期采食量相近,营养物质消化率并未出现显著差异。
3个生长阶段2组羔羊营养物质消化率无显著差异,说明55日龄后羔羊瘤胃发育基本成熟,早期断奶并补饲代乳粉对羔羊育肥期营养物质消化能力没有显著影响。
3.3 早期断奶并补饲代乳粉对羔羊血清生化指标的持续影响早期断奶羔羊与随母哺乳羔羊在各营养物质消化率上无显著差异,表明羔羊胃肠道消化饲粮的能力相似,消化是机体与外界环境交流互作的途径之一,那么营养物质吸收进入机体内环境后,其参与体内代谢、维持动物机体能氮平衡等情况是否相同仍需进行指标检测。血清UN含量与饲粮含氮量和动物机体代谢情况紧密相关,是评价动物机体蛋白质代谢和饲粮氨基酸平衡的指标[28]。本试验中,早期断奶羔羊65、120日龄血清UN含量高于随母哺乳羔羊。前人研究发现反刍动物血清UN含量与机体氮利用率成反比[29]。通常认为血清UN含量高于5~9 mg/dL可能是采食过多造成氮浪费,即氮摄入超量[29],本试验中早期断奶羔羊各日龄血清UN含量均高于5.8 mmol/L(16 mg/dL),原因可能是EW组羔羊65、120日龄采食量高于ER组羔羊,蛋白质摄入量增加,2组羔羊粗蛋白质消化率相近,导致血清UN含量增加。
GH、IGF-1是与生长有关的内分泌激素,本试验结果显示早期断奶羔羊65日龄血清GH含量显著高于随母哺乳羔羊,可能是断奶应激抑制了羔羊生长发育,65日龄时羔羊断奶应激虽减弱,但生长速度仍相对较慢,促使垂体分泌GH以缓解生长抑制。Mao等[30]的研究探究此种现象的机制时发现,生长速度慢的肉鸡血清GH含量高于生长速度快的肉鸡。早期断奶羔羊120日龄血清GH、IGF-1含量均显著高于随母哺乳羔羊,同时早期断奶羔羊100~120日龄平均日增重显著增加,表现出较好的生长性能,说明此时垂体分泌的GH量增加,作用靶器官相应受体促进IGF-1的产生。
本试验发现65日龄时2组羔羊血清GLU含量没有显著差异。Sowińska等[31]研究不同断奶日龄羔羊的断奶应激时发现50日龄断奶的羔羊断奶应激明显,饲粮中能量利用效率降低,导致血清GLU含量显著升高。根据本试验血清GLU含量的结果,可得出与羔羊生长性能变化类似的结论:EW组羔羊65日龄时断奶应激已减缓甚至消失。羔羊瘤胃组织氧化丁酸为BHBA,因此血清BHBA含量可反映瘤胃上皮代谢能力及发育情况。Deelen等[32]研究发现幼畜血清BHBA含量与采食量呈正相关,早期断奶羔羊在育肥后期血清BHBA含量显著低于随母哺乳羔羊,可能是育肥前期随母哺乳羔羊采食量低,而育肥后期采食量逐渐升高,致使血清BHBA含量显著增加,同时结合羔羊生长性能、消化情况可以发现早期断奶羔羊瘤胃丁酸代谢能力相比随母哺乳羔羊较弱。
3.4 早期断奶并补饲代乳粉对180日龄羔羊肉品质的影响羔羊肉品质的改善可有效增加羊肉的市场需求,提高养殖收益[33]。饲养管理和饲喂时间对羔羊肉品质产生不同程度的影响[34],随着饲养时间的增加,羔羊肉品质发生显著变化[35]。本研究中,早期断奶并补饲代乳粉对180日龄羔羊的屠宰率没有显著影响,同Belanche等[36]的研究结果一致。Lanza等[37]研究发现饲喂代乳粉组羔羊40日龄时羊肉不饱和脂肪酸比例高于饲喂母乳组。Ekiz等[38]研究了断奶时间对羔羊胴体品质的影响,试验发现45和75日龄断奶羔羊120日龄屠宰率、胴体重、胴体体尺等均低于随母哺乳羔羊(哺乳至120日龄),表现出较差的产肉性能。本试验结果与上述研究结果存在差异的原因可能是屠宰日龄的选择不同以及羔羊断奶后短时间内存在断奶应激、摄入营养物质不足等抑制生长因素,使得平均日增重降低,而进入育肥期后,相同且适宜的饲养环境使因断奶造成的增重差异缩小乃至消失。滴水损失率和熟肉率反映了肉的系水力,与羊肉风味紧密相关[39]。本试验中2组羔羊背最长肌的滴水损失率、熟肉率、眼肌面积及GR值均无显著差异,说明早期断奶并补饲代乳粉对180日龄羔羊肉品质没有产生显著影响,结合2组羔羊180日龄生长性能、营养物质消化率及血清生化指标均未发生显著变化可知,羔羊180日龄时由早期断奶产生的代谢印记已经消失。
4 结论早期断奶并补饲代乳粉提高了羔羊哺乳阶段(25~65日龄)的开食料采食量,产生的断奶应激抑制了羔羊生长,但随着羔羊日龄的增加,断奶应激逐渐减弱。早期断奶并补饲代乳粉提高了羔羊育肥前期(66~120日龄)的生长性能,但对羔羊育肥后期(121~180日龄)的生长性能、血清生化指标、消化性能及肉品质均没有显著影响,说明由早期断奶产生的代谢印记在育肥后期已经消失。
致谢:
感谢毕研亮老师全程指导屠宰试验,感谢师兄吕小康、赵国宏,师姐李文娟、周丽雪、王贝,同学郭伟在屠宰试验过程中提供的帮助。感谢山东临清润林牧业有限公司提供的良好的试验环境和生活环境,以及该公司员工给予的全力帮助。
| [1] |
CALDER P C, SUSANNE K E, DE JONG E C, et al. Early nutrition and immunity-progress and perspectives[J]. British Journal of Nutrition, 2006, 96(4): 774-790. |
| [2] |
HEGARTY R S, SHANDS C, MARCHANT R, et al. Effects of available nutrition and sire breeding values for growth and muscling on the development of crossbred lambs.1:growth and carcass characteristics[J]. Australian Journal of Agricultural Research, 2006, 57(6): 593-603. |
| [3] |
LUCAS A.Programming by early nutrition in man[M]//BOCK G R, WHELAN J.Ciba foundation symposium.London: Novartis Foundation Symposia, 1991, 156: 38-50.
|
| [4] |
SEFIDBAKHT N, FARID A. Effect of early weaning and hormone treatments on induction of estrus, conception and lambing of fall-lambing Karakul ewes[J]. Journal of Animal Science, 1977, 45(2): 311-319. |
| [5] |
柴建民.断母乳日龄对羔羊生长性能与胃肠道发育的影响[D].硕士学位论文.北京: 中国农业科学院, 2015. http://cdmd.cnki.com.cn/Article/CDMD-82101-1015379119.htm
|
| [6] |
EMSEN E, YAPRAK M, BILGIN O C, et al. Growth performance of Awassi lambs fed calf milk replacer[J]. Small Ruminant Research, 2004, 53(1/2): 99-102. |
| [7] |
SENA H D S, SANTOS K, SILVA M X, et al. Learning, memory and stress evaluation in lambs weaned at different ages[J]. Journal of Animal Science Advances, 2013, 3(9): 431-438. |
| [8] |
NAPOLITANO F, DE ROSA G, SEVI A. Welfare implications of artificial rearing and early weaning in sheep[J]. Applied Animal Behaviour Science, 2008, 110(1/2): 58-72. |
| [9] |
BHATT R S, TRIPATHI M K, VERMA D L, et al. Effect of different feeding regimes on pre-weaning growth rumen fermentation and its influence on post-weaning performance of lambs[J]. Journal of Animal Physiology and Animal Nutrition, 2010, 93(5): 568-576. |
| [10] |
张乃锋, 柴建民, 王世琴, 等. 早期补饲代乳粉对断奶后羔羊生长性能及体尺指标的影响[J]. 现代畜牧兽医, 2017(10): 1-6. |
| [11] |
SOBERON F, RAFFRENATO E, EVERETT R W, et al. Preweaning milk replacer intake and effects on long-term productivity of dairy calves[J]. Journal of Dairy Science, 2012, 95(2): 783-793. |
| [12] |
刘洁, 刁其玉, 赵一广, 等. 肉用绵羊饲料养分消化率和有效能预测模型的研究[J]. 畜牧兽医学报, 2012, 43(8): 1230-1238. |
| [13] |
祁敏丽, 马铁伟, 刁其玉, 等. 饲粮营养限制对断奶湖羊羔羊生长、屠宰性能以及器官发育的影响[J]. 畜牧兽医学报, 2016, 47(8): 1601-1609. |
| [14] |
柴建民, 王波, 祁敏丽, 等. 不同开食料采食量断液体饲粮对羔羊生长发育的影响[J]. 中国农业科学, 2018, 51(2): 341-350. |
| [15] |
张丽英. 饲料分析及饲料质量检测技术[M]. 2版. 北京: 中国农业大学出版社, 2003.
|
| [16] |
RAINERI C, STIVARI T S S, GAMEIRO A H. Lamb production costs:analyses of composition and elasticities analysis of lamb production costs[J]. Asian-Australasian Journal of Animal Sciences, 2015, 28(8): 1209-1215. |
| [17] |
陈丽佳. 广东农业先进适用技术评价指标体系研究[J]. 广东科技, 2009(16): 3-6. |
| [18] |
CHAI J M, DIAO Q Y, WANG H C, et al. Effects of weaning age on growth, nutrient digestibility and metabolism, and serum parameters in Hu lambs[J]. Animal Nutrition, 2015, 1(4): 344-348. |
| [19] |
LV X K, CHAI J M, DIAO Q Y, et al. The signature microbiota drive rumen function shifts in goat kids introduced to solid diet regimes[J]. Microorganisms, 2019, 7(11): 516. |
| [20] |
解彪, 张乃锋, 崔凯, 等. 早期断奶羔羊饲喂不同中性洗涤纤维水平饲粮对羔羊育肥期生长性能、血清学指标和屠宰性能的影响[J]. 动物营养学报, 2018, 30(6): 2172-2181. |
| [21] |
MOALLEM U, WERNER D, LEHRER H, et al. Long-term effects of ad libitum whole milk prior to weaning and prepubertal protein supplementation on skeletal growth rate and first-lactation milk production[J]. Journal of Dairy Science, 2010, 93(6): 2639-2650. |
| [22] |
VAN DER MEULEN J, KOOPMANS S J, DEKKER R A, et al. Increasing weaning age of piglets from 4 to 7 weeks reduces stress, increases post-weaning feed intake but does not improve intestinal functionality[J]. Animal:An International Journal of Animal Bioscience, 2010, 4(10): 1653-1661. |
| [23] |
ENRÍQUEZ D, HÖTZEL M J, UNGERFELD R. Minimising the stress of weaning of beef calves:a review[J]. Acta Veterinaria Scandinavica, 2011, 53(1): 28-35. |
| [24] |
BOSI P, GREMOKOLINI C, TREVISI P. Dietary regulations of the intestinal barrier function at weaning[J]. Asian-Australasian Journal of Animal Sciences, 2003, 16(4): 596-608. |
| [25] |
KAMALZADEH A, VAN BRUCHEM J, KOOPS W J, et al. Feed quality restriction and compensatory growth in growing sheep:feed intake, digestion, nitrogen balance and modelling changes in feed efficiency[J]. Livestock Production Science, 1997, 52(3): 209-217. |
| [26] |
ALI NOROUZIAN M, VALIZADEH R, VAHMANI P. Rumen development and growth of Balouchi lambs offered alfalfa hay pre- and post-weaning[J]. Tropical Animal Health and Production, 2011, 43(6): 1169-1174. |
| [27] |
KOSGEY I S, BAKER R L, UDO H M J, et al. Successes and failures of small ruminant breeding programmes in the tropics:a review[J]. Small Ruminant Research, 2006, 61(1): 13-28. |
| [28] |
WERNER M, HEPP C, SOTO C, et al. Effects of a long distance transport and subsequent recovery in recently weaned crossbred beef calves in Southern Chile[J]. Livestock Science, 2013, 152(1): 42-46. |
| [29] |
BLOME R M, DRACKLEY J K, MCKEITH F K, et al. Growth, nutrient utilization, and body composition of dairy calves fed milk replacers containing different amounts of protein[J]. Journal of Animal Science, 2003, 81(6): 1641-1655. |
| [30] |
MAO J N, BURNSIDE J, POSTEL-VINAY M C, et al. Ontogeny of growth hormone receptor gene expression in tissue of growth-selected strains of broiler chickens[J]. Journal of Endocrinology, 1998, 156(1): 67-75. |
| [31] |
SOWIŃSKA J, BRZOSTOWSKI H, TAŃSKI Z, et al. The weaning stress response in lambs of different age[J]. Czech Journal of Animal Science, 2001, 46(11): 465-468. |
| [32] |
DEELEN S M, LESLIE K E, STEELE M A, et al. Validation of a calf-side β-hydroxybutyrate test and its utility for estimation of starter intake in dairy calves around weaning[J]. Journal of Dairy Science, 2016, 99(9): 7624-7633. |
| [33] |
MORTIMER S I, VAN DER WERF J H J, JACOB R H, et al. Genetic parameters for meat quality traits of Australian lamb meat[J]. Meat Science, 2014, 96(2): 1016-1024. |
| [34] |
BISPO E, MORENO T, THOMAS A, et al. Effects of weaning and finishing feeding treatment on fatty acids, especially cis and trans C18 : 1 isomers, in the longissimus thoracis muscle of Galician Blond calves[J]. Animal, 2011, 5(5): 802-812. |
| [35] |
侯鹏霞.滩羊羔羊早期补饲以及不同体重阶段羊肉品质的研究[D].硕士学位论文.银川: 宁夏大学, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10749-1014226550.htm
|
| [36] |
BELANCHE A, COOKE J, JONES E, et al. Short-and long-term effects of conventional and artificial rearing strategies on the health and performance of growing lambs[J]. Animal, 2019, 13(4): 740-749. |
| [37] |
LANZA M, BELLA M, PRIOLO A, et al. Lamb meat quality as affected by a natural or artificial milk feeding regime[J]. Meat Science, 2006, 73(2): 313-318. |
| [38] |
EKIZ B, KOCAK O, YALCINTAN H, et al. Effects of suckling duration on growth, slaughtering and carcass quality characteristics of Kivircik lambs[J]. Tropical Animal Health and Production, 2015, 48(2): 395-401. |
| [39] |
AGUAYO-ULLOA L A, LA LAMA G C M D, PASCUAL-ALONSO M, et al. Effect of feeding regime during finishing on lamb welfare, production performance and meat quality[J]. Small Ruminant Research, 2013, 111(1/2/3): 147-156. |




