2. 中国农业大学动物科技学院, 动物营养学国家重点实验室, 北京 100193
2. State Key Laboratory of Animal Nutrition, College of Animal Science and Technology, China Agricultural University, Beijing 100193, China
据报道,全球范围内反刍动物每年的甲烷排放量为100万t左右,约占全球甲烷排放总量的20%,对全球气候变暖具有很大威胁[1]。此外,反刍动物甲烷排放会造成饲料能量的浪费,降低饲料转化效率[2]。近年来,体内和体外的试验研究均发现不同种类的硝基化合物具有高效的甲烷抑制作用[3-7],而且硝基化合物还能够抑制沙门氏菌、大肠杆菌和幽门弯曲杆菌等多种病原菌[8]。
虽然硝基化合物能够通过降低反刍动物甲烷排放和抑制病原菌而对畜牧业生产和环境保护具有重要意义,但是黄芪、冠花、木兰属等牧草植物由于含有硝基化合物而引起动物不同程度的中毒。Anderson等[9]综述了含有3-硝基丙醇和3-硝基丙酸的牧草植物对家畜的毒性及其代谢的研究,发现硝基毒素能够不可逆地抑制琥珀酸脱氢酶而阻碍动物机体的能量(ATP)合成。但是瘤胃微生物能够代谢转化这些硝基毒素而达到脱毒作用,这为硝基化合物在反刍动物甲烷减排方面的实践应用提供了理论基础。此外,目前关于化学工业合成的硝基化合物(包括硝基烷烃、硝氧基化合物、芳香族硝基化合物等)的代谢脱毒研究资料较少。本文主要介绍了硝基化合物的分类,并综述了硝基化合物的毒性及其在动物机体的代谢脱毒机制研究进展。
1 硝基化合物硝基化合物是指化学结构中含有硝基官能团的化合物,即烃分子中的氢原子被硝基官能团取代生成的衍生物[10]。硝基化合物的化学结构式为R-NO2,R为芳香烃或脂肪烃,硝基基团与碳原子以共价键结合,由于硝基基团为强吸电子基团,通常使其相连的α碳原子的氢原子解离为H+而具有酸性[8]。硝基化合物是极性化合物,一般为无色或淡黄色液体,微溶于水,可用作医药、染料、香料、炸药等工业的化工原料及有机合成试剂[8]。
1.1 硝基烷烃硝基烷烃是指烷烃的氢原子被硝基官能团取代后生成的化合物,一般不存在天然的生物合成的硝基烷烃,多为化学工业合成途径制得[8]。硝基烷烃在工业生产中有多种用途:药品和农药的合成,油漆和涂料的交联剂,卤代烃的稳定剂以及电路板的清洗剂[8]。目前,较为常见的硝基烷烃多为短链硝基烷烃,如硝基甲烷、硝基乙烷、1-硝基丙烷和2-硝基丙烷等。
近年来,研究硝基乙烷具有较强的甲烷抑制作用,受到人们的关注。Anderson等[11]、Gutierrez-Bañuelos等[12]、Božic等[13]、Zhou等[14]以及Zhang等[15]研究发现,硝基乙烷的甲烷抑制效率高达90%以上(表 1)。
|
|
表 1 体外培养条件下硝基化合物对甲烷生成的影响 Table 1 Effects of nitrocompounds on methane production under in vitro culture condition |
硝基烷烃取代物主要包括硝基醇和硝基酸类化合物,即直链或支链碳链烷烃主链上含有硝基和1个羟基或羧基官能团的化合物。目前研究较多的硝基烷烃取代物主要包括硝基乙醇、硝基丙醇以及硝基丙酸。
硝基乙醇,其化学结构式为HO-CH2-CH2-NO2,浅黄色液体,其密度为1.27 g/mL,熔点和沸点均不高。Anderson等[11]发现,在100% CO2培养条件下,硝基乙醇的体外甲烷抑制效率高达95%。此外,Zhang等[15]研究发现,硝基乙醇能够通过抑制瘤胃产甲烷菌以及甲烷生成所需的辅酶而抑制甲烷的生成,抑制效率在90%以上。
硝基丙醇包括2-硝基丙醇和和3-硝基丙醇,其化学结构式如图 1所示,均为淡黄色液体,有轻微的刺鼻性气味,密度为1.185 g/mL。2-硝基丙醇多为化学合成,而3-硝基丙醇存在于黄芪、冠花、木蓝属等植物中。硝基丙醇的甲烷抑制效率在60%~90%[10, 14]。
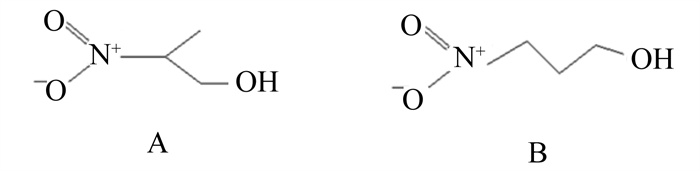
|
图 1 2-硝基丙醇(A)和3-硝基丙醇(B)的结构式 Fig. 1 Structural formula of 2-nitropropanol (A) and 3-nitropropanol (B) |
硝基丙酸,较多研究的是3-硝基丙酸,为白色结晶化合物,其化学结构式为HOOC-CH2-CH2-CH2-NO2,密度为1.673 g/mL,溶于水、乙醇、乙酸乙酯及其他部分有机溶剂。3-硝基丙酸也存在于发红的甘蔗、黄芪属和冠花属等牧草植物中(表 2)[9]。此外,3-硝基丙酸是曲霉属和青霉属的少数菌种产生的有毒代谢产物。天然的3-硝基丙酸和3-硝基丙醇在牧草植物中通常以单体、二或三体糖甙或糖酯类共轭化合物形式存在,但二者不能同时存在于同一种牧草植物中[9]。这些天然的3-硝基丙酸和3-硝基丙醇植物代谢物既能够抑制瘤胃内产甲烷菌的活性,还可以抑制一些病原菌(如沙门氏菌、大肠杆菌和弯曲杆菌等)[8]。
|
|
表 2 含有3-硝基丙酸的牧草及其位置 Table 2 Forage source containing 3-nitropropionic acid and its position[9] |
目前关于硝氧基化合物研究较多的是3-硝基酯-1-丙醇(3-NOP)。3-硝基酯-1-丙醇是无色液体,呈现弱碱性,密度为1.19 g/mL,是一种甲基辅酶M类似物[1]。在瘤胃发酵生成甲烷的过程中需要多种酶的参与,其中甲基辅酶M是甲烷生成的重要辅酶,而3-硝基酯-1-丙醇作为甲基辅酶M类似物,能够替代甲基辅酶M结合辅酶B,从而减少甲基辅酶M还原生成的甲烷[16]。Soliva等[17]通过体外连续培养试验对比研究了3-硝基酯-1-丙醇和溴乙烷磺酸对瘤胃发酵甲烷生成的影响,结果发现3-硝基酯-1-丙醇同溴乙烷磺酸一样,能够通过抑制甲基辅酶M而显著降低甲烷生成。Martínez-Fernández等[18]在绵羊饲粮中添加100 mg/d的3-硝基酯-1-丙醇,显著降低了绵羊瘤胃发酵甲烷的生成量(高达23.7%)。Reynolds等[19]研究发现,通过瘤胃瘘管直接向瘤胃内投喂500或2 500 mg/d的3-硝基酯-1-丙醇使泌乳奶牛的甲烷产量分别降低了6.6%和9.8%。而Haisan等[20]在泌乳奶牛饲粮中添加2 500 mg/d的3-硝基酯-1-丙醇,能够通过降低瘤胃内甲烷菌的数量(2.69×108个/mL减少为0.95×108个/mL)而使泌乳奶牛的甲烷产量从17.8 g/kg DMI降至7.18 g/kg DMI。Hristov等[21]在荷斯坦奶牛饲粮中添加40~80 mg/kg DM 3-硝基酯-1-丙醇,通过12周的饲养试验发现荷斯坦奶牛的甲烷排放量减少了40%。对于肉牛,Romero-Perez等[22]指出,安格斯肉牛的甲烷排放量随饲粮3-硝基酯-1-丙醇添加水平的提高而呈线性下降。此外,Vyas等[5]对比研究了莫能菌素和3-硝基酯-1-丙醇对杂交阉牛甲烷排放的影响,结果发现,3-硝基酯-1-丙醇显著降低了肉牛甲烷排放量(高达40%),且提高了肉牛的饲料转化效率。
此外,关于3-硝基酯-1-丙醇的衍生物3-硝基乙酯丙酸和2, 2-二甲基-3-(硝氧基)丙酸的作用也有研究,这些硝氧基衍生物均具有降低瘤胃发酵甲烷生成的作用[16]。
1.4 芳香族硝基化合物芳香族硝基化合物是指硝基基团直接与芳香环相连的化合物,其结构式为Ar-NO2,Ar为芳香烃。芳香族硝基化合物为无色或淡黄色高沸点液体或低熔点固体,不溶于水,有剧毒。芳香族硝基化合物常作为生产炸药和油漆的原料。其生物活性包括抗菌、对动物机体和细胞有毒性。此外,Jin等[23]通过体外发酵试验发现,芳香族硝基化合物的衍生物N-[2-(硝氧基)乙基]-3-吡啶甲酰胺(330.0 μmol/L)能够抑制瘤胃发酵甲烷的生成,抑制率达90.4%。
2 硝基化合物的毒性及其代谢脱毒 2.1 硝基化合物的毒性在20世纪早期,Marsh等[24]首次发现植物中含有硝基毒素。Stermitz等[25]在长叶黄芪中首次分离鉴定出含有3-硝基丙醇的糖甙化合物和含有3-硝基丙酸的葡萄糖酯类,这些糖甙类和糖酯类化合物被认为是硝基毒素。紧接着,大量的黄芪和冠花类牧草植物中也相继被发现含有3-硝基丙醇或3-硝基丙酸的糖甙和糖酯类硝基毒素。含有3-硝基丙醇的糖甙化合物通常被称为米瑟毒甙(miserotoxin),而含有3-硝基丙酸糖酯类结合物被称为狗角藤毒甙(karakin)。属牧草植物木本黄芪(Astragalus miser var. serotinus)中的硝基毒素多为米瑟毒甙,其含量为植物干物质含量的2%~6%,1头500 kg的牛需采食3~9 kg的新鲜黄芪属牧草植物才会引起中毒[26]。与3-硝基丙醇相比,3-硝基丙酸的毒性更强,但由于大部分含有3-硝基丙醇的牧草植物中硝基毒素含量较高,一般为3-硝基丙酸牧草植物的2倍,因此含有3-硝基丙醇的牧草植物与含有3-硝基丙酸的牧草植物的硝基毒性相当[9]。此外,牧草植物的硝基毒素含量受到日照时间、环境湿度、温度以及生长季节的影响[9]。
研究表明,硝基毒素会引起不同动物(鸡、鼠、猪、兔等)机体的中毒[27](表 3)。此外,给牛、羊直接静脉注射3-硝基丙醇,其半数致死量(LD50)分别为30和52 mg/kg BW[24](表 3),而给牛、羊经口灌服3-硝基丙醇时,其半数致死量分别增加至57和118 mg/kg BW[28](表 3)。此外,与糖疳和糖酯类的米瑟毒甙或狗角藤毒甙相比,3-硝基丙醇的直接毒性更强,其对大鼠的半数致死量分别为2 500和77 mg/kg BW[29]。而且急性、高剂量的硝基毒性可能会引起大量的亚硝酸盐产生,进而引起高铁血红蛋白症。但是截至目前,3-硝基丙醇和3-硝基丙酸的中毒机制尚不完全明确,研究发现其对生物体内一些重要的酶系统如琥珀酸脱氢酶、过氧化氢酶、谷氨酸脱羧酶、单胺氧化酶等均有不同程度的抑制和失活,进而阻碍了三羧酸循环的进行,最终导致动物组织器官的损害[9]。
|
|
表 3 部分硝基化合物的半数致死量 Table 3 LD50 of some nitrocompounds |
其他烷烃类硝基化合物(如硝基乙烷)及其衍生物(如硝基乙醇、硝基丙醇、硝基丙酸)和硝氧基化合物(如3-硝基酯-1-丙醇)多为化学工业合成的产物,近年来被认为具有高效的甲烷抑制作用[15, 21, 30]。这些硝基化合物一般对瘤胃产甲烷菌具有显著的抑制作用,对于其他瘤胃微生物的毒性作用较小(表 2)。Anderson等[31]通过饲养试验发现,饲粮添加72和120 mg/kg BW的硝基乙烷和2-硝基丙醇只显著降低了绵羊的瘤胃产甲烷活性,而对瘤胃VFA没有显著影响,这说明硝基乙烷和2-硝基丙醇对瘤胃微生物的发酵没有明显的毒性作用。Zhang等[7]对比研究了饲粮添加硝基乙醇和莫能菌素对育肥羔羊生长性能和产甲烷活性的影响,结果发现硝基乙醇更能够通过降低瘤胃发酵甲烷的生成而提高育肥羔羊的饲料转化效率。Vyas等[5]通过莫能菌素和3-硝基酯-1-丙醇的对比饲养试验发现,3-硝基酯-1-丙醇能够显著降低杂交阉牛的甲烷排放(40%)而提高肉牛的饲料转化效率。此外,这2个体内研究均未报道动物机体的中毒症状,这说明硝基乙醇和3-硝基酯-1-丙醇的硝基毒性对于反刍动物的生长性能可能没有负面作用。
芳香族硝基化合物的硝基基团能够被细菌或动物机体内的酶类(NADPH: 细胞色素P450还原酶、NADP+铁氧还原蛋白还原酶等)还原,而引起细菌、细胞和动物机体的氧化应激[8]。
2.2 硝基化合物的代谢转化与脱毒研究表明,给反刍动物静脉注射或经口灌服3-硝基丙醇时,硝基毒素的致死量不同:静脉注射时,3-硝基丙醇对牛、羊的致死量分别为30和52 mg/kg BW[26];经口灌服时,3-硝基丙醇对牛、羊的致死量则分别显著增加到57和118 mg/kg BW[28],这表明瘤胃微生物确实具有代谢硝基化合物的能力,硝基毒素能够被硝基代谢细菌所降解利用而达到脱毒作用。Majak等[32]通过严格厌氧技术,在瘤胃液中分离鉴定出10种能够代谢硝基化合物的微生物:栖瘤胃拟杆菌(Bacteriodes ruminicola)、脱硫弧菌(Desulfovibrio desulfuricans)、埃氏巨型球菌(Megasphaera elsdenii)、反刍月形单胞菌(Selenomonas ruminantium)、产碱韦荣菌(Veillonella alcalescens)、梭菌属(Clostridium)、粪球菌属(Coprococcus)、乳杆菌属(Lactobacillus)、枝杆菌属(Ramibacterium)和消化链球菌属(Peptostreptococcus)。此外,这些硝基毒素代谢微生物也被发现具有代谢亚硝酸盐的能力。
2.2.1 硝基丙醇和硝基丙酸的代谢脱毒关于硝基毒素代谢的研究最先起于牧草植物中的天然硝基化合物,即含有3-硝基丙醇的米瑟毒甙和含有3-硝基丙酸的狗角藤毒甙等(图 2)。由于反刍动物瘤胃内栖息着大量微生物,具有降解代谢硝基毒素的作用。瘤胃微生物通过分泌β-葡萄糖苷酶和酯酶将米瑟毒甙、狗角藤毒甙等水解释放出3-硝基丙醇和3-硝基丙酸。其中,一小部分3-硝基丙醇和3-硝基丙酸被瘤胃上皮吸收进入血液循环,而大部分3-硝基丙醇和3-硝基丙酸被瘤胃微生物代谢生成3-氨基丙醇和β-丙氨酸。然后,β-丙氨酸能够被瘤胃微生物进一步代谢利用,而3-氨基丙醇在瘤胃内的进一步代谢目前还没有明确结论[9]。此外,Majak等[32]指出,瘤胃微生物在降解代谢3-硝基丙醇和3-硝基丙酸的脱毒过程中会伴随有亚硝酸盐的生成,而亚硝酸盐作为中间代谢产物进一步被瘤胃微生物代谢还原生成氨而被利用。Zhang等[33]的体外批次发酵试验也同样证明,硝基乙烷、硝基乙醇和2-硝基丙醇在体外瘤胃微生物的代谢过程中确实存在亚硝酸盐的生成。瘤胃微生物对硝基毒素和亚硝酸盐的代谢速率排序为:3-硝基丙酸>3-硝基丙醇>亚硝酸盐,而且瘤胃微生物对硝基毒素的代谢脱毒需要严格的厌氧环境[30]。
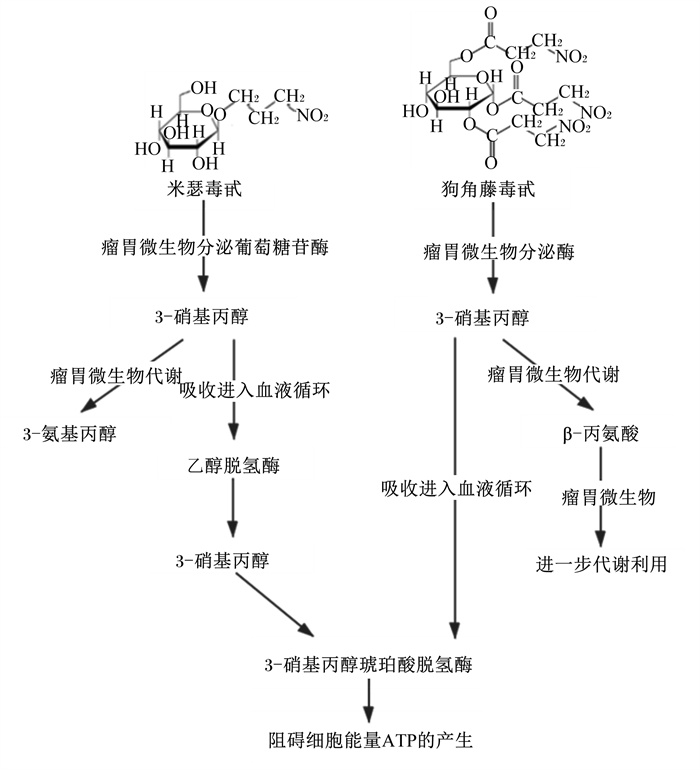
|
图 2 牧草植物在反刍动物瘤胃内的硝基毒素代谢 Fig. 2 Metabolism of nitrotoxin form forage in ruminants[9] |
截止目前,脱毒脱氮杆菌(Denitrobacterium detoxificans)是唯一鉴定分离的具有专性代谢硝基化合物的瘤胃细菌[34]。正常情况下,反刍动物瘤胃内含有Denitrobacterium detoxificans约103个/mL,添加硝基化合物能够显著促进瘤胃内Denitrobacterium detoxificans的富集增长。Anderson等[34]在严格厌氧条件下纯培养了Denitrobacterium detoxificans,并在培养液中添加3-硝基丙酸和3-硝基丙醇,培养结束后通过液相高效色谱法测定到3-硝基丙酸和3-硝基丙醇的代谢产物——β-丙氨酸和3-氨基-丙醇,以及少量的亚硝酸盐。Ochoa-García等[6]在最近的研究中同样发现,3-硝基丙酸在体外瘤胃培养液的代谢产物是β-丙氨酸。
对于非反刍动物,3-硝基丙酸能够被前段消化道分泌的酯酶水解代谢,由于3-硝基丙酸在前段消化道的快速吸收,进而阻断了3-硝基丙酸在后段消化道微生物的代谢分解[9]。此外,非反刍动物体内缺少水解米瑟毒甙、狗角藤毒甙的β-葡萄糖苷酶和酯酶,这导致了牧草植物的米瑟毒甙和狗角藤毒甙对非反刍动物的毒性比3-硝基丙酸的毒性较弱[9]。但是,3-硝基丙醇和2-硝基丙醇除瘤胃微生物代谢途径外,还存在乙醇脱氢酶途径将硝基丙醇和硝基乙醇代谢生成丙烯醛和亚硝酸盐,丙烯醛是一种与蛋白质或其他单分子共价结合的不稳定亲电体[8]。
2.2.2 硝基烷烃的代谢脱毒目前,硝基烷烃的代谢脱毒机制研究资料较少。但是Gutierrez-Bañuelos等[12]通过体外发酵试验发现,添加硝基乙烷能够显著增加Denitrobacterium detoxificans的数量(高达1 000倍),说明Denitrobacterium detoxificans可能具有降解代谢硝基乙烷的作用。在反刍动物体内,硝基乙烷的代谢脱毒可能与硝基丙醇和硝基丙酸的代谢脱毒过程一样,硝基乙烷被瘤胃微生物主要代谢生成乙胺(ethylamine)以及少量亚硝酸盐[34],但是目前还没有关于瘤胃微生物对硝基乙烷降解代谢产物的鉴定检测。Machle等[35]给兔静脉注射或经口灌服硝基乙烷,结果只检测到17%~19%的硝基乙烷回收率,这说明硝基乙烷能够被动物机体代谢。Scott[36-37]研究发现,硝基乙烷能够在血液中生成乙醛和亚硝酸盐,但是亚硝酸盐的生成量很少,并能迅速氧化生成硝酸盐。乙醛则被乙醛脱氢酶水解生成乙酸进入三羧酸循环(图 3)。
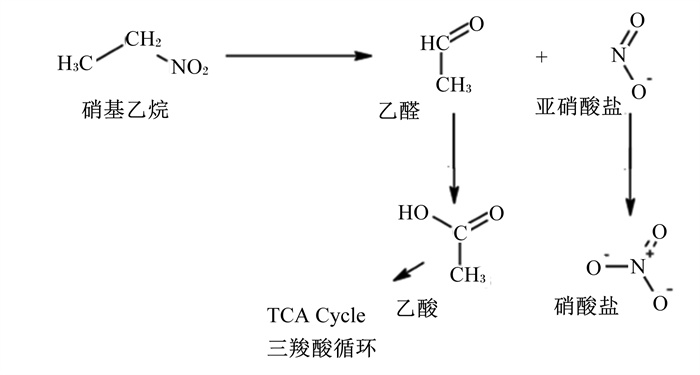
|
图 3 硝基乙烷在兔体内的代谢 Fig. 3 Metabolism of nitroethane in rabbits[8] |
芳香族硝基化合物的代谢是由NAD(P)H:硝基还原酶系统完成,芳香族硝基化合物通过生成中间体亚硝基化合物而进一步代谢生成羟胺化合物[38]。目前尚未有芳香族硝基化合物在反刍动物瘤胃内的代谢研究。此外,硝氧基化合物,主要是3-硝基酯-1-丙醇的动物饲养试验表明,3-硝基酯-1-丙醇能够抑制瘤胃产甲烷菌的活性,进而减少反刍动物的甲烷排放,但是3-硝基酯-1-丙醇对瘤胃总细菌和总原虫数量没有显著影响[20]。此外,Martínez-Fernández等[18]和Romero-Perez等[22]报道,3-硝基酯-1-丙醇对绵羊和肉牛的瘤胃微生物区系也没有显著影响。这些体内研究发现,3-硝基酯-1-丙醇主要作为甲基辅酶M的替代物而对瘤胃产甲烷菌具有专性抑制作用,但是对其他瘤胃微生物以及动物健康都没有不利影响,这间接说明3-硝基酯-1-丙醇的硝基毒性较低,可能能够被瘤胃微生物降解代谢。但是目前关于3-硝基酯-1-丙醇的代谢研究资料确实较少,将来应该给予更多关注。
综上所述,反刍动物瘤胃微生物对硝基化合物的代谢脱毒机制可能是:栖息在瘤胃内的Denitrobacterium detoxificans等细菌,通过氧化H2、甲酸或少量乳酸获得能量以供自身生长,同时将作为电子受体的硝基化合物还原为各自的胺类(如3-硝基丙酸→β-丙氨酸、3-硝基丙醇→3-氨基丙醇、2-硝基丙醇→2-氨基丙醇和硝基乙醇→氨基乙醇)以及少量亚硝酸盐,这些胺类和亚硝酸盐进一步被瘤胃微生物降解利用而达到脱毒效果。
3 小结综上所述,硝基化合物可以具体划分为硝基烷烃、硝基烷烃衍生物(硝基醇、硝基酸)、硝氧基化合物以及芳香族硝基化合物。无论是牧草植物含有的天然硝基化合物还是化学工业合成的硝基化合物,均能够高效抑制瘤胃发酵甲烷的生成,但硝基化合物含有的硝基毒素同时会引起动物机体不同程度的中毒。而瘤胃微生物具有代谢转化硝基毒素的能力,能够降解硝基化合物生成各自的胺类物质及少量亚硝酸盐,这些代谢产物能够被反刍动物瘤胃微生物进一步代谢利用而达到脱毒作用。但目前相关反刍动物瘤胃微生物对于硝基化合物代谢转化过程及其最终代谢产物的研究资料较少,需要研究学者做进一步的深入研究。
| [1] |
DUIN E C, WAGNER T, SHIMA S, et al. Mode of action uncovered for the specific reduction of methane emissions from ruminants by the small molecule 3-nitrooxypropanol[J]. Proceedings of the National Academy of Sciences of the United States of America, 2016, 113(22): 6172-6177. DOI:10.1073/pnas.1600298113 |
| [2] |
LLONCH P, HASKELL M J, DEWHURST R J, et al. Current available strategies to mitigate greenhouse gas emissions in livestock systems: an animal welfare perspective[J]. Animal, 2017, 11(2): 274-284. DOI:10.1017/S1751731116001440 |
| [3] |
ANDERSON R C, HUWE J K, SMITH D J, et al. Effect of nitroethane, dimethyl-2-nitroglutarate and 2-nitro-methyl-propionate on ruminal methane production and hydrogen balance in vitro[J]. Bioresource Technology, 2010, 101(14): 5345-5349. DOI:10.1016/j.biortech.2009.11.108 |
| [4] |
ANDERSON R C, RASMUSSEN M A. Use of a novel nitrotoxin metabolizing bacterium to reduce ruminal methane production[J]. Bioresource Technology, 1998, 64(2): 89-95. DOI:10.1016/S0960-8524(97)00184-3 |
| [5] |
VYAS D, MCGINN S M, DUVAL S M, et al. Optimal dose of 3-nitrooxypropanol for decreasing enteric methane emissions from beef cattle fed high-forage and high-grain diets[J]. Animal Production Science, 2016, 58(6): 1049-1055. |
| [6] |
OCHOA-GARCÍA P A, AREVALOS-SÁNCHEZ M M, RUIZ-BARRERA O, et al. In vitro reduction of methane production by 3-nitro-1-propionic acid is dose-dependent1[J]. Journal of Animal Science, 2019, 97(3): 1317-1324. DOI:10.1093/jas/skz012 |
| [7] |
ZHANG Z W, WANG Y L, CHEN Y Y, et al. Nitroethanol in comparison with monensin exhibits greater feed efficiency through inhibiting rumen methanogenesis more efficiently and persistently in feedlotting lambs[J]. Animals, 2019, 9(10): 784. DOI:10.3390/ani9100784 |
| [8] |
SMITH D J, ANDERSON R C. Toxicity and metabolism of nitroalkanes and substituted nitroalkanes[J]. Journal of Agricultural and Food Chemistry, 2013, 61(4): 763-779. DOI:10.1021/jf3039583 |
| [9] |
ANDERSON R C, MAJAK W, RASSMUSSEN M A, et al. Toxicity and metabolism of the conjugates of 3-nitropropanol and 3-nitropropionic acid in forages poisonous to livestock[J]. Journal of Agricultural and Food Chemistry, 2005, 53(6): 2344-2350. DOI:10.1021/jf040392j |
| [10] |
张振威, 王彦芦, 赵宇琼, 等. 硝基化合物抑制瘤胃发酵甲烷生成的机理研究进展[J]. 中国畜牧杂志, 2017, 53(3): 3-8. ZHANG Z W, WANG Y L, ZHAO Y Q, et al. Research progress on inhibition of the effects of nitro-compounds on methane production from rumen fermentation and its mechanism[J]. Chinese Journal of Animal Science, 2017, 53(3): 3-8 (in Chinese). |
| [11] |
ANDERSON R C, CALLAWAY T R, VAN KESSEL J A S, et al. Effect of select nitrocompounds on ruminal fermentation; an initial look at their potential to reduce economic and environmental costs associated with ruminal methanogenesis[J]. Bioresource Technology, 2003, 90(1): 59-63. DOI:10.1016/S0960-8524(03)00086-5 |
| [12] |
GUTIERREZ-BAÑUELOS H, ANDERSON R C, CARSTENS G E, et al. Effects of nitroethane and monensin on ruminal fluid fermentation characteristics and nitrocompound-metabolizing bacterial populations[J]. Journal of Agricultural and Food Chemistry, 2008, 56(12): 4650-4658. DOI:10.1021/jf800756c |
| [13] |
BOŽIC A K, ANDERSON R C, CARSTENS G E, et al. Effects of the methane-inhibitors nitrate, nitroethane, lauric acid, Lauricidin® and the Hawaiian marine algae Chaetoceros on ruminal fermentation in vitro[J]. Bioresource Technology, 2009, 100(17): 4017-4025. DOI:10.1016/j.biortech.2008.12.061 |
| [14] |
ZHOU Z M, MENG Q X, YU Z T. Effects of methanogenic inhibitors on methane production and abundances of methanogens and cellulolytic bacteria in in vitro ruminal cultures[J]. Applied and Environmental Microbiology, 2011, 77(8): 2634-2639. DOI:10.1128/AEM.02779-10 |
| [15] |
ZHANG Z W, WANG Y L, WANG W K, et al. The inhibitory action mode of nitrocompounds on in vitro rumen methanogenesis: a comparison of nitroethane, 2-nitroethanol and 2-nitro-1-propanol[J]. The Journal of Agricultural Science, 2019, 157(6): 471-479. DOI:10.1017/S0021859619000868 |
| [16] |
ZHANG Z W, CAO Z J, WANG Y L, et al. Nitrocompounds as potential methanogenic inhibitors in ruminant animals: a review[J]. Animal Feed Science and Technology, 2017, 236: 107-114. |
| [17] |
SOLIVA C R, AMELCHANKA S L, DUVAL S M, et al. Ruminal methane inhibition potential of various pure compounds in comparison with garlic oil as determined with a rumen simulation technique (Rusitec)[J]. The British Journal of Nutrition, 2011, 106(1): 114-122. DOI:10.1017/S0007114510005684 |
| [18] |
MARTÍNEZ-FERNÁNDEZ G, ABECIA L, ARCO A, et al. Effects of ethyl-3-nitrooxy propionate and 3-nitrooxypropanol on ruminal fermentation, microbial abundance, and methane emissions in sheep[J]. Journal of Dairy Science, 2014, 97(6): 3790-3799. DOI:10.3168/jds.2013-7398 |
| [19] |
REYNOLDS C K, HUMPHRIES D J, KIRTON P, et al. Effects of 3-nitrooxypropanol on methane emission, digestion, and energy and nitrogen balance of lactating dairy cows[J]. Journal of Dairy Science, 2014, 97(6): 3777-3789. DOI:10.3168/jds.2013-7397 |
| [20] |
HAISAN J, SUN Y, GUAN L L, et al. The effects of feeding 3-nitrooxypropanol on methane emissions and productivity of Holstein cows in mid lactation[J]. Journal of Dairy Science, 2014, 97(5): 3110-3119. DOI:10.3168/jds.2013-7834 |
| [21] |
HRISTOV A N, OH J, GIALLONGO F, et al. An inhibitor persistently decreased enteric methane emission from dairy cows with no negative effect on milk production[J]. Proceedings of the National Academy of Sciences of the United States of America, 2015, 112(34): 10663-10668. DOI:10.1073/pnas.1504124112 |
| [22] |
ROMERO-PEREZ A, OKINE E K, MCGINN S M, et al. The potential of 3-nitrooxypropanol to lower enteric methane emissions from beef cattle[J]. Journal of Animal Science, 2014, 92(10): 4682-4693. DOI:10.2527/jas.2014-7573 |
| [23] |
JIN W, MENG Z X, WANG J, et al. Effect of nitrooxy compounds with different molecular structures on the rumen methanogenesis, metabolic profile, and methanogenic community[J]. Current Microbiology, 2017, 74(8): 891-898. DOI:10.1007/s00284-017-1261-7 |
| [24] |
MARSH C D, CLAWSON A B. Astragalus tetrapterus, a new poisonous plant of Utah and Nevada[M]. Washington, D.C.: U.S. Dept. of Agriculture, 1920.
|
| [25] |
STERMITZ F R, NORRIS F A, WILLIAMS M C. Miserotoxin, new naturally occurring nitro compound[J]. Journal of the American Chemical Society, 1969, 91(16): 4599-4600. DOI:10.1021/ja01044a078 |
| [26] |
JAMES L F, HARTLEY W J, WILLIAMS M C, et al. Field and experimental studies in cattle and sheep poisoned by nitro-bearing Astragalus or their toxins[J]. American Journal of Veterinary Research, 1980, 41(3): 377-382. |
| [27] |
GREGORY N G, ORBELL G M, HARDING D R. Poisoning with 3-nitropropionic acid in possums (Trichosurus vulpecula)[J]. New Zealand Veterinary Journal, 2000, 48(3): 85-87. DOI:10.1080/00480169.2000.36166 |
| [28] |
GUSTINE D L. Aliphatic nitro compounds in crownvetch: a review[J]. Crop Science, 1979, 19(2): 197-203. DOI:10.2135/cropsci1979.0011183X001900020007x |
| [29] |
MAJAK W, PASS M A, MADRYGA F J. Toxicity of miserotoxin and its aglycone (3-nitropropanol) to rats[J]. Toxicology Letters, 1983, 19(1/2): 171-178. |
| [30] |
ANDERSON R C, KRUEGER N A, STANTON T B, et al. Effects of select nitrocompounds on in vitro ruminal fermentation during conditions of limiting or excess added reductant[J]. Bioresource Technology, 2008, 99(18): 8655-8661. DOI:10.1016/j.biortech.2008.04.064 |
| [31] |
ANDERSON R C, CARSTENS G E, MILLER R K, et al. Effect of oral nitroethane and 2-nitropropanol administration on methane-producing activity and volatile fatty acid production in the ovine rumen[J]. Bioresource Technology, 2006, 97(18): 2421-2426. DOI:10.1016/j.biortech.2005.10.013 |
| [32] |
MAJAK W, CHENG K J. Identification of rumen bacteria that anaerobically degrade aliphatic nitrotoxins[J]. Canadian Journal of Microbiology, 1981, 27(7): 646-650. DOI:10.1139/m81-099 |
| [33] |
ZHANG Z W, WANG Y L, WANG W K, et al. The antimethanogenic nitrocompounds can be cleaved into nitrite by rumen microorganisms: a comparison of nitroethane, 2-nitroethanol, and 2-nitro-1-propanol[J]. Metabolites, 2019, 10(1): 15. DOI:10.3390/metabo10010015 |
| [34] |
ANDERSON R C, RASMUSSEN M A, ALLISON M J. Metabolism of the plant toxins nitropropionic acid and nitropropanol by ruminal microorganisms[J]. Applied and Environmental Microbiology, 1993, 59(9): 3056-3061. DOI:10.1128/aem.59.9.3056-3061.1993 |
| [35] |
MACHLE W, SCOTT E W, TREON J F. Metabolism of mononitroparaffins: recovery of nitroethane from animal organism[J]. The Journal of Industrial Hygiene and Toxicology, 1942, 24: 5-9. |
| [36] |
SCOTT E W. The metabolism of mononitroparaffins. Ⅱ. The metabolic products of nitroethane[J]. The Journal of Industrial Hygiene and Toxicology, 1942, 24: 226-228. |
| [37] |
SCOTT E W. The metabolism of mononitroparaffins.Ⅲ.The concentration of nitroethane, nitrite and nitrate in the blood of rabbits during exposure by inhalation and oral administration[J]. The Journal of Industrial Hygiene and Toxicology, 1943, 25: 20-25. |
| [38] |
VALIAUGA B, MISEVIČIENĒ L, RICH M H, et al. Mechanism of two-/four-electron reduction of nitroaromatics by oxygen-insensitive nitroreductases: the role of a non-enzymatic reduction step[J]. Molecules, 2018, 23(7): 1672. DOI:10.3390/molecules23071672 |




